nur für Forschungszwecke
AZD5363 (Capivasertib) Akt Inhibitor
Kat.-Nr.S8019
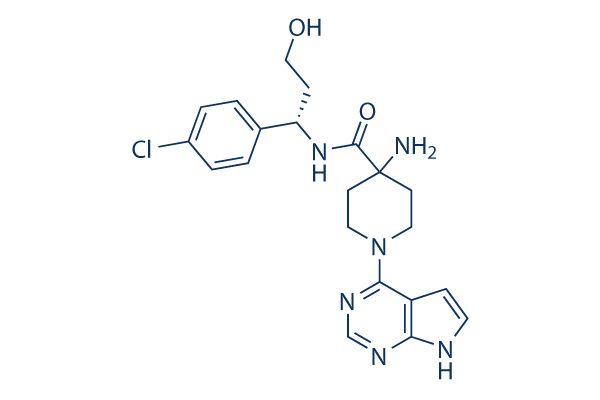
Chemische Struktur
Molekulargewicht: 428.92
Qualitätskontrolle
| Verwandte Ziele | PI3K mTOR GSK-3 ATM/ATR DNA-PK AMPK PDPK1 PTEN PP2A PDK |
|---|---|
| Weitere Akt Inhibitoren | SC79 MK-2206 Dihydrochloride Ipatasertib (GDC-0068) Perifosine GSK690693 Triciribine (API-2) Afuresertib (GSK2110183) CCT128930 A-674563 HCl Akti-1/2 |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| PC-3 | Function Assay | 10 μM | 12 h | induces autophagy | 23258740 | |
| LNCaP | Cell Viability Assay | 0-1000 nM | 0-4 d | reduced LNCaP cell viability in a dose- and time-dependent manner | 23258740 | |
| DU145 | Function Assay | 0.5/1/10 μM | 48 h | downregulates the phosphorylation of downstream pathway proteins in a dose-dependent manner | 23258740 | |
| PC-3 | Function Assay | 0.5/1/10 μM | 48 h | downregulates the phosphorylation of downstream pathway proteins in a dose-dependent manner | 23258740 | |
| C4-2 | Growth Inhibition Assay | 100-5000 nM | 72 h | increases the fraction of cells undergoing cell death | 23966621 | |
| LNCaP | Growth Inhibition Assay | 100-5000 nM | 72 h | increases the fraction of cells undergoing cell death | 23966621 | |
| C4-2 | Growth Inhibition Assay | 1-10000 nM | 0-3 d | inhibits cell viability dose dependently | 23966621 | |
| LNCaP | Growth Inhibition Assay | 1-10000 nM | 0-3 d | inhibits cell viability dose dependently | 23966621 | |
| C4-2 | Function Assay | 5 μM | 0-24 h | inhibits phosphorylation of the distal AKT-pathway biomarkers including PRAS40, eIF4E, 4E-BP1, mTOR, and P70 S6 kinase in a time-dependent manner | 23966621 | |
| LNCaP | Function Assay | 5 μM | 0-24 h | inhibits phosphorylation of the distal AKT-pathway biomarkers including PRAS40, eIF4E, 4E-BP1, mTOR, and P70 S6 kinase in a time-dependent manner | 23966621 | |
| C4-2 | Function Assay | 5 μM | 0-24 h | induces AKTS473 and AKTT308 phosphorylation in a time dependent manner | 23966621 | |
| LNCaP | Function Assay | 5 μM | 0-24 h | induces AKTS473 and AKTT308 phosphorylation in a time dependent manner | 23966621 | |
| PAMC82 | Growth Inhibition Assay | IC50=30 μM | 24088382 | |||
| MKN74 | Growth Inhibition Assay | IC50=30 μM | 24088382 | |||
| GTL-16 | Growth Inhibition Assay | IC50=30 μM | 24088382 | |||
| SNU-5 | Growth Inhibition Assay | IC50=30 μM | 24088382 | |||
| NUGC-4 | Growth Inhibition Assay | IC50=30 μM | 24088382 | |||
| SNU-216 | Growth Inhibition Assay | IC50=30 μM | 24088382 | |||
| AZ521 | Growth Inhibition Assay | IC50=25.448 μM | 24088382 | |||
| NUGC-3 | Growth Inhibition Assay | IC50=21.873 μM | 24088382 | |||
| OCUM-1 | Growth Inhibition Assay | IC50=14.515 μM | 24088382 | |||
| SNU-16 | Growth Inhibition Assay | IC50=11.097 μM | 24088382 | |||
| SNU-484 | Growth Inhibition Assay | IC50=7.392 μM | 24088382 | |||
| KATO III | Growth Inhibition Assay | IC50=7.267 μM | 24088382 | |||
| HS746T | Growth Inhibition Assay | IC50=6.084 μM | 24088382 | |||
| SNU-668 | Growth Inhibition Assay | IC50=6.003 μM | 24088382 | |||
| SNU-601 | Growth Inhibition Assay | IC50=5.938 μM | 24088382 | |||
| SNU-1 | Growth Inhibition Assay | IC50=5.258 μM | 24088382 | |||
| SNU-638 | Growth Inhibition Assay | IC50=4.523 μM | 24088382 | |||
| SNU-620 | Growth Inhibition Assay | IC50=3.384 μM | 24088382 | |||
| MKN1 | Growth Inhibition Assay | IC50=2.421 μM | 24088382 | |||
| 23132/87 | Growth Inhibition Assay | IC50=1.671 μM | 24088382 | |||
| NCI-N87 | Growth Inhibition Assay | IC50=1.037 μM | 24088382 | |||
| AGS | Growth Inhibition Assay | IC50=0.552 μM | 24088382 | |||
| IM95m | Growth Inhibition Assay | IC50=0.51 μM | 24088382 | |||
| HGC27 | Growth Inhibition Assay | IC50=0.445 μM | 24088382 | |||
| PC-9 | Function Assay | 1/5/10 μM | 4/24 h | increases AKT phosphorylation | 24957682 | |
| NCI-H522 | Function Assay | 1/5/10 μM | 4/24 h | increases AKT phosphorylation | 24957682 | |
| PC-9 | Growth Inhibition Assay | IC50=9.3 (±1.2) μM | 24957682 | |||
| NCI-H522 | Growth Inhibition Assay | IC50=11.3 (±2.7) μM | 24957682 | |||
| MR49F | Growth Inhibition Assay | 0-5 μM | 48 h | inhibits cell growth in a dose dependent manner | 25151012 | |
| MR49C | Growth Inhibition Assay | 0-5 μM | 48 h | inhibits cell growth in a dose dependent manner | 25151012 | |
| SKBR3 | Growth Inhibition Assay | 0-1.35 μM | 5 d | enhances the growth inhibition of AZD8931 | 26095475 | |
| KPL4 | Growth Inhibition Assay | 0-1.35 μM | 5 d | enhances the growth inhibition of AZD8931 | 26095475 | |
| BT474c | Growth Inhibition Assay | 0-1.35 μM | 5 d | enhances the growth inhibition of AZD8931 | 26095475 | |
| HCC1954 | Growth Inhibition Assay | 0-1.35 μM | 5 d | enhances the growth inhibition of AZD8931 | 26095475 | |
| TamR | Growth Inhibition Assay | 400 nM | 6 d | increased drug sensitivity of 4-OHT and fulvestrant | 26351323 | |
| T74D LTED | Growth Inhibition Assay | 100 nM | 6 d | increased drug sensitivity of 4-OHT and fulvestrant | 26351323 | |
| ZR75 LTED | Growth Inhibition Assay | 100 nM | 6 d | increased drug sensitivity of 4-OHT and fulvestrant | 26351323 | |
| MCF7 LTED | Growth Inhibition Assay | 200 nM | 6 d | increased drug sensitivity of 4-OHT and fulvestrant | 26351323 | |
| 1%MCF7 | Growth Inhibition Assay | 400 nM | 6 d | increased drug sensitivity of 4-OHT and fulvestrant | 26351323 | |
| T74D | Growth Inhibition Assay | 100 nM | 6 d | increased drug sensitivity of 4-OHT and fulvestrant | 26351323 | |
| ZR75 | Growth Inhibition Assay | 100 nM | 6 d | increased drug sensitivity of 4-OHT and fulvestrant | 26351323 | |
| MCF7 | Growth Inhibition Assay | 200 nM | 6 d | increased drug sensitivity of 4-OHT and fulvestrant | 26351323 | |
| LNCaP | Function assay | Inhibition of Akt in PTEN-deficient human LNCaP cells assessed as phosphorylation of GSK3beta, IC50 = 0.06 μM. | 23394218 | |||
| MDA-MB-468 | Function assay | 2 hrs | Inhibition of Akt in human MDA-MB-468 cells assessed as inhibition of GSK3beta phosphorylation after 2 hrs by laser scanning cytometry, IC50 = 0.089 μM. | 23394218 | ||
| LNCaP | Function assay | Inhibition of Akt in PTEN-deficient human LNCaP cells assessed as phosphorylation of PRAS40, IC50 = 0.22 μM. | 23394218 | |||
| BT474c | Function assay | Inhibition of Akt in human BT474c cells harboring HER2+/PIK3CA double mutant assessed as phosphorylation of PRAS40, IC50 = 0.31 μM. | 23394218 | |||
| MDA-MB-468 | Function assay | Inhibition of Akt in PTEN-deficient human MDA-MB-468 cells assessed as phosphorylation of GSK3beta, IC50 = 0.38 μM. | 23394218 | |||
| MDA-MB-468 | Function assay | Inhibition of Akt in PTEN-deficient human MDA-MB-468 cells assessed as phosphorylation of PRAS40, IC50 = 0.39 μM. | 23394218 | |||
| BT474c | Function assay | Inhibition of Akt in human BT474c cells harboring HER2+/PIK3CA double mutant assessed as phosphorylation of GSK3beta, IC50 = 0.76 μM. | 23394218 | |||
| RT4 | Function assay | Inhibition of PKA in TSC1 deficient human RT4 cells assessed as S6 phosphorylation, IC50 = 1 μM. | 23394218 | |||
| RT4 | Function assay | Inhibition of P70S6K in TSC1 deficient human RT4 cells assessed as S6 phosphorylation, IC50 = 5 μM. | 23394218 | |||
| PTEN-null LNCAP | Function assay | 1 hr | Inhibition of Akt in human PTEN-null LNCAP cells assessed as suppression in PRAS40 phosphorylation after 1 hr by ELISA analysis, IC50 = 0.3368 μM. | 27089211 | ||
| HCT116 | Antiproliferative assay | 72 hrs | Antiproliferative activity against human HCT116 cells after 72 hrs by SRB assay, IC50 = 5.2 μM. | 27089211 | ||
| OVCAR8 | Antiproliferative assay | 72 hrs | Antiproliferative activity against human OVCAR8 cells after 72 hrs by SRB assay, IC50 = 7.27 μM. | 27089211 | ||
| A673 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for A673 cells | 29435139 | |||
| DAOY | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for DAOY cells | 29435139 | |||
| Saos-2 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Saos-2 cells | 29435139 | |||
| SK-N-SH | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SK-N-SH cells | 29435139 | |||
| NB1643 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for NB1643 cells | 29435139 | |||
| MG 63 (6-TG R) | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for MG 63 (6-TG R) cells | 29435139 | |||
| Rh41 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Rh41 cells | 29435139 | |||
| SK-N-MC | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SK-N-MC cells | 29435139 | |||
| NB-EBc1 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for NB-EBc1 cells | 29435139 | |||
| LAN-5 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for LAN-5 cells | 29435139 | |||
| Rh18 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Rh18 cells | 29435139 | |||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 428.92 | Formel | C21H25ClN6O2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1143532-39-1 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | C1CN(CCC1(C(=O)NC(CCO)C2=CC=C(C=C2)Cl)N)C3=NC=NC4=C3C=CN4 | ||
Löslichkeit
|
In vitro |
DMSO
: 86 mg/mL
(200.5 mM)
Ethanol : 20 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
Moderate präklinische Verträglichkeit und PD-Eigenschaften eines Akt-Inhibitors. Deutlich unterschiedliches Profil zu anderen Akt-Inhibitoren in der klinischen Entwicklung.
|
|---|---|
| Targets/IC50/Ki |
Akt1
(Cell-free assay) 3 nM
Akt2
(Cell-free assay) 8 nM
Akt3
(Cell-free assay) 8 nM
ROCK2
(Cell-free assay) 56 nM
|
| In vitro |
Capivasertib (AZD5363) ist ein potenter Akt-Inhibitor mit IC50 von 3 nM, 8 nM und 8 nM für Akt1, Akt2 bzw. Akt3. Es hemmt die Phosphorylierung von Akt-Substraten in Zellen mit einer Potenz von etwa 0,3 bis 0,8 μM. Diese Verbindung hemmt die Proliferation von 41 von 182 soliden und hämatologischen Tumorzelllinien mit einer Potenz von < 3 μM. Aktivierende Mutationen in PIK3CA, Verlust oder Inaktivierung des Tumorsuppressors PTEN oder HER2-Amplifikation sind alle signifikant prädiktiv für das Ansprechen auf AZD5363. Zusätzlich wird auch eine Korrelation zwischen dem RAS-Mutationsstatus von Zelllinien und der Resistenz dagegen beobachtet. |
| Kinase-Assay |
Caliper Off-Chip Inkubation Mobilität Shift Assay
|
|
Die Fähigkeit von Capivasertib (AZD5363) und anderen Verbindungen, die Aktivität von AKT1, AKT2 und AKT3 zu hemmen, wird mittels des Caliper Off-Chip Incubation Mobility Shift Assays bewertet. Aktive rekombinante AKT1, AKT2 oder AKT3 werden mit einem 5-FAM-markierten, kundenspezifisch synthetisierten Peptidsubstrat zusammen mit steigenden Konzentrationen dieser Verbindung inkubiert. Die finalen Reaktionen enthielten 1 bis 3 nM AKT1-, AKT2- oder AKT3-Enzyme; 1,5 mM Peptidsubstrat; ATP bei K m für jede AKT-Isoform; 10 mM MgCl2, 4 mM DTT, 100 mM HEPES und 0,015 % Brij-35. Die Reaktionen werden 1 Stunde bei Raumtemperatur inkubiert und durch Zugabe eines Puffers gestoppt, der 100 mM HEPES, 0,015 % Brij-35-Lösung, 0,1 % Beschichtungsreagenz, 40 mM EDTA und 5 % DMSO enthält. Die Platten werden dann mit einem Caliper LC3000 analysiert, was die Trennung von Peptidsubstrat und phosphoryliertem Produkt durch Elektrophorese mit anschließender Detektion und Quantifizierung der laserinduzierten Fluoreszenz ermöglicht.
|
|
| In vivo |
Die orale Verabreichung von Capivasertib (AZD5363) (100, 300 mg/kg) an Nacktmäuse führt zu dosis- und zeitabhängigen Reduktionen der PRAS40-, GSK3β- und S6-Phosphorylierung in BT474c-Xenotransplantaten, reversiblen Erhöhungen der Blutglukosekonzentrationen und dosisabhängigen Abnahmen der 2[18F]Fluor-2-deoxy-d-glukose (18F-FDG)-Aufnahme in U87-MG-Xenotransplantaten. Die chronische orale Verabreichung dieser Verbindung (130, 200 und 300 mg/kg) führt zu einer dosisabhängigen Wachstumshemmung von Xenotransplantaten, die von verschiedenen Tumortypen stammen, einschließlich HER2+-Brustkrebsmodellen. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | pAKT / AKT / pGSK3β / GSK3β HER3 / pHER3 / HER2 / pHER2 / pPRAS40 / pS6 / p-4EBP1 / pFOXO / pERK / PARP / Cleaved PARP |
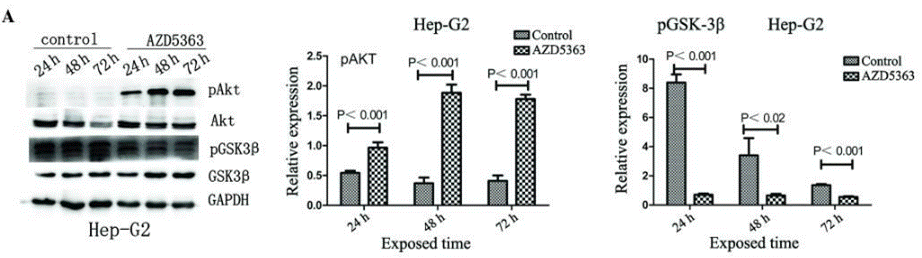
|
26998062 |
| Immunofluorescence | p-Chk2 / γ-H2AX |
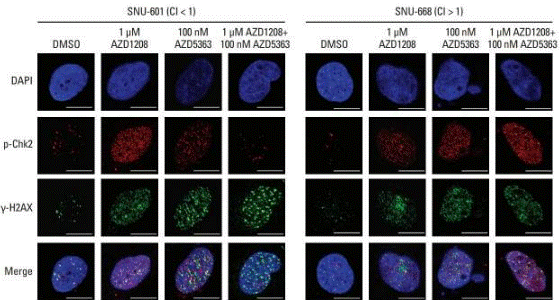
|
29879757 |
| Growth inhibition assay | Cell viability |
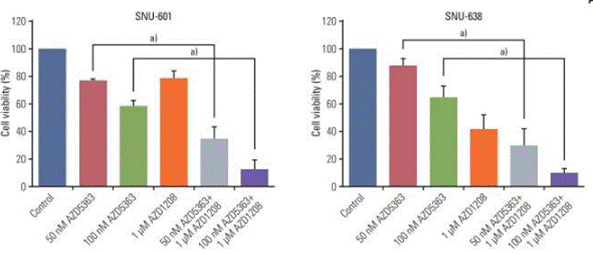
|
29879757 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT03310541 | Completed | Breast Cancer|Prostate Cancer|Advanced Solid Tumors |
Memorial Sloan Kettering Cancer Center |
October 11 2017 | Phase 1 |
| NCT01992952 | Active not recruiting | Estrogen Receptor Positive Breast Cancer |
Velindre NHS Trust|AstraZeneca|Cenduit LLC|Covance|Cardiff and Vale University Health Board |
May 2014 | Phase 1|Phase 2 |
| NCT02338622 | Completed | Advanced Cancer |
Royal Marsden NHS Foundation Trust|Institute of Cancer Research United Kingdom|AstraZeneca |
March 31 2014 | Phase 1 |
| NCT02121639 | Completed | Prostate Cancer |
University Hospital Southampton NHS Foundation Trust|AstraZeneca|Cancer Research UK |
January 29 2014 | Phase 1|Phase 2 |
| NCT02077569 | Completed | Invasive Breast Cancer |
University of Nottingham|AstraZeneca|Cancer Research UK|National Cancer Research Network |
January 2014 | Phase 2 |
| NCT01692262 | Completed | Metastatic Castrate-Resistant Prostate Cancer (mCRPC)|Efficacy|Safety and Tolerability|Pharmacokinetics|Pharmacodynamics|Tumour Response. |
AstraZeneca |
November 2012 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
