nur für Forschungszwecke
CCT128930 Akt Inhibitor
Kat.-Nr.S2635
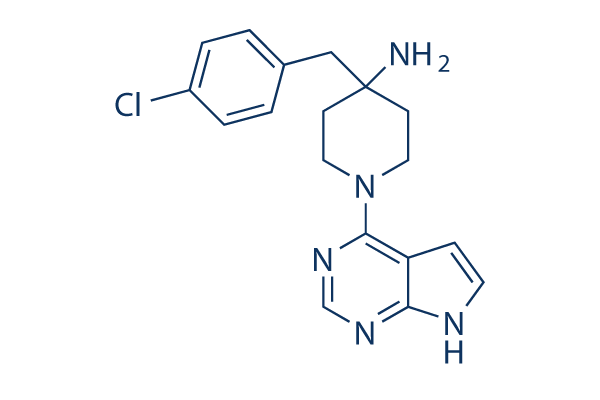
Chemische Struktur
Molekulargewicht: 341.84
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- HPLC
- SDS
- Datenblatt
| Verwandte Ziele | PI3K mTOR GSK-3 ATM/ATR DNA-PK AMPK PDPK1 PTEN PP2A PDK |
|---|---|
| Weitere Akt Inhibitoren | SC79 AZD5363 (Capivasertib) MK-2206 Dihydrochloride Ipatasertib (GDC-0068) Perifosine GSK690693 Triciribine (API-2) Afuresertib (GSK2110183) A-674563 HCl Akti-1/2 |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| U87MG cells | Function assay | Inhibition of PKB in human U87MG cells assessed as GSK3-beta phosphorylation by ELISA, IC50=0.66 nM | ||||
| PC3M cells | Function assay | Inhibition of PKB in human PC3M cells assessed as GSK3-beta phosphorylation by ELISA, IC50=0.003 μM | ||||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 341.84 | Formel | C18H20ClN5 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 885499-61-6 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | C1CN(CCC1(CC2=CC=C(C=C2)Cl)N)C3=NC=NC4=C3C=CN4 | ||
Löslichkeit
|
In vitro |
DMSO
: 25 mg/mL
(73.13 mM)
Ethanol : 5 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Akt2
(Cell-free assay) 6 nM
p70 S6K
(Cell-free assay) 120 nM
PKA
(Cell-free assay) 168 nM
|
|---|---|
| In vitro |
CCT128930 zeigt eine ausgeprägte antiproliferative Aktivität gegen PTEN-defiziente humane Tumorzelllinien, einschließlich U87MG-Glioblastomzellen, LNCaP-Prostatakrebszellen und PC3-Prostatakrebszellen, mit GI50-Werten von 6,3 μM, 0,35 μM bzw. 1,9 μM. Darüber hinaus verursacht diese Verbindung einen G1-Arrest in PTEN-null U87MG-Glioblastomzellen und eine Blockade des Akt-Signalwegs.
|
| Kinase-Assay |
Kinase-Assays
|
|
Das Profiling gegen 50 verschiedene humane Kinasen wird unter Verwendung von 10 μM CCT128930 bei einer ATP-Konzentration durchgeführt, die der Km für jedes Enzym entspricht.
|
|
| In vivo |
CCT128930 bei 25 mg/kg i.p. zeigt einen ausgeprägten Antitumor-Effekt in etablierten PTEN-null U87MG-Glioblastom-Xenotransplantaten mit einem Behandlungs:Kontroll (T/C)-Verhältnis von 48% am Tag 12. In HER2-positiven, PIK3CA-mutierten BT474-Brustkrebs-Xenotransplantaten führt diese Verbindung bei 40 mg/kg ebenfalls zu einem tiefgreifenden Antitumor-Effekt mit vollständigem Wachstumsstillstand und einem T/C-Verhältnis von 29% am Tag 22. Diese chemische Substanz, intravenös verabreicht, erreicht eine Spitzenkonzentration von 6,4 μM im Plasma und wird mit einer relativ kurzen Halbwertszeit, einem hohen Verteilungsvolumen und einer schnellen Clearance eliminiert, was eine Fläche unter der Kurve AUC0-∞ von 4,6 μM·h ergibt. Intraperitoneal verabreicht, führt es zu einer Spitzen-Plasmakonzentration von 1,3 μM und der entsprechenden AUC0-∞ von 1,3 μM·h. Die orale Verabreichung dieser Verbindung führt zu einer Spitzen-Plasmakonzentration von nur 0,43 μM und einer entsprechend niedrigen AUC0-∞ von 0,4 μM·h.
|
Literatur |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
