nur für Forschungszwecke
GGTI 298 TFA salt Transferase Inhibitor
Kat.-Nr.S7466
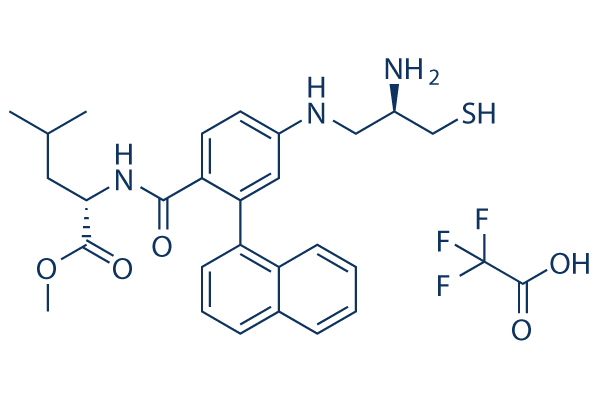
Chemische Struktur
Molekulargewicht: 593.66
Qualitätskontrolle
- Zitiert in Nature Medicine für seine erstklassige Qualität
- COA
- NMR
-
Warum Mikroanalyse?
- Datenblatt
- SDS
- Zitiert in Nature Medicine für seine erstklassige Qualität
- COA
- NMR
- Datenblatt
- SDS
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 593.66 | Formel | C27H33N3O3S.C2HF3O2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1217457-86-7 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC(C)CC(C(=O)OC)NC(=O)C1=C(C=C(C=C1)NCC(CS)N)C2=CC=CC3=CC=CC=C32.C(=O)(C(F)(F)F)O | ||
Löslichkeit
|
In vitro |
DMSO
: 100 mg/mL
(168.44 mM)
Ethanol : 100 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
GGTase I
|
|---|---|
| In vitro |
Es wurde gezeigt, dass der Geranylgeranyltransferase-I-Inhibitor GGTI-298 menschliche Tumorzellen in der G1-Phase des Zellzyklus arretiert und Apoptose induziert. Die Behandlung der menschlichen Lungenkarzinomzelllinie Calu-1 mit GGTI-298 führt zu einer Hemmung der Phosphorylierung des Retinoblastomproteins, einem kritischen Schritt für den G1/S-Übergang. Die Kinaseaktivitäten zweier G1/S-Cyclin-abhängiger Kinasen, CDK2 und CDK4, werden in Calu-1-Zellen, die mit GGTI-298 behandelt wurden, gehemmt. GGTI-298 hat wenig Einfluss auf die Expressionsniveaus von CDK2, CDK4, CDK6, Cyclinen D1 und E, verringert aber die Niveaus von Cyclin A. GGTI-298 erhöht die Niveaus der Cyclin-abhängigen Kinase-Inhibitoren p21 und p15 und hatte wenig Einfluss auf die von p27 und p16. GGTI-298 fördert die Bindung von p21 und p27 an CDK2, während es deren Bindung an CDK6 verringert. Die Behandlung führt zu einer erhöhten Bindung von p15 an CDK4, was mit einer verringerten Bindung an p27 einhergeht. Die Vorbehandlung von Fibroblasten mit GGTI-298 blockiert die PDGF- und Epidermal-Growth-Factor-abhängige Tyrosinphosphorylierung ihrer entsprechenden Tyrosinkinase-Rezeptoren. GGTI-298 hat antiproliferative Effekte auf Fibroblasten, Epithel- und glatte Muskelzellen, und diese Zellwachstumshemmung scheint durch einen G1-Phasen-Arrest vermittelt zu werden. |
| In vivo |
GGTI-298 hemmt das Tumorwachstum bei Nacktmäusen. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | p-IκB-α / IκB-α |
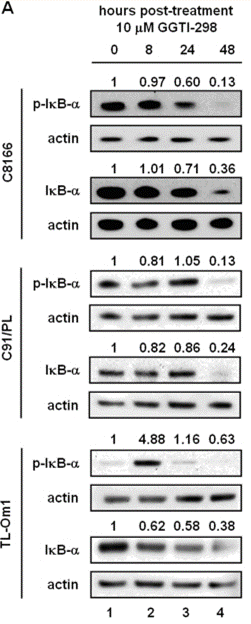
|
22069517 |
| Growth inhibition assay | Cell viability |
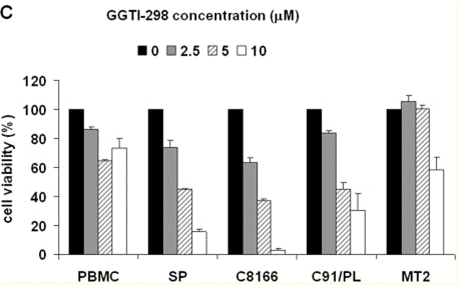
|
22069517 |
| Immunofluorescence | YAP |
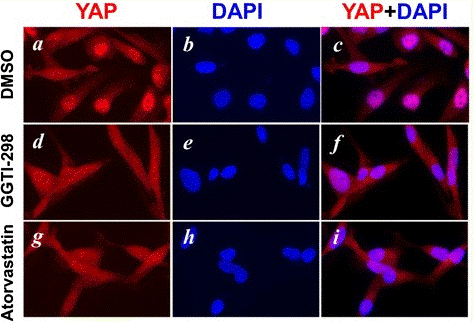
|
25745361 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
