nur für Forschungszwecke
Palonosetron 5-HT Receptor Antagonist
Kat.-Nr.S5740
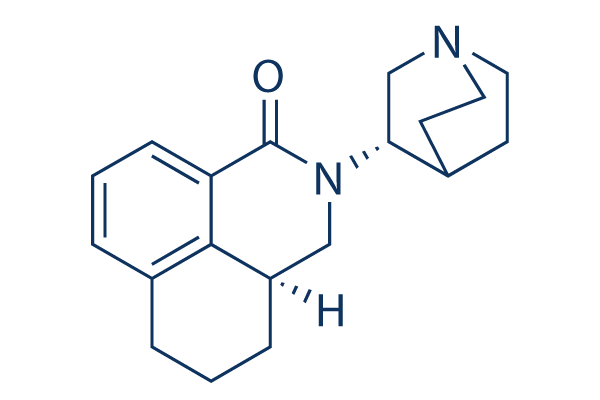
Chemische Struktur
Molekulargewicht: 296.41
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- SDS
- Datenblatt
| Verwandte Ziele | Adrenergic Receptor AChR COX Calcium Channel Histamine Receptor Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Weitere 5-HT Receptor Inhibitoren | WAY-100635 Maleate Serotonin (5-HT) HCl Puerarin BRL-15572 Dihydrochloride SB269970 HCl Ketanserin RS-127445 Nuciferine Flopropione BRL-54443 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 296.41 | Formel | C19H24N2O |
Lagerung (Ab dem Eingangsdatum) | 3 years -20°C powder |
|---|---|---|---|---|---|
| CAS-Nr. | 135729-61-2 | -- | Lagerung von Stammlösungen |
|
|
| Synonyme | RS25259, RS 25259 197 | Smiles | C1CC2CN(C(=O)C3=CC=CC(=C23)C1)C4CN5CCC4CC5 | ||
Löslichkeit
|
In vitro |
DMSO
: 59 mg/mL
(199.04 mM)
|
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
5-HT3 receptor
0.17 nM(Ki)
|
|---|---|
| In vitro |
Diese Verbindung ist ein 5-HT3 receptor Antagonist mit einer hohen Bindungsaffinität für diesen Rezeptor und geringer oder keiner Affinität für andere Rezeptoren. |
| In vivo |
Palonosetron hat eine längere Halbwertszeit und eine höhere Bindungsaffinität als die 5-HT3 receptor Antagonisten der ersten Generation. Nach intravenöser Verabreichung dieser Verbindung bei gesunden Probanden und Krebspatienten folgt auf einen anfänglichen Rückgang der Plasmakonzentration eine langsame Elimination aus dem Körper. Die mittlere maximale Plasmakonzentration und die Fläche unter den Konzentrations-Zeit-Kurven sind im Allgemeinen dosisproportional im Dosisbereich von 0,3 bis 90 μg/kg bei gesunden Probanden und bei Krebspatienten. Diese Verbindung hat ein Verteilungsvolumen von ungefähr 8,3 ± 2,5 L/kg und ist zu 62% an Plasmaproteine gebunden. Es wird durch renale Ausscheidung und metabolische Wege aus dem Körper eliminiert. Die mittlere terminale Eliminationshalbwertszeit beträgt ungefähr 40 Stunden. |
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT04486157 | Completed | Healthy |
HK inno.N Corporation |
March 18 2021 | Phase 1 |
| NCT04466046 | Completed | Postoperative Nausea and Vomiting |
Daegu Catholic University Medical Center |
September 4 2019 | -- |
| NCT03148704 | Unknown status | Palonosetron |
Cttq |
March 8 2017 | -- |
| NCT00982995 | Terminated | Nausea|Vomiting|Terminally Ill |
University of Michigan Rogel Cancer Center |
November 2010 | Phase 2 |
| NCT01074697 | Completed | Nausea|Vomiting|Genital Neoplasms Female |
Odense University Hospital|Helsinn Healthcare SA |
April 2010 | Phase 3 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
