nur für Forschungszwecke
SB705498 TRP Channel Antagonist
Kat.-Nr.S2773
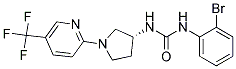
Chemische Struktur
Molekulargewicht: 429.23
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- HPLC
- SDS
- Datenblatt
| Verwandte Ziele | CFTR CRM1 CD markers AChR Calcium Channel Sodium Channel Potassium Channel GABA Receptor ATPase GluR |
|---|---|
| Weitere TRP Channel Inhibitoren | 2-APB (2-Aminoethyl Diphenylborinate) SKF96365 AMG-517 GSK2193874 GSK1016790A HC-030031 Capsazepine EIPA (L593754) HC-067047 ML-SI3 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 429.23 | Formel | C17H16BrF3N4O |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 501951-42-4 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | C1CN(CC1NC(=O)NC2=CC=CC=C2Br)C3=NC=C(C=C3)C(F)(F)F | ||
Löslichkeit
|
In vitro |
DMSO
: 86 mg/mL
(200.35 mM)
Ethanol : 20 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
hTRPV1
7.6(pKi)
hTRPV1
7.1(pIC50)
|
|---|---|
| In vitro |
SB705498 (0,3 nM-1 μM) hemmt potent die Capsaicin-induzierte Aktivierung von menschlichem TRPV1, das in 1321N1-Zellen oder HEK293-Zellen exprimiert wird, mit scheinbaren pKi-Werten von 7,5 bzw. 7,6. Die gleichzeitige Applikation von 100 nM dieser Verbindung hemmt schnell, vollständig und reversibel hTRPV1, das in HEK293-Zellen exprimiert wird. Diese Chemikalie hat keinen signifikanten Effekt auf endogene [Ca2+]-Antworten in HEK293-Zellen, die durch muskarinische Acetylcholinrezeptoraktivierung mit Carbachol oder Speicher-gesteuerte Kanal-vermittelte Ca2+-Aufnahme nach Depletion intrazellulärer Speicher mit dem Ca2+-Pumpen-Inhibitor Thapsigargin hervorgerufen werden. Diese Verbindung (10 pM-1 μM) hat auch keinen signifikanten antagonistischen Effekt gegenüber dem eng verwandten TRPV1-Rezeptor-Paralog TRPV4, der transient in HEK293-Zellen exprimiert und mit dem synthetischen Liganden 4α-Phorbol-12,13-didecanoat (10 μM) aktiviert wird. Diese Chemikalie zeigt eine gute antagonistische Potenz sowohl gegen das Ratten- als auch das Meerschweinchen-TRPV1. Sie antagonisiert Ratten- und Meerschweinchen-TRPV1 mit pKi-Werten von 7,5 bzw. 7,3. Die gleichzeitige Applikation von 100 nM bis 10 μM dieser Verbindung zum Gleichgewichtszustand einer aufrechterhaltenen Capsaicin-Antwort führt zu einer schnellen und vollständigen Hemmung von hTRPV1 bei -70 mV. Sie hemmt die Capsaicin-vermittelte Aktivierung von hTRPV1 mit einer IC50 von 3 nM und 17 nM bei positiven bzw. negativen Haltepotentialen (-70 mV und +70 mV). Die gleichzeitige Applikation von 1 μM dieser Chemikalie während der Plateauphase der Antwort führt zu einer vollständigen und reversiblen Hemmung der TRPV1-vermittelten Leitfähigkeit. Diese Verbindung zeigt eine annähernd gleiche Aktivität gegenüber multiplen und diversen chemischen und physikalischen Aktivierungsmodi des TRPV1-Rezeptors. Sie zeigt wenig oder keine Aktivität gegenüber einer Vielzahl von Ionenkanälen, Rezeptoren und Enzymen. Diese Chemikalie bewirkt eine vollständige Blockade der Wärme- sowie der pH-Aktivierung von hTRPV1.
|
| In vivo |
SB705498 zeigt eine potente und reversible Blockade gegen die multiplen Aktivierungsmodi von TRPV1, nämlich die Vanilloid- (Capsaicin-), Wärme- und säurevermittelte Aktivierung des Rezeptors. Diese Verbindung zeigt eine ausgezeichnete Aktivität bei 10 und 30 mg/kg p.o. mit guter Reversion der Allodynie. Es wurde auch gezeigt, dass es im Meerschweinchen-FCA-Modell bei 10 mg/kg p.o. eine 80%ige Reversion der Allodynie bewirkt.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT01476098 | Completed | Rhinitis |
GlaxoSmithKline |
April 2011 | Phase 2 |
| NCT01424397 | Completed | Rhinitis |
GlaxoSmithKline |
April 14 2011 | Phase 2 |
| NCT01424514 | Completed | Rhinitis |
GlaxoSmithKline |
December 1 2010 | Phase 2 |
| NCT01439308 | Completed | Rhinitis |
GlaxoSmithKline |
December 2009 | Phase 2 |
| NCT00461682 | Terminated | Irritable Colon |
GlaxoSmithKline |
January 26 2007 | Phase 2 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
