nur für Forschungszwecke
Syringic acid Antioxidant Chemikalie
Kat.-Nr.S3629
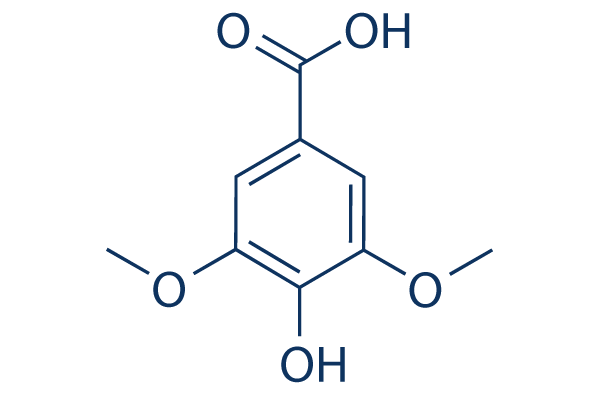
Chemische Struktur
Molekulargewicht: 198.17
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- SDS
- Datenblatt
| Verwandte Ziele | EGFR VEGFR JAK PDGFR FGFR Src HIF FLT FLT3 HER2 |
|---|---|
| Weitere Antioxidant Inhibitoren | Elamipretide (SS-31, MTP-131) Tangeretin (+)-Catechin Silymarin Oleuropein (-)Epicatechin Hydroxygenkwanin Cocoa Extract Sesamol Flavanone |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 198.17 | Formel | C9H10O5 |
Lagerung (Ab dem Eingangsdatum) | 3 years -20°C powder (seal) |
|---|---|---|---|---|---|
| CAS-Nr. | 530-57-4 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | 3,5-dimethyl ether Gallic Acid, 3,5-dimethoxy-4-hydroxy Benzoic Acid, NSC 2129, SYRA | Smiles | COC1=CC(=CC(=C1O)OC)C(=O)O | ||
Löslichkeit
|
In vitro |
DMSO
: 39 mg/mL
(196.8 mM)
Ethanol : 39 mg/mL Water : 1 mg/mL |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| In vitro |
Syringic acid verbessert die Expressionen von TH, DAT und VMAT2 und schwächt auch signifikant die MPTP/p2-induzierte erhöhte Expression von Entzündungsmarkern ab. Diese Vorbehandlung mit der Verbindung hemmt offensichtlich die H2O2-induzierte RGC-5-Zellschädigung und verringert auch die H2O2-induzierte ROS-Produktion und den MDA-Gehalt. Sie kann RGC-5-Zellen vor Apoptose schützen, die durch H2O2 induziert wird, durch die Aktivierung des PI3K/Akt-Signalwegs. Diese Chemikalie zeigt eine zeit- und dosisabhängige (IC50 = 0,95-1,2 mg/mL) antimitogene Wirkung gegen Krebszellen mit geringer Zytotoxizität auf normale Fibroblasten (≤20%). Sie verändert den Zellzyklus (S/G2-M- oder G1/G2-M-Phasen) in einer zeitabhängigen Weise, induziert Apoptose, hemmt die DNA-Bindungsaktivität von NFκB (p ≤ 0,0001), chymotrypsinähnliche/PGPH (peptidyl-glutamyl peptide-hydrolyzing) (p ≤ 0,0001) und die trypsinähnlichen (p ≤ 0,002) Aktivitäten des 26S-Proteasoms und Angiogenesis. Es sensibilisiert Krebszellen auch differential für Standard-Chemotherapien mit einem deutlichen Anstieg ihrer Empfindlichkeit gegenüber Camptothecin (500-fach), 5FU (20.000-fach), Doxorubicin (210-fach), Taxol (3134-fach), Vinblastin (1000-fach), Vincristin (130-fach) und Amsacrin (107-fach) im Vergleich zu alleinigen Standardmedikamenten. Diese Verbindung übt ihre chemotherapeutischen und chemosensibilisierenden Effekte durch eine Reihe von Mechanismen aus, darunter Zellzyklusarrest, Apoptoseinduktion, Hemmung der Zellproliferation, Zellmigration, Angiogenesis, NFκB-DNA-Bindung und Proteasomaktivitäten. |
|---|---|
| In vivo |
Syringic acid hat hepatoprotektive Wirkungen in verschiedenen Tiermodellen. Die orale Verabreichung dieser Verbindung (10 mg/kg Körpergewicht) wurde als teilweise Wiederherstellung von Lern- und Gedächtnisstörungen durch Amyloid-β-induzierte Neurotoxizität bei Mäusen berichtet. Es erleichtert auch schützende Wirkungen auf die Niere bei Nierenischämie-Reperfusion-Verletzungen. Antimikrobielle Aktivitäten dieser Chemikalie wurden auch gegen verschiedene Krankheitserreger berichtet. Die Antikrebswirkungen wurden an A549-Lungenkarzinomzellen untersucht und zeigten apoptotische Wirkungen mit einem IC50 von 30 μM. Diese Säure dämpft die Erhöhung der Glykoproteinkomponenten bei normalen und diabetischen Ratten. Sie kann die Insulinsekretion von Pankreas-β-Zellen erhöhen und den Plasmaglukosespiegel normalisieren. |
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT05025189 | Completed | Healthy |
University of California Los Angeles|The California Table grape Commission |
October 5 2020 | Not Applicable |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
