nur für Forschungszwecke
TEPP-46 (ML265) PKM2-Aktivator
Kat.-Nr.S7302
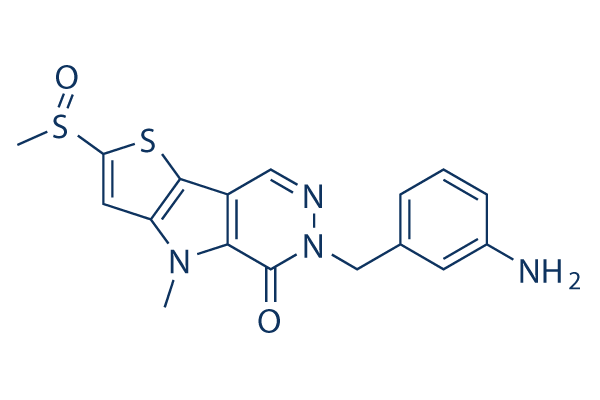
Chemische Struktur
Molekulargewicht: 372.46
Qualitätskontrolle
| Verwandte Ziele | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Weitere PKM Inhibitoren | Mitapivat (AG-348) (±)-Shikonin PKM2-IN-1 (Compound 3k) DASA-58 DL-Serine ZIP Alkannin TP-1454 |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| BL21 | Function assay | 4 uM | 50 mins | Activation of recombinant human PKM2 expressed in Escherichia coli BL21 at 4 uM incubated for 50 mins measured over 40 mins | 29641204 | |
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 372.46 | Formel | C17H16N4O2S2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1221186-53-3 | -- | Lagerung von Stammlösungen |
|
|
| Synonyme | CID-44246499, NCGC00186528 | Smiles | CN1C2=C(C3=C1C(=O)N(N=C3)CC4=CC(=CC=C4)N)SC(=C2)S(=O)C | ||
Löslichkeit
|
In vitro |
DMSO
: 72 mg/mL
(193.3 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
PKM2
|
|---|---|
| In vitro |
TEPP-46 (ML265) aktiviert PKM2 in vitro potent mit einem AC50 = 92 nM und zeigt eine hohe Selektivität gegenüber den anderen 3 Pyruvatkinase-Isoformen. Es bindet an der Dimer-Dimer-Grenzfläche des PKM2-Homotetramers und ist in der Lage, PKM2 im Zelllysat von mit Pervanadat behandelten Zellen zu aktivieren, was eine Bedingung ist, die bekanntermaßen die PKM2-Aktivität durch Akkumulation von Phosphotyrosinpeptiden hemmt. Diese Verbindung erhöhte die Verdopplungszeit von H1299-Zellen unter hypoxischen Bedingungen signifikant, zeigte aber interessanterweise keinen Effekt unter Normoxie. |
| Kinase-Assay |
PKM2-Aktivitätstest
|
|
Die Pyruvatkinase-Aktivität wird durch Überwachung der Pyruvat-abhängigen Umwandlung von NADH zu NAD+ durch Laktatdehydrogenase (LDH) gemessen. Kurz gesagt, für Zelllinienexperimente wird das Medium 1 Stunde vor Beginn der Behandlung mit DMSO oder TEPP-46 (ML265) durch frisches Medium ersetzt. Wo angegeben, werden außerdem 100 μM Pervanadat 10 Minuten vor der Zelllyse hinzugefügt. Die Zellen werden auf Eis mit RIPA-Puffer, der 2 mM DTT und Proteaseinhibitoren enthält, lysiert und durch Zentrifugation bei 21.000 × g geklärt. 5 μL des Überstands werden zur Bestimmung der Pyruvatkinase-Aktivität verwendet. Die Pyruvatkinase-Aktivität wurde anschließend auf den Gesamtproteingehalt normalisiert.
|
|
| In vivo |
In einem 7-wöchigen Maus-Xenograft-Modell (H1299-Maus-Xenograft) reduzierte die Aktivierung von PKM2 mit TEPP-46 (ML265) die Tumorgröße und das Auftreten signifikant ohne Anzeichen akuter Toxizität. Diese Verbindung zeigte auch überlegene Plasmakonzentrationen, die über die 24-Stunden-Studie hinweg auf höheren Niveaus blieben, und zeigte eine gute orale Bioverfügbarkeit, eine geringe Clearance, eine lange Halbwertszeit und ein gutes Verteilungsvolumen. . |
Literatur |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
