nur für Forschungszwecke
Abiraterone P450 (e.g. CYP17) Inhibitor
Kat.-Nr.S1123
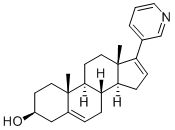
Chemische Struktur
Molekulargewicht: 349.51
Qualitätskontrolle
| Verwandte Ziele | Dehydrogenase HSP Transferase PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism Drug Metabolite |
|---|---|
| Weitere P450 (e.g. CYP17) Inhibitoren | Apigenin Baicalein Avasimibe Naringenin Diosmetin Alizarin Orteronel Benzbromarone Sodium Danshensu Naringin |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| JM109 | Growth inhibition assay | Inhibition of C-terminal His-tagged recombinant human CYP17A1delta19H mutant expressed in Escherichia coli JM109 cells assessed as decrease in progesterone hydroxylation in presence of cytochrome P450 reductase by HPLC-UV method, IC50=0.0094μM. | 29792703 | |||
| P450c17-LNCaP | Growth inhibition assay | In vitro cytochrome P450 17A1 inhibition was assayed using the rapid acetic acid releasing assay (AARA), utilizing intact P450c17-expressing Escherichia coli or P450c17-LNCaP cells as the enzyme source, IC50=0.8μM. | 12773039 | |||
| V79MZh11B1 | Growth inhibition assay | Inhibition of human CYP11B1 expressed in hamster V79MZh11B1 cells, IC50=1.608μM. | 18672868 | |||
| V79MZh11B1 | Growth inhibition assay | Inhibition of recombinant CYP11B1 expressed in expressed in V79MZh11B1 cells, IC50=1.608μM. | 19211174 | |||
| V79MZh | Growth inhibition assay | Inhibition of human CYP11B1 expressed in hamster V79MZh cells, IC50=1.61μM. | 20550118 | |||
| V79MZh | Growth inhibition assay | Inhibition of human CYP11B1 expressed in hamster V79MZh cells using [1,2-3H]-11-deoxycorticosterone as substrate, IC50=1.61μM. | 23859149 | |||
| V79MZh | Growth inhibition assay | Inhibition of human CYP11B2 expressed in hamster V79MZh cells, IC50=1.75μM. | 20550118 | |||
| V79MZh | Growth inhibition assay | Inhibition of human CYP11B2 expressed in hamster V79MZh cells using [1,2-3H]-11-deoxycorticosterone as substrate, IC50=1.75μM. | 23859149 | |||
| V79MZh11B2 | Growth inhibition assay | Inhibition of human CYP11B2 expressed in hamster V79MZh11B2 cells, IC50=1.751μM. | 18672868 | |||
| LNCAP | Antiproliferative assay | 72 hrs | Antiproliferative activity against human LNCAP cells after 72 hrs by MTT assay, IC50=3.29μM. | 29310026 | ||
| hTERT-BJ | Cytotoxicity assay | 48 hrs | Cytotoxicity against human hTERT-BJ cells assessed as cell growth inhibition after 48 hrs SRB assay, GI50=4.5μM. | 29172080 | ||
| PC3 | Antiproliferative assay | 72 hrs | Antiproliferative activity against human PC3 cells after 72 hrs by MTT assay, IC50=5.94μM. | 29310026 | ||
| MGC803 | Antiproliferative assay | 72 hrs | Antiproliferative activity against human MGC803 cells after 72 hrs by MTT assay, IC50=7.72μM. | 29310026 | ||
| HeLa | Antiproliferative assay | 48 hrs | Antiproliferative activity against human HeLa cells after 48 hrs by SRB assay, GI50=7.9μM. | 29172080 | ||
| PC3 | Cytotoxicity assay | 48 hrs | Cytotoxicity against human PC3 cells assessed as growth inhibition after 48 hrs by MTT assay, IC50=9.32μM. | 24148837 | ||
| GES-1 | Antiproliferative assay | 72 hrs | Antiproliferative activity against human GES-1 cells after 72 hrs by MTT assay, IC50=13.12μM. | 29310026 | ||
| T47D | Growth inhibition assay | 72 hrs | Growth inhibition of human T47D cells after 72 hrs by MTT assay, IC50=16.9μM. | 27209562 | ||
| MDA-MB-231 | Growth inhibition assay | 72 hrs | Growth inhibition of human MDA-MB-231 cells after 72 hrs by MTT assay, IC50=19.2μM. | 27209562 | ||
| MCF7 | Growth inhibition assay | 72 hrs | Growth inhibition of human MCF7 cells after 72 hrs by MTT assay, IC50=19.3μM. | 27209562 | ||
| MDA-MB-361 | Growth inhibition assay | 72 hrs | Growth inhibition of human MDA-MB-361 cells after 72 hrs by MTT assay, IC50=20.4μM. | 27209562 | ||
| T47D | Antiproliferative assay | 48 hrs | Antiproliferative activity against human T47D cells after 48 hrs by SRB assay, GI50=24μM. | 29172080 | ||
| WiDr | Antiproliferative assay | 48 hrs | Antiproliferative activity against human WiDr cells after 48 hrs by SRB assay, GI50=42μM. | 29172080 | ||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 349.51 | Formel | C24H31NO |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 154229-19-3 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | CB-7598 | Smiles | CC12CCC(CC1=CCC3C2CCC4(C3CC=C4C5=CN=CC=C5)C)O | ||
Löslichkeit
|
In vitro |
Ethanol : 0.2 mg/mL
DMSO
: 0.1 mg/mL
(0.28 mM)
Water : 0.02 mg/mL |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
Approved for the treatment of docetaxel-treated castration-resistant prostate cancer.
|
|---|---|
| Targets/IC50/Ki |
CYP17
(Cell-free assay) 2 nM
|
| In vitro |
Abiraterone bindet und hemmt den Wildtyp- und mutierten Androgen Receptor (AR). Diese Verbindung hemmt die In-vitro-Proliferation und die Androgen Receptor-regulierte Genexpression von Androgen Receptor-positiven Prostatakrebszellen, was durch Androgen Receptor-Antagonismus zusätzlich zur Hemmung der Steroidogenese erklärt werden könnte. Tatsächlich wird die Aktivierung des mutierten Androgen Receptor durch Eplerenon durch höhere Konzentrationen dieser Chemikalie gehemmt. Es verdrängt Liganden sowohl von WT-AR als auch von T877A mit einer EC50 von 13,4 μM bzw. 7,9 μM. Diese Verbindung hemmt die Lyase-Aktivität mit einer IC50 von 5,8 nM in Mikrosomen aus Rattenhoden. Abirateronacetat hemmt die T-Sekretion signifikant (−48 %) und erhöht im Gegenzug die LH-Konzentration (192 %).
|
| Kinase-Assay |
C17,20-Lyase-Aktivitätstest
|
|
Mikrosomen werden auf eine finale Proteinkonzentration von 50 μg/mL in der Reaktionsmischung verdünnt, die 0,25 M Saccharose, 20 mM Tris–HCl (pH 7,4), 10 mM G6P und 1,2 IU/mL G6PDH enthielt. Nach Äquilibrierung bei 37 °C für 10 Minuten wird die Reaktion durch Zugabe von βNADP initiiert, um eine finale Konzentration von 0,6 mM zu erhalten. Vor der Verteilung von 600 μL der Reaktionsmischung in jedes Röhrchen wird Abiraterone unter einem Stickstoffstrom zur Trockne eingedampft und dann 10 Minuten lang bei 37 °C inkubiert. Nach der Inkubation mit dieser Verbindung werden 500 μL der Reaktionsmischung in Röhrchen überführt, die 1 μM des Enzymsubstrats 17OHP enthalten. Nach weiteren 10 Minuten Inkubation werden die Röhrchen auf Eis gelegt und die Reaktion durch Zugabe von 0,1 ml NaOH 1N gestoppt. Die Röhrchen werden tiefgefroren und bei –20 °C gelagert, bis sie auf Δ4A-Spiegel untersucht werden. Ein Δ4A-RIA wird entwickelt und auf einem Mikrotiterplattenformat unter Verwendung eines spezifischen Antikörpers gegen Δ4A automatisiert. Die Trennung von freiem und gebundenem Antigen wird mit einer Dextran-beschichteten Kohlesuspension erreicht. Nach der Zentrifugation werden Aliquote des klaren Überstands in Duplikaten in einem 1450 MicrobetaPlus Flüssigkeitsszintillationszähler gezählt. Die Δ4A-Konzentrationen unbekannter Proben werden aus der Standardkurve bestimmt. Die Nachweisgrenze beträgt 0,5 ng/mL und die intra- und inter-Assay-Variationskoeffizienten betragen 10,7 bzw. 17,6 % bei einem Assay-Wert von 13 ng/mL. Die Rate der enzymatischen Reaktion wird als pmol Δ4A, gebildet pro 10 Minuten und pro mg Protein, ausgedrückt. Der Wert der maximalen Aktivität ohne Inhibitor (Kontrolle) wird auf 100 % gesetzt. Die IC50-Werte werden unter Verwendung einer nicht-linearen Analyse aus dem Plot der Enzymaktivität (%) gegen den Logarithmus der Inhibitorkonzentration berechnet.
|
|
| In vivo |
Abiraterone hemmt CYP17 mit einer IC50 von 72 nM in humanen Hodenmikrosomen. Diese Verbindung reduziert die Größe keines der Organe signifikant. Sie reduziert die Testosteronspiegel stark und erreicht fast das Niveau der Orchiektomie-Kontrolle. Die Testosteronspiegel werden durch diese Chemikalie um mehr als 95 % im Vergleich zur Kontrollgruppe reduziert.
|
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | eIF4E / eIF4G / eIF4E / eIF4G / AR p-4EBP1 / 4EBP1 |
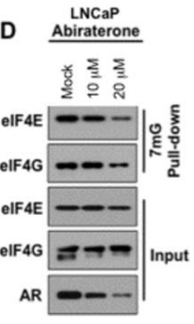
|
22174412 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT06014853 | Completed | Prostate Cancer |
Bukwang Pharmaceutical|Dyna Therapeutics |
August 10 2023 | Phase 1 |
| NCT03348670 | Active not recruiting | Prostate Cancer |
Han Xu M.D. Ph.D. FAPCR Sponsor-Investigator IRB Chair|Medicine Invention Design Inc |
August 18 2023 | Phase 2|Phase 3 |
| NCT05737082 | Completed | Healthy |
Hanmi Pharmaceutical Company Limited |
March 30 2023 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
