nur für Forschungszwecke
Amlodipine Calcium Channel Inhibitor
Kat.-Nr.S1905
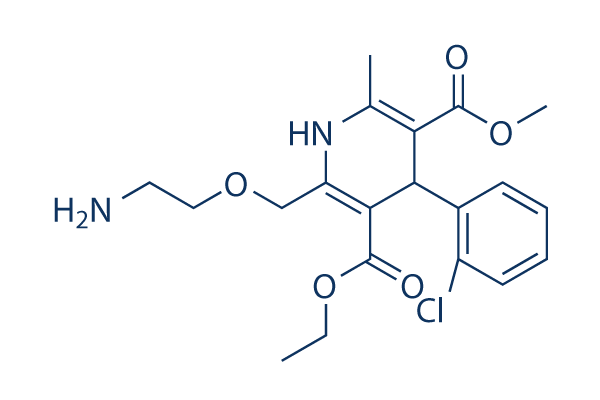
Chemische Struktur
Molekulargewicht: 408.88
Qualitätskontrolle
| Verwandte Ziele | CFTR CRM1 CD markers AChR Sodium Channel Potassium Channel GABA Receptor TRP Channel ATPase GluR |
|---|---|
| Weitere Calcium Channel Inhibitoren | Bay K 8644 Tetrandrine Nilvadipine Flunarizine 2HCl Cilnidipine YM-58483 (BTP2) Ionomycin Imperatorin Manidipine 2HCl Astragaloside A |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 408.88 | Formel | C20H25ClN2O5 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 88150-42-9 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | UK-48340 | Smiles | CCOC(=O)C1=C(NC(=C(C1C2=CC=CC=C2Cl)C(=O)OC)C)COCCN | ||
Löslichkeit
|
In vitro |
DMSO
: 82 mg/mL
(200.54 mM)
Ethanol : 82 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Calcium channel
|
|---|---|
| In vitro |
Amlodipine verursacht eine dosisabhängige Zunahme der Nitritproduktion. Diese Verbindung erhöht auch die Nitritproduktion in großen Koronararterien und in der Aorta. Dies wird auf unterschiedliche physikalisch-chemische Wechselwirkungen der Membran zurückgeführt. Diese Chemikalie trägt zu unterschiedlichen biophysikalischen Wechselwirkungen der Membran bei, die zu potenten lipidantioxidativen Effekten führen, unabhängig von der Modulation der Calcium Channel. Sie erhöht den Gehalt an glatten Muskelzellen in Plaques (P<0,05), während Atenolol die Plaqueentzündung verringert. Diese Verbindung dämpft intrazelluläre neuronale Ca2+-Erhöhungen, die durch KCl-Depolarisation ausgelöst werden, beeinflusst jedoch nicht Ca2+-Veränderungen, die durch die Aktivierung des N-methyl-D-aspartat-Rezeptors ausgelöst werden. Sie hemmt auch dosisabhängig die durch freie Radikale verursachte Schädigung von Lipidbestandteilen der Membran, unabhängig von der Ca2+-Kanalmodulation.
|
| In vivo |
Amlodipine führt bei spontan hypertensiven Ratten zu einer Regression der kardiovaskulären Hypertrophie und einer Verbesserung der endothelialen Dysfunktion. Diese Verbindung reduziert signifikant die Aortenhypertrophie, die endotheliale Dysfunktion, die LOX-1-Expression, die aortale O(2)(-)- und ONOO(-)-Produktion sowie die Plasmawerte von freiem 8-F(2)alpha-Isoprostan bei Ang II-infundierten Ratten. Sie besitzt in vivo antihypertensive und antioxidative Aktivität, die viele der oxidativen Stress-abhängigen Mechanismen, die an Ang II-vermittelten kardiovaskulären Schäden beteiligt sind, wirksam hemmt.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
