nur für Forschungszwecke
Chenodeoxycholic Acid FXR Agonist
Kat.-Nr.S1843
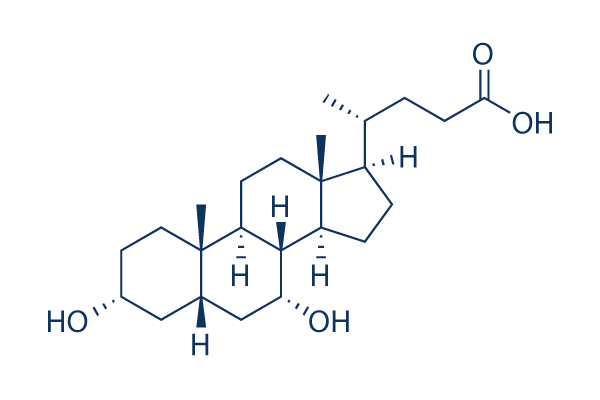
Chemische Struktur
Molekulargewicht: 392.57
Qualitätskontrolle
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 392.57 | Formel | C24H40O4 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 474-25-9 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | Chenodiol, Chenodesoxycholic acid, Chenocholic acid,CDCA | Smiles | CC(CCC(=O)O)C1CCC2C1(CCC3C2C(CC4C3(CCC(C4)O)C)O)C | ||
Löslichkeit
|
In vitro |
DMSO
: 79 mg/mL
(201.23 mM)
Ethanol : 79 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| In vitro |
Chenodeoxycholic acid (CDCA) und Deoxycholic acid (DCA) hemmen beide 11 beta HSD2 mit IC(50)-Werten von 22 mM bzw. 38 mM und verursachen eine Cortisol-abhängige nukleäre Translokation und erhöhen die Transkriptionsaktivität des Mineralocorticoid-Rezeptors (MR). Diese Verbindung kann das Wachstum von Ishikawa-Zellen stimulieren, indem sie eine signifikante Zunahme der Cyclin D1-Protein- und mRNA-Expression durch die Aktivierung des Membran-G-Protein-gekoppelten Rezeptors (TGR5)-abhängigen Signalwegs induziert. Diese Chemikalie induziert LDL-Rezeptor-mRNA-Spiegel ungefähr um das 4-Fache und mRNA-Spiegel für HMG-CoA-Reduktase und HMG-CoA-Synthase um das 2-Fache in einer kultivierten menschlichen Hepatomzelllinie, Hep G2. Der durch diese Verbindung induzierte Isc wird (≥67%) durch Bumetanid, BaCl2 und den CFTR (Cystic Fibrosis Transmembrane Conductance Regulator)-Inhibitor CFTRinh-172 gehemmt. Der durch diese Chemikalie stimulierte Isc wird um 43% durch den Adenylatcyclase-Inhibitor MDL12330A reduziert und erhöht die intrazelluläre cAMP-Konzentration. Die Behandlung mit dieser Verbindung aktiviert C/EBPβ, wie durch die Zunahme seiner Phosphorylierung, nukleären Akkumulation und Expression in HepG2-Zellen gezeigt wird. Es verstärkt die Luziferase-Gen-Transkription aus dem Konstrukt, das den -1.65-kb GSTA2-Promotor enthält, der das C/EBP-Response-Element (pGL-1651) enthält. Diese chemische Behandlung aktiviert die AMP-aktivierte Proteinkinase (AMPK), was zu einer Aktivierung der extrazellulären signalregulierten Kinase 1/2 (ERK1/2) führt, wie die Ergebnisse von Experimenten mit einer dominant-negativen Mutante von AMPKα und einem chemischen Inhibitor zeigen. |
Literatur |
|
|---|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT05130047 | Completed | Chronic Diarrhea|Irritable Bowel Syndrome With Diarrhea|Bile Acid Malabsorption|Bile Acid Diarrhea|Bile Acid Malabsorption Syndrome Type II|Functional Diarrhea |
Michael Camilleri MD|NGM Biopharmaceuticals Inc|Mayo Clinic |
December 1 2021 | Phase 2 |
| NCT03168555 | Completed | Bile Acid Malabsorption|Cholelithiasis |
Zealand University Hospital |
June 22 2017 | Phase 4 |
| NCT01865812 | Completed | Primary Biliary Cirrhosis |
Intercept Pharmaceuticals |
December 3 2013 | Phase 2 |
| NCT01570439 | Unknown status | Anonymous Donors at Blood Donation Center (NUH) |
National University Hospital Singapore |
January 2012 | -- |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
