nur für Forschungszwecke
A-803467 Sodium Channel Inhibitor
Kat.-Nr.S2785
Chemische Struktur
Molekulargewicht: 357.79
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- SDS
- Datenblatt
| Verwandte Ziele | CFTR CRM1 CD markers AChR Calcium Channel Potassium Channel GABA Receptor TRP Channel ATPase GluR |
|---|---|
| Weitere Sodium Channel Inhibitoren | Camostat Mesilate cariporide Tolperisone HCl Vinpocetine Veratramine Bulleyaconi cine A Ambroxol HCl Benzocaine Nefopam HCl Benzocaine hydrochloride |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 357.79 | Formel | C19H16ClNO4 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 944261-79-4 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | COC1=CC(=CC(=C1)NC(=O)C2=CC=C(O2)C3=CC=C(C=C3)Cl)OC | ||
Löslichkeit
|
In vitro |
DMSO
: 72 mg/mL
(201.23 mM)
Ethanol : 11 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
The 1st small-molecule blocker of sodium channels showing both high potency and significant subtype-selectivity among the sodium channel family.
|
|---|---|
| Targets/IC50/Ki |
Na(V1.8) channel
8 nM
|
| In vitro |
A-803467 blockiert potent rekombinante menschliche oder Ratten-NaV1.8-Kanäle mit IC50 von 8 nM bzw. 45 nM bei einem Haltepotential von -40 mV. Im Ruhezustand blockiert diese Verbindung auch potente menschliche NaV1.8-Kanäle mit einer IC50 von 79 nM. Es blockiert Tetrodotoxin-resistente (TTX-R) Ströme in Neuronen des dorsalen Wurzelganglions der Ratte in einer konzentrationsabhängigen Weise mit einer IC50 von 140 nM, potenter im Vergleich zu Mexiletin und Lamotrigin mit einer IC50 von >30 μM. Diese Chemikalie zeigt eine 300- bis 1.000-fach höhere Selektivität für hNaV1.8 gegenüber hNaV1.2, hNaV1.3, hNaV1.5 und hNaV1.7-Kanälen mit einer IC50 von 7,38 μM, 2,45 μM, 7,34 μM bzw. 6,74 μM. Es zeigt keine signifikante Aktivität gegen andere Kanäle und Rezeptoren, die in peripheren sensorischen Neuronen exprimiert werden, einschließlich TRPV1, P2X2/3, CaV2.2 und KCNQ2/3-Kanälen mit einer IC50 von >10 μM. Diese Verbindung zeigt auch keine oder nur eine schwache Aktivität gegen ein breites Screening-Panel von Zelloberflächenrezeptoren, Ionenkanälen und Enzymen mit einer IC50 von >2 μM. Bei 0,3 μM, aber nicht bei 0,1 μM, hemmt es signifikant die Erzeugung spontaner und elektrisch ausgelöster Aktionspotentiale.
|
| In vivo |
Im Einklang mit seinen Wirkungen auf die neuronale Aktionspotential-Elektrogenese in vitro reduziert die systemische Verabreichung von A-803467 (20 mg/kg, i.v.) an Ratten mit spinaler Nervenligatur sowohl spontane als auch von Frey-Haar-evozierte Entladungen von weitreichenden dynamischen Neuronen im Rückenmark-Dorsalhorn signifikant um 66 % bzw. 53 % im Vergleich zu den Ausgangswerten. Die Verabreichung dieser Verbindung reduziert auch dosisabhängig die mechanische Allodynie in einer Vielzahl von Ratten-Schmerzmodellen, einschließlich spinaler Nervenligatur (ED50 = 47 mg/kg, i.p.), Ischiasnervenverletzung (ED50 = 85 mg/kg, i.p.), Capsaicin-induzierter sekundärer mechanischer Allodynie (ED50 ≈ 100 mg/kg, i.p.) und thermischer Hyperalgesie nach intraplantarer vollständiger Freund's-Adjuvans-Injektion (ED50 = 41 mg/kg, i.p.). Diese Chemikalie ist inaktiv gegen Formalin-induzierte Nozizeption und akuten thermischen und postoperativen Schmerz sowie in einem Chemotherapie-induzierten Schmerzmodell (Vincristin).
|
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | HERC2 / USP33 / USP20 |
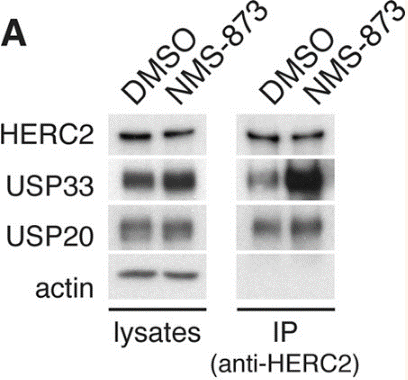
|
24855649 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
