nur für Forschungszwecke
Apremilast PDE Inhibitor
Kat.-Nr.S8034
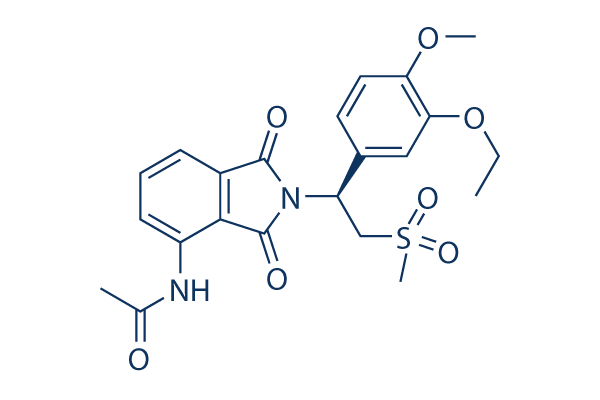
Chemische Struktur
Molekulargewicht: 460.5
Qualitätskontrolle
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 460.5 | Formel | C22H24N2O7S |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 608141-41-9 | -- | Lagerung von Stammlösungen |
|
|
| Synonyme | CC-10004 | Smiles | CCOC1=C(C=CC(=C1)C(CS(=O)(=O)C)N2C(=O)C3=C(C2=O)C(=CC=C3)NC(=O)C)OC | ||
Löslichkeit
|
In vitro |
DMSO
: 92 mg/mL
(199.78 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
PDE4
74 nM
TNF-α
77 nM
|
|---|---|
| In vitro |
Apremilast ist potenter in der Hemmung von PDE4 im Vergleich zu cAMP- oder cGMP-hydrolysierenden Enzymen aus anderen PDE-Familien. Diese Verbindung zeigt ein breites Spektrum an entzündungshemmender Aktivität in einer Vielzahl von Zelltypen, hemmt die Produktion von TNF-α, IL-12 und IL-23 sowie die Reaktionen von NK-Zellen und Keratinozyten. Es wurde festgestellt, dass es die Zymosan-induzierte PMN-Produktion von IL-8 mit einer IC50 von 94 nM hemmt. Diese Chemikalie hemmt die fMLF-induzierte PMN-CD18- und CD11b-Expression mit einer IC50 von 390 nM bzw. 74 nM und hemmt die fMLF-induzierte Adhäsion von PMN an HUVECs mit einer IC50 von 150 nM. Es hemmt die Keratinozyten-TNF-α-Produktion, ohne die Lebensfähigkeit der Keratinozyten, gemessen an den intrazellulären ATP-Spiegeln, zu beeinflussen. .
|
| Kinase-Assay |
PDE4-inhibitorische Aktivität
|
|
Zellen (1 × 109) werden in PBS gewaschen und in kaltem Homogenisationspuffer (20 mM Tris-HCl, pH 7,1, 3 mM 2-Mercaptoethanol, 1 mM MgCl2, 0,1 mM EGTA, 1 μM PMSF, 1 μg/mL Leupeptin) lysiert. Nach der Homogenisation in einem Dounce-Homogenisator wird der Überstand durch Zentrifugation gesammelt und auf eine Sephacryl S-200-Säule geladen, die in Homogenisationspuffer äquilibriert ist. PDE wird in Homogenisationspuffer eluiert, und die Rolipram-empfindlichen Fraktionen werden gepoolt und in Aliquots gelagert. Die Enzymaktivität wird in 50 mM Tris-HCl, pH 7,5, 5 mM MgCl2 und 1 μM cAMP (wovon 1 % 3H cAMP ist) in Gegenwart unterschiedlicher Inhibitorkonzentrationen bestimmt. Die verwendete Extraktmenge wird vorab bestimmt, um sicherzustellen, dass die Reaktionen im linearen Bereich liegen und weniger als 15 % des Gesamtsubstrats verbraucht werden. Die Reaktionen werden bei 30 °C für 30 Minuten durchgeführt und durch 2-minütiges Kochen beendet. Die Proben werden dann gekühlt und mit Schlangengift (1 mg/mL) bei 30 °C für 15 Minuten behandelt. Nicht verwendetes Substrat wird durch Inkubation mit 200 μL AG1-X8-Harz für 15 Minuten entfernt. Die Proben werden dann bei 3000 U/min für 5 Minuten zentrifugiert und 50 μL der wässrigen Phase zur Zählung entnommen. Jeder Datenpunkt wird doppelt durchgeführt, wobei die Aktivität als Prozentsatz der Kontrolle ausgedrückt wird. Die IC50 wird aus Dosis-Wirkungs-Kurven von drei unabhängigen Experimenten bestimmt.
|
|
| In vivo |
Apremilast ist in Gegenwart menschlicher Mikrosomen stabil (t1/2 > 60 min). Es ist zu 90 % proteingebunden im menschlichen Plasma. Die orale und intravenöse Verabreichung dieser Verbindung bei weiblichen Ratten zeigte, dass es eine gute Pharmakokinetik mit geringer Clearance, einem moderaten Verteilungsvolumen und einer oralen Bioverfügbarkeit von 64 % aufweist. In einem LPS-induzierten TNF-α-Inhibitionsmodell bei Ratten wurde die TNF-α-inhibitorische Fähigkeit dieser Verbindung in vivo untersucht, und die ED50 wurde auf 0,03 mg/kg bestimmt. In einem anderen LPS-induzierten Neutrophilie-Modell bei Ratten zeigte diese Verbindung einen ED50-Bereich von 0,3 mg/kg bis 0,9 mg/kg.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT06382987 | Recruiting | Plaque Psoriasis |
Bristol-Myers Squibb |
January 22 2024 | -- |
| NCT06122649 | Recruiting | Plaque Psoriasis |
Amgen |
November 27 2023 | Phase 3 |
| NCT06108544 | Recruiting | Plaque Psoriasis |
Takeda |
November 6 2023 | Phase 3 |
| NCT06088043 | Recruiting | Plaque Psoriasis |
Takeda |
November 6 2023 | Phase 3 |
| NCT05926882 | Completed | Alopecia Areata |
Jinnah Postgraduate Medical Centre |
August 1 2022 | Phase 4 |
| NCT04804553 | Recruiting | Active Juvenile Psoriatic Arthritis |
Amgen |
March 17 2022 | Phase 3 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
