nur für Forschungszwecke
BMS-345541 IKK-1/IKK-2 Inhibitor
Kat.-Nr.S8044
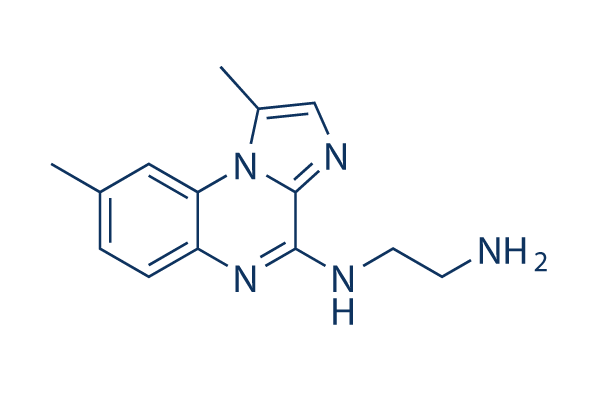
Chemische Struktur
Molekulargewicht: 255.32
Qualitätskontrolle
| Verwandte Ziele | NF-κB HDAC Antioxidant ROS Nrf2 AP-1 MALT NOD |
|---|---|
| Weitere IκB/IKK Inhibitoren | TBK1/IKKε-IN-5 Wedelolactone IKK-16 TPCA-1 Bay 11-7085 IMD 0354 MRT67307 HCl SC-514 WS6 Mesalazine (5-ASA) |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| THP1 cells | Function assay | Inhibition of LPS-induced TNFalpha secretion in THP1 cells, IC50=4 μM | 17197177 | |||
| SF9 cells | Function assay | 20 μM | Inhibition of purified recombinant histidine-HA-tagged IKK-beta expressed in SF9 cells at 20 uM | 18702457 | ||
| H460 | Cytotoxicity assay | 72 hrs | Cytotoxicity against human H460 cells assessed as reduction in cell viability after 72 hrs by MTT assay, IC50 = 2.8 μM. | 29655083 | ||
| LLC | Cytotoxicity assay | 72 hrs | Cytotoxicity against mouse LLC cells measured after 72 hrs by MTT assay, IC50 = 4.8 μM. | 27886548 | ||
| A549 | Cytotoxicity assay | 72 hrs | Cytotoxicity against human A549 cells measured after 72 hrs by MTT assay, IC50 = 5.6 μM. | 27886548 | ||
| NCI-H1975 | Cytotoxicity assay | 72 hrs | Cytotoxicity against human NCI-H1975 cells assessed as reduction in cell viability after 72 hrs by MTT assay, IC50 = 8 μM. | 29655083 | ||
| A549 | Cytotoxicity assay | 72 hrs | Cytotoxicity against human A549 cells assessed as reduction in cell viability after 72 hrs by MTT assay, IC50 = 8.6 μM. | 29655083 | ||
| NCI-H1650 | Cytotoxicity assay | 72 hrs | Cytotoxicity against human NCI-H1650 cells assessed as reduction in cell viability after 72 hrs by MTT assay, IC50 = 9.3 μM. | 29655083 | ||
| Jurkat | Function assay | Inhibition of LPS-induced TNFalpha production in Jurkat cells, EC50 = 13.3 μM. | 17540562 | |||
| HL7702 | Cytotoxicity assay | 72 hrs | Cytotoxicity against human HL7702 cells assessed as reduction in cell viability after 72 hrs by MTT assay, IC50 = 15.3 μM. | 29655083 | ||
| NCI-H1650 | Cytotoxicity assay | 72 hrs | Cytotoxicity against human NCI-H1650 cells measured after 72 hrs by MTT assay, IC50 = 19.9 μM. | 27886548 | ||
| TC32 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for TC32 cells | 29435139 | |||
| A673 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for A673 cells | 29435139 | |||
| DAOY | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for DAOY cells | 29435139 | |||
| Saos-2 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Saos-2 cells | 29435139 | |||
| BT-37 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for BT-37 cells | 29435139 | |||
| RD | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for RD cells | 29435139 | |||
| SK-N-SH | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SK-N-SH cells | 29435139 | |||
| BT-12 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for BT-12 cells | 29435139 | |||
| MG 63 (6-TG R) | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for MG 63 (6-TG R) cells | 29435139 | |||
| NB1643 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for NB1643 cells | 29435139 | |||
| OHS-50 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for OHS-50 cells | 29435139 | |||
| Rh41 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Rh41 cells | 29435139 | |||
| SJ-GBM2 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SJ-GBM2 cells | 29435139 | |||
| SK-N-MC | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SK-N-MC cells | 29435139 | |||
| NB-EBc1 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for NB-EBc1 cells | 29435139 | |||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 255.32 | Formel | C14H17N5 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 445430-58-0 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC1=CC2=C(C=C1)N=C(C3=NC=C(N23)C)NCCN | ||
Löslichkeit
|
In vitro |
Water : 58 mg/mL
DMSO
: 9 mg/mL
(35.24 mM)
Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
Allosteric IKK inhibitor with anti-inflammatory activity.
|
|---|---|
| Targets/IC50/Ki |
IKK2
(Cell-free assay) 0.3 μM
IKK1
(Cell-free assay) 4 μM
|
| In vitro |
BMS-345541 hemmt dosisabhängig die TNF-α-stimulierte Phosphorylierung von IκBα in THP-1-Monozytenzellen mit einer IC50 von ~4 μM. Diese Verbindung hemmt die Lipopolysaccharid-stimulierten Tumornekrosefaktor-α, Interleukin-1β, Interleukin-8 und Interleukin-6 in THP-1-Zellen mit IC50-Werten im Bereich von 1 bis 5 μM. Es bindet in einer wechselseitig ausschließenden Weise in Bezug auf einen Peptidinhibitor, der den Aminosäuren 26 - 42 von IκBα mit Ser-32 und Ser-36, die zu Aspartaten geändert wurden, entspricht, und in einer nicht-wechselseitig ausschließenden Weise in Bezug auf ADP. Diese Chemikalie bindet an ähnliche allosterische Stellen auf IKK-1 und IKK-2, was dann die aktiven Stellen der Untereinheiten unterschiedlich beeinflusst. Es beeinflusst mehrere mitotische Zellzyklusübergänge, einschließlich des mitotischen Eintritts, der Prometaphase zur Anaphase-Progression und der Zytokinese. Das Hinzufügen dieser Verbindung zu den Zellen, die aus dem Arrest in der G-Phase freigesetzt wurden, blockiert die Aktivierung von Aurora A, B und C, die Cdk1-Aktivierung und die Histon-H3-Phosphorylierung. Die Behandlung der mitotischen Zellen mit dieser Chemikalie führt zu einem verfrühten Abbau von Cyclin B1 und Securin, einer defekten Chromosomentrennung und einer unsachgemäßen Zytokinese. Es wurde auch festgestellt, dass es den Spindel-Checkpoint in Nocodazol-arrestierten Zellen überwindet. Diese Effekte sind nicht primär auf eine direkte hemmende Wirkung dieser Verbindung auf mitotische Kinasen wie Cdk1, Aurora A oder B, Plk1 oder NEK2 zurückzuführen. Diese Verbindung (10 μM) hemmt das Wachstum von normalen menschlichen epidermalen Melanozyten und metastatischen Melanomzellen (SK-MEL-5, A375 und Hs 294T) um 96 % bzw. 99 % nach 72 Stunden. Die Anwendung von 100 μM davon auf SK-MEL-5-Zellkulturen führt zu 87 % apoptotischen Zellen nach 24 Stunden auf Kaspsase-unabhängige und AIF-abhängige Mitochondrien-vermittelte Weise. Die Behandlung mit dieser Chemikalie (10 μM) führt zu einer Reduktion der IKK-Aktivitäten und der NF-kB-Aktivität sowie der CXCL1-Produktion um 76 % bzw. 95 %. Es hemmt das Wachstum der T-Zell-akuten lymphoblastischen Leukämie (T-ALL)-Zelllinien BE-13, RPMI-8402 und DND-41, die alle eine Notch1-Mutation aufweisen, und T-ALL-Primärzellen von pädiatrischen Patienten mit einer IC50 von 2-6 μM. 5 μM dieser Verbindung induzieren einen Arrest in der G2/M-Phase des Zellzyklus in BE-13- und DND-41-Zellen und eine Zunahme des Sub-G1-Peaks in RPMI-8402-Zellen. 5 μM davon, 16 Stunden lang behandelt, führen zu einer Zunahme apoptotischer Zellen in all diesen Zellen, begleitet von einer zeitabhängigen Spaltung von Procaspase-8, Procaspase-3 und Poly(ADP-Ribose)-Polymerase (PARP). Diese Chemikalie (5 μM) induziert eine zeitabhängige Dephosphorylierung von IκBα und p65. T-ALL-Zellen, die damit behandelt wurden, zeigen eine nukleäre Translokation von FOXO3a und die Wiederherstellung seiner Funktionen, einschließlich der Kontrolle der p21Cip1-Expressionsspiegel. Es hemmt die TNFα-induzierte Expression von ICAM-1 und VCAM-1 in menschlichen Nabelschnurvenen-Endothelzellen mit einer IC50 von 5 μM. |
| Kinase-Assay |
Enzymassays
|
|
Assays zur Messung der enzymkatalysierten Phosphorylierung von GST-IκBα werden durchgeführt, indem Enzym (eine Endkonzentration von 0,5 μg/mL) bei 30 °C zu Lösungen von 100 μg/mL GST-IκBα und 5 μM [33P]ATP in 40 mM Tris HCl, pH 7,5, mit 4 mM MgCl2, 34 mM Natriumphosphat, 3 mM NaCl, 0,6 mM Kaliumphosphat, 1 mM KCl, 1 mM Dithiothreitol, 3 % (w/v) Glycerin und 250 μg/mL Rinderserumalbumin gegeben wird. Die spezifische Aktivität von [33P]ATP, das im Assay verwendet wird, beträgt 100 Ci/mmol. Nach 5 min werden die Kinase-Reaktionen durch Zugabe von 2× Laemmli-Probenpuffer gestoppt und 1 min bei 90 °C wärmebehandelt. Die Proben werden dann auf NuPAGE 10 % BisTris-Gele geladen. Nach Abschluss der SDS-PAGE werden die Gele auf einem Flachgel-Trockner getrocknet. Die Banden werden dann mit einem 445Si PhosphorImager detektiert und die Radioaktivität mit der ImageQuant-Software quantifiziert. Unter diesen Bedingungen ist der Phosphorylierungsgrad von GST-IκBα linear mit der Zeit und der Enzymkonzentration.
|
|
| In vivo |
BMS-345541 hemmt das Melanom-Tumorwachstum dosisabhängig effektiv. Tumortragende Mäuse, die mit 75 mg/kg dieser Verbindung behandelt wurden, zeigten eine effektive Hemmung des Wachstums von SK-MEL-5-, A375- und Hs 294T-Tumoren um 86 %, 69 % bzw. 67 % im Vergleich zu Kontrolltieren, die nur mit dem Vehikel behandelt wurden. Diese Verbindung, oral in Dosen von 100 mg/kg verabreicht, reduziert die Schwere der Dextransulfat-Natrium-induzierten Kolitis bei Mäusen mit einem Gewichtsverhältnis, einer klinischen Bewertung des Dickdarms, einem mittleren Verletzungsscore und einem mittleren Entzündungsscore von 0,86 (vs. 0,77 der Vehikelgruppe), 1,0 (vs. 2,5 der Vehikelgruppe), 5,66 (vs. 8,52 der Vehikelgruppe) bzw. 6,82 (vs. 12,33 der Vehikelgruppe). Diese Chemikalie (100 mg/kg), oral per Schlundsonde in Wasser einmal täglich ab dem Zeitpunkt der ersten Kollagenimmunisierung verabreicht, hemmt die klinischen Anzeichen der Krankheit im murinen CIA-Modell (0 vs. ~8 der Vehikelgruppe), begleitet von einer reduzierten Pfotenschwellung. Sie reduziert den kumulativen Arthritis-Verletzungsscore von 4,4 auf 0, begleitet von einem geringeren Grad an Tibiotarsalgelenksschäden und einer geringeren Schwere von Entzündungen, Synovialhyperplasie, Knochenresorption und Knorpelerosion. Es wurden keine erkennbaren Verletzungen in den Gelenken der Tiere beobachtet, die histologisch nicht von denen von altersentsprechenden, krankheitsfreien Kontrolltieren zu unterscheiden waren. Diese Verbindung hemmt dosisabhängig die IL-1β-Botschaft, wobei Tiere in der 100 mg/kg-Dosisgruppe Werte zeigten, die mit denen von krankheitsfreien Kontrolltieren vergleichbar waren. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
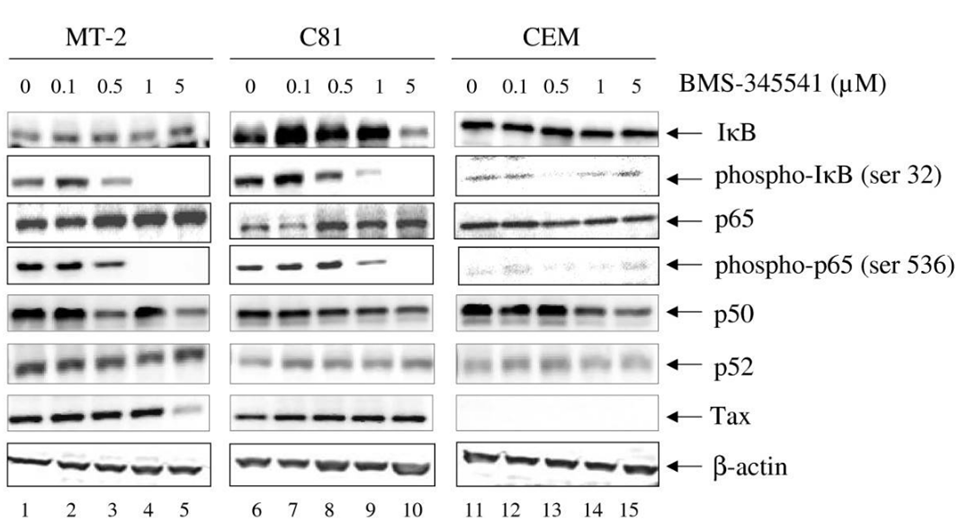
| Western blot | IkB / p-IkB / p65 / p-p65 / p50 / p52 / Tax caspase-3 (p17) / PARP / cleaved PARP |
|
18544167 |
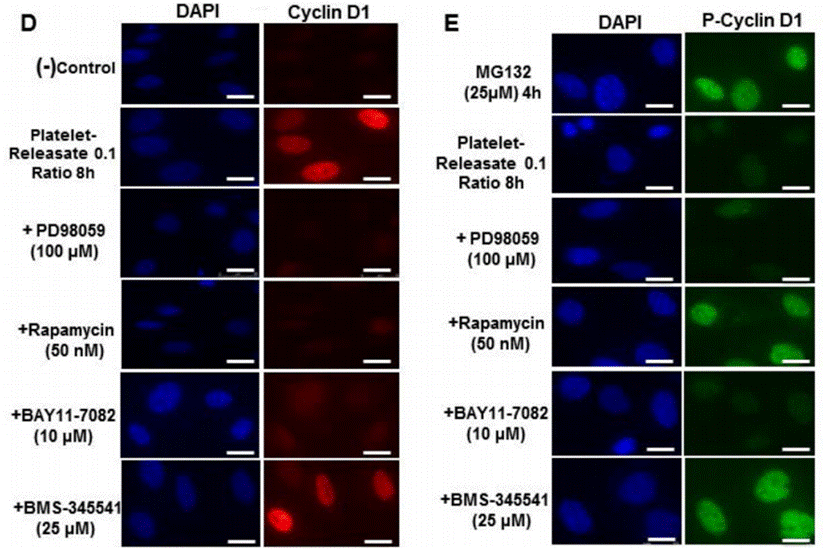
| Immunofluorescence | Cyclin D1 / p-Cyclin D1 NF-κB-p65 |
|
27546592 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
