nur für Forschungszwecke
Setanaxib (GKT137831) NOX1/4 Inhibitor
Kat.-Nr.S7171
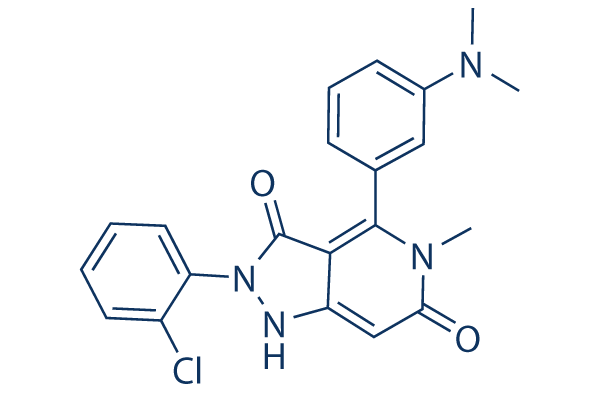
Chemische Struktur
Molekulargewicht: 394.85
Qualitätskontrolle
| Verwandte Ziele | PD-1/PD-L1 CXCR STING AhR Immunology & Inflammation related CD markers Interleukins Anti-infection Antioxidant COX |
|---|---|
| Weitere NADPH-oxidase Inhibitoren | NAD+ (β-DPN) DPI (Diphenyleneiodonium chloride) Apocynin 2-Acetylphenothiazine (ML171) GLX351322 GSK2795039 VAS2870 gp91ds-tat Isuzinaxib (APX-115 free base) |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| HPAECs | Proliferation assay | 0.1-20 μM | 24 h | no significant effect on proliferation | 22904198 | |
| HPASMCs | Proliferation assay | 0.1-20 μM | 24 h | attenuated cell proliferation | 22904198 | |
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 394.85 | Formel | C21H19ClN4O2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1218942-37-0 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | GKT831 | Smiles | CN1C(=O)C=C2C(=C1C3=CC(=CC=C3)N(C)C)C(=O)N(N2)C4=CC=CC=C4Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 78 mg/mL
(197.54 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Ferroptosis
NOX1
(Cell-based assay) 110 nM(Ki)
NOX4
(Cell-based assay) 140 nM(Ki)
|
|---|---|
| In vitro |
Setanaxib (GKT137831) mindert die Hypoxie-induzierte H(2)O(2)-Freisetzung, Zellproliferation und TGF-β1-Expression und dämpft die Reduzierung von PPARγ in HPAECs und HPASMCs. Es verhindert auch oxidativen Stress als Reaktion auf Hyperglykämie in menschlichen Aortenendothelzellen. |
| In vivo |
Bei WT- und SOD1mut-Mäusen blockiert Setanaxib (GKT137831) (60 mg/kg i.g.) die Leberfibrose und reguliert Marker für oxidativen Stress, Entzündungen und Fibrose herunter. Diese Verbindung (60 mg/kg/d p.o.) mindert auch chronische Hypoxie-induzierte rechtsventrikuläre Hypertrophie, vaskuläre Umgestaltung, Lungenzellproliferation und hypoxische Veränderungen der Lungen-PPARγ- und TGF-β1-Expression im Mausmodell der chronischen Hypoxie-Exposition. Bei diabetischen Apolipoprotein-E-defizienten Mäusen mindert es (60 mg/kg/d p.o.) die durch Diabetes mellitus beschleunigte Atherosklerose. Darüber hinaus beseitigt es bei AngII-infundierten c-hNox4Tg-Mäusen die Zunahme des oxidativen Stresses, unterdrückt den Akt-mTOR- und NF-κB-Signalweg und mindert die kardiale Umgestaltung. |
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
