nur für Forschungszwecke
JNJ-1661010 FAAH Inhibitor
Kat.-Nr.S2828
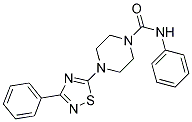
Chemische Struktur
Molekulargewicht: 365.45
Qualitätskontrolle
| Verwandte Ziele | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Weitere FAAH Inhibitoren | URB597 Biochanin A PF-3845 PF-04457845 JNJ-42165279 LY-2183240 FAAH-IN-2 BIA 10-2474 JZL195 URB937 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 365.45 | Formel | C19H19N5OS |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 681136-29-8 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | Takeda-25 | Smiles | C1CN(CCN1C2=NC(=NS2)C3=CC=CC=C3)C(=O)NC4=CC=CC=C4 | ||
Löslichkeit
|
In vitro |
DMSO
: 36 mg/mL
(98.5 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
FAAH (rat)
10 nM
FAAH (human)
12 nM
|
|---|---|
| In vitro |
FAAH, vorinkubiert mit JNJ-1661010, deutet auf eine langsame Reversibilität der Wechselwirkung zwischen dieser Verbindung und dem aktiven Zentrum hin, die bei höheren Temperaturen beschleunigt wird. Diese Verbindung ist ein kovalenter, mechanismusbasierter Substratinhibitor, wie durch LC-ESI-MS untersucht. Es dockt mit dem Phenylthiadiazol im hydrophoben Tunnel und dem Phenylharnstoff in der hydrophilen Tasche von FAAH an.
|
| In vivo |
JNJ-1661010 (20 mg/kg i.p.) hemmt FAAH für bis zu 4 Stunden nach der Verabreichung um mindestens 85 %, was zu einer Akkumulation von Lipidlethanolamiden im Rattenhirn führt. Diese Verbindung kehrt die taktile Allodynie dosisabhängig mit einer maximalen Wirksamkeit von etwa 90 % 30 Minuten nach der Dosis sowohl bei Mäusen mit leichter thermischer Verletzung (MTI) als auch im Rattenmodell um. Es (20 mg/kg) kehrt die taktile Allodynie um 60,8 % nach 30 Minuten im Rattenmodell der Spinalnervenligationsverletzung um. Diese Chemikalie (50 mg/kg i.p.) zeigt eine signifikante Abschwächung der Hyperalgesie 30 Minuten nach der Dosis im Ratten-Carrageenan-Modell des entzündlichen Schmerzes. Ratten, die mit dieser Verbindung (20 mg/kg i.p.) behandelt wurden, haben eine Plasma-Cmax von 26,9 μM bei einer Tmax von 0,75 h und eine Cmax im Gehirn von 6,04 μM bei einer Tmax von 2 h. Es (20 mg/kg i.p.) hemmt die Gehirn-FAAH und erhöht den AEA-Spiegel im Gehirngewebe von Ratten.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
