nur für Forschungszwecke
Lomerizine 2HCl Calcium Channel Inhibitor
Kat.-Nr.S4084
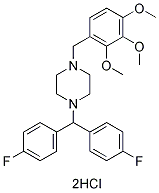
Chemische Struktur
Molekulargewicht: 541.46
Qualitätskontrolle
| Verwandte Ziele | CFTR CRM1 CD markers AChR Sodium Channel Potassium Channel GABA Receptor TRP Channel ATPase GluR |
|---|---|
| Weitere Calcium Channel Inhibitoren | Bay K 8644 Tetrandrine Nilvadipine Flunarizine 2HCl Cilnidipine YM-58483 (BTP2) Ionomycin Imperatorin Manidipine 2HCl Astragaloside A |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 541.46 | Formel | C27H30F2N2O3.2HCl |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 101477-54-7 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | KB-2796 | Smiles | COC1=C(C(=C(C=C1)CN2CCN(CC2)C(C3=CC=C(C=C3)F)C4=CC=C(C=C4)F)OC)OC.Cl.Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 8 mg/mL
(14.77 mM)
Ethanol : 3 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
L-type calcium channel
T-type calcium channel
|
|---|---|
| In vitro |
Lomerizine (0,1 μM und 1 μM) reduziert signifikant die Glutamat-induzierte Neurotoxizität in kultivierten Netzhautneuronen von Ratten. Lomerizine (1 μM) zeigt auch schützende Wirkungen gegen N-methyl-D-aspartat- und Kainat-induzierte Neurotoxizität in kultivierten Netzhautneuronen von Ratten.
|
| In vivo |
Lomerizine (0,1 mg/kg und 1 mg/kg, i.v.) vor der Ischämie und unmittelbar nach der Reperfusion reduziert dosisabhängig die Netzhautschädigung in der Rattenretina. Lomerizine (30 mg/kg, oral) reduziert die sekundäre Nekrose nach 2 Wochen und die sekundäre Caspase-3-Expression nach 3 Wochen bei erwachsenen Piebald-Virol-Glaxo (PVG) Ratten. Lomerizine (30 mg/kg, oral) reduziert morphologische Störungen, oxidativen Stress und die Phosphacan-Expression und begrenzt frühe Anstiege der Makrophagenzahlen bei weiblichen PVG Hooded Ratten. Lomerizine (30 mg/kg, oral) schützt RGCs vor sekundärem Tod nach 4 Wochen, stellt jedoch die Verhaltensfunktion (optokinetischer Nystagmus) bei weiblichen PVG Hooded Ratten nicht vollständig wieder her. Lomerizine (0,1 mg/kg oder 0,3 mg/kg) erhöht signifikant die Durchblutung in der Kaninchenretina und im Sehnervenkopf (ONH), aber die Durchblutung änderte sich wenig in der Aderhaut oder im Iris-Ziliarkörper. Lomerizine (0,1 und 0,3 mg/kg, i.v.) erhöht signifikant die Gewebedurchblutung im Sehnervenkopf und die putative Durchblutung in der langen hinteren Ziliararterie mit einer geringeren Blutdrucksenkung (0,3 mg/kg, i.v.) und ohne Änderung der Herzfrequenz beim Kaninchen. Lomerizine (0,1 und 0,3 mg/kg, i.v.) hemmt die Hypoperfusion im Sehnervenkopf des Kaninchens.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
