nur für Forschungszwecke
Metformin Hydrochloride Antihyperglykämisches Mittel
Kat.-Nr.S1950
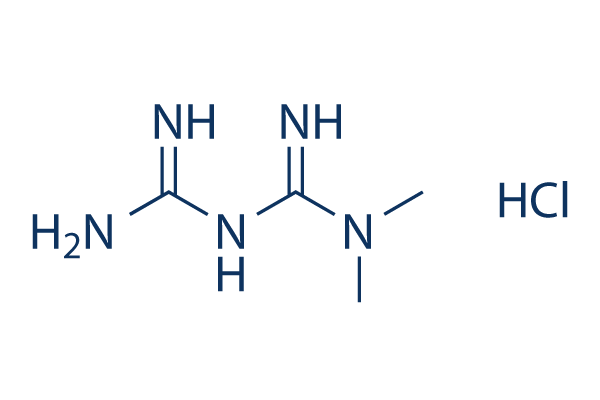
Chemische Struktur
Molekulargewicht: 165.62
Qualitätskontrolle
Produkte, die oft zusammen verwendet werden mit Metformin Hydrochloride
| Verwandte Ziele | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Mitochondrial Metabolism Drug Metabolite |
|---|---|
| Weitere Carbohydrate Metabolism Inhibitoren | 2-DG (2-Deoxy-D-glucose) Bromopyruvic acid (3-BP) Lonidamine Dorzagliatin LY2608204 Voglibose 1-Deoxynojirimycin 4',7-Dimethoxy-5-Hydroxyflavone AZD1656 Nodakenetin |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| human HepG2 cells | Function assay | 1 mM | 24 h | Activation of AMPK in human HepG2 cells assessed as reduction of gluconeogenesis at 1 mM after 24 hrs by enzymatic colorimetric assay | 26471090 | |
| mouse 3T3L1 cells | Function assay | 1 mM | Induction of AMPK phosphorylation in mouse 3T3L1 cells at 1 mM by Western blot analysis | 25216379 | ||
| human HepG2 cells | Function assay | 1 mM | 24 h | Reduction of glucose consumption in insulin-resistant human HepG2 cells at 1 mM after 24 hrs by glucose oxidase method in presence of 22.2 mM of glucose | 23025244 | |
| human MDA-MB-231 cells | Function assay | 1 to 20 mM | 24 h | Antiproliferative activity against human MDA-MB-231 cells at 1 to 20 mM after 24 hrs by MTT assay. | 22459208 | |
| human HepG2 cells | Function assay | 24 h | Increase in glucose consumption in insulin-resistant human HepG2 cells after 24 hrs, EC50=0.27 μM. | 21856048 | ||
| Hs575T | Function assay | 20 mM | 24 hrs | Inhibition of mTOR phosphorylation in triple-negative human Hs575T cells at 20 mM after 24 hrs by immunoblot analysis | 23490148 | |
| Hs578T | Antiinvasive assay | 20 mM | 17 hrs | Antiinvasive activity against triple-negative human Hs578T cells at 20 mM after 17 hrs by light microscopic analysis | 23490148 | |
| Hs575T | Function assay | 20 mM | 24 hrs | Activation of AMPK in triple-negative human Hs575T cells at 20 mM after 24 hrs by immunoblot analysis | 23490148 | |
| L6 | Function assay | 2 mM | 4 hrs | Increase in glucose uptake in rat L6 cells at 2 mM treated for 4 hrs post 30 mins AMPK inhibitor compound C treatment | 29128163 | |
| HepG2 | Function assay | 1 mM | 24 hrs | Induction of glucose consumption in human HepG2 cells at 1 mM incubated for 24 hrs | 28651984 | |
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 165.62 | Formel | C4H11N5.HCl |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1115-70-4 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | 1,1-Dimethylbiguanide HCl | Smiles | CN(C)C(=N)N=C(N)N.Cl | ||
Löslichkeit
|
In vitro |
Water : 33 mg/mL Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
AMPK
(Hepatocytes) |
|---|---|
| In vitro |
Metformin (500 μM) aktiviert AMPK in Hepatozyten, wodurch die Aktivität der Acetyl-CoA-Carboxylase (ACC) reduziert, die Fettsäureoxidation induziert und die Expression lipogener Enzyme unterdrückt wird. Metformin (2 mM) aktiviert den Muskel-AMPK und fördert die Glukoseaufnahme. Metformin (500 μM) oder AICAR unterdrücken die SREBP-1-mRNA-Expression in Rattenhepatozyten stark. Metformin verbessert die Hyperglykämie, ohne die Insulinsekretion zu stimulieren, eine Gewichtszunahme zu fördern oder eine Hypoglykämie zu verursachen. Metformin hat positive Auswirkungen auf zirkulierende Lipide, die mit einem erhöhten kardiovaskulären Risiko verbunden sind. Metformin senkt die hepatische Glukoseproduktion und erhöht die Glukoseaufnahme in Skelettmyozyten. Metformin benötigt LKB1 in der Leber, um den Blutzuckerspiegel zu senken. Metformin (2 mM) führt zu einem signifikanten Anstieg der Aktivität sowohl der α1- als auch der α2-haltigen Komplexe in Muskelzellen. Metformin (2 mM) erhöht auch die Threonin-172-Phosphorylierung in Muskelzellen. |
| In vivo |
Die Behandlung mit Metformin (100 mg/ml, p.o.) führt zu einer signifikanten Abnahme der hepatischen Expression von mRNAs für SREBP-1, FAS und S14 bei SD-Ratten, was mit den in Zellen dokumentierten Effekten übereinstimmt. Metformin senkt auch die hepatischen Lipide bei übergewichtigen Mäusen. Metformin (250 mg/kg, i.p.) erhöht die AMPK-Phosphorylierung in der Leber von Wildtyp-Mäusen. Die Behandlung mit Metformin (250 mg/kg, i.p.) reduziert den Blutzucker bei Wildtyp-Mäusen unter einer fettreichen Diät um mehr als 50%. Die Behandlung mit Metformin (250 mg/kg, i.p.) senkt auch den Blutzucker bei ob/ob-Mäusen um 40%. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | p-AMPK / AMPK / p-mTOR / mTOR / p-S6K / S6K TTP / p-STAT3 / STAT3 / c-Myc pACC / ACC / pS6 / S6 pSTAT3 (Ser727) / STAT3 / Jak2 / Cdk5 / pNFκB / Bcl-2 / Bcl-XL / c-Myc |
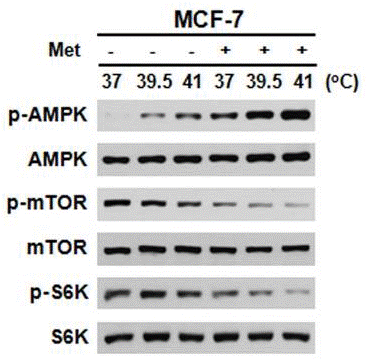
|
24505341 |
| Immunofluorescence | LKB1 PAR CD86 / CD206 beta-catenin / AMPK |
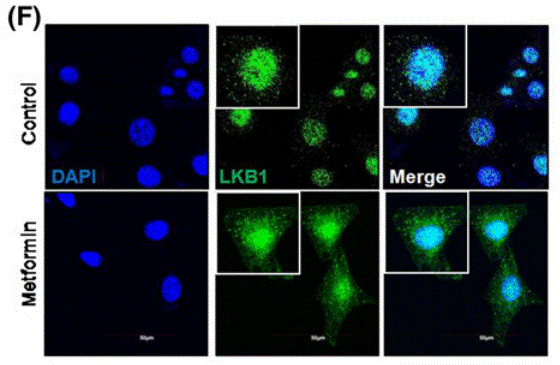
|
29601127 |
| Growth inhibition assay | Cell viability |
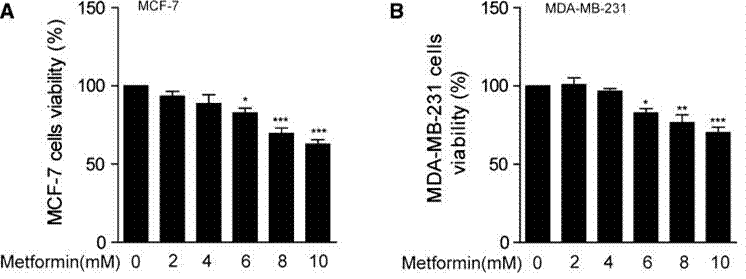
|
26956973 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT05910554 | Not yet recruiting | Sarcoidosis Pulmonary |
University of Maryland Baltimore |
May 1 2024 | Phase 2 |
| NCT06120881 | Recruiting | Type 2 Diabetes |
University of California San Francisco|National Institute of Diabetes and Digestive and Kidney Diseases (NIDDK) |
April 1 2024 | Early Phase 1 |
| NCT06147050 | Not yet recruiting | Long COVID |
Purpose Life Sciences |
April 2024 | Phase 3 |
| NCT06296836 | Not yet recruiting | Diabetes Mellitus Type 2 |
University of Illinois at Chicago|Emily Hanners|Dulal Bhaumik|Avisek Datta|Peggy Choye|Hailey Soni|Annesti Elmasri|Julie Jun|Colin Goodman |
April 1 2024 | Phase 4 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
