nur für Forschungszwecke
Niraparib (MK-4827) PARP Inhibitor
Kat.-Nr.S2741
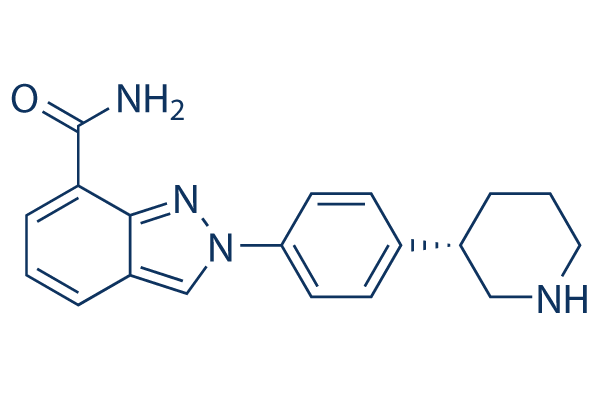
Chemische Struktur
Molekulargewicht: 320.39
Qualitätskontrolle
| Verwandte Ziele | HDAC ATM/ATR DNA-PK WRN DNA/RNA Synthesis Topoisomerase PPAR Sirtuin Casein Kinase eIF |
|---|---|
| Weitere PARP Inhibitoren | XAV-939 AZD5305 (Saruparib) Veliparib (ABT-888) PJ34 HCl AG-14361 Iniparib (BSI-201) G007-LK Pamiparib UPF 1069 A-966492 |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| HeLa cells | Function assay | Inhibition of PARP in hydrogen peroxide-induced human HeLa cells assessed as inhibition DNA-damage-induced PARylation, EC50=0.004 μM | 19873981 | |||
| A549 cells | Cytotoxicity assay | 5-7 days | Cytotoxicity against human A549 cells transfected with BRCA2 shRNA assessed as inhibition of cell proliferation after 5 to 7 days by CellTiter-Blue assay, CC50=0.011 μM | 25761096 | ||
| MDA-MB-436 cells | Proliferation assay | 6 days | Antiproliferative activity against human MDA-MB-436 cells expressing BRCA1 5396 + 1G>A mutant after 6 days by cell titer-blue assay, CC50=18 nM | 19873981 | ||
| SUM1315MO2 cells | Cytotoxicity assay | 12 days | Cytotoxicity against human SUM1315MO2 cells carrying BRCA1 mutant assessed as inhibition of cell proliferation after 12 days by CellTiter-Blue assay, CC50=0.02 μM | 25761096 | ||
| DoTc2-4510 cells | Cytotoxicity assay | 5-7 days | Cytotoxicity against human DoTc2-4510 cells carrying BRCA2 mutant assessed as inhibition of cell proliferation after 5 to 7 days by CellTiter-Blue assay, CC50=0.023 μM | 25761096 | ||
| SUM149PT cells | Cytotoxicity assay | 5-7 days | Cytotoxicity against human SUM149PT cells carrying BRCA1 mutant assessed as inhibition of cell proliferation after 5 to 7 days by CellTiter-Blue assay, CC50=0.024 μM | 25761096 | ||
| UWB1.289 cells | Cytotoxicity assay | 5-7 days | Cytotoxicity against human UWB1.289 cells carrying BRCA1 mutant assessed as inhibition of cell proliferation after 5 to 7 days by CellTiter-Blue assay, CC50=0.056 μM | 25761096 | ||
| Capan1 cells | Cytotoxicity assay | Cytotoxicity against BRCA2-deficient human Capan1 cells, CC50=0.09 μM | 25761096 | |||
| Jurkat cells | Function assay | Inhibition of PARP1 in human Jurkat cells assessed as reduction of cell viability after 96 hrs by MTS assay in presence of 100 uM of temozolomide, EC50=0.2 μM | 23850199 | |||
| BT20 cells | Cytotoxicity assay | 5-7 days | Cytotoxicity against human BT20 cells assessed as inhibition of cell proliferation after 5 to 7 days by CellTiter-Blue assay, CC50=2.2 μM | 25761096 | ||
| Antiproliferative assay | HeLa | 7 days | Antiproliferative activity against BRCA1 deficient human HeLa cells after 7 days by cell titer-blue assay, CC50 = 0.033 μM. | 19873981 | ||
| Function assay | HeLa | Inhibition of PARP in hydrogen peroxide-induced human HeLa cells assessed as inhibition DNA-damage-induced PARylation, EC90 = 0.045 μM. | 19873981 | |||
| Antiproliferative assay | Capan1 | 13 days | Antiproliferative activity against human Capan1 cells expressing BRCA2 6174delT mutation and loss of wild-type allele after 13 days by cell titer-blue assay, CC50 = 0.09 μM. | 19873981 | ||
| Antiproliferative assay | HeLa | 7 days | Antiproliferative activity against human HeLa cells expressing wild type BRCA1 after 7 days by cell titer-blue assay, CC50 = 0.86 μM. | 19873981 | ||
| Function assay | Jurkat | 96 hrs | Inhibition of PARP1 in human Jurkat cells assessed as reduction of cell viability after 96 hrs by MTS assay, EC50 = 31 μM. | 23850199 | ||
| Function assay | CAPAN-1 | Inhibition of PARP in BRCA2-deficient human CAPAN-1 cells assessed as inhibition of hydrogen peroxide-induced PARylation by cell-based assay, IC50 = 0.0035 μM. | 25761096 | |||
| Function assay | HeLa | Inhibition of PARP in human HeLa cells assessed as inhibition of hydrogen peroxide-induced PARylation by cell-based assay, EC50 = 0.004 μM. | 25761096 | |||
| Function assay | A2780 | Inhibition of PARP in human A2780 cells assessed as inhibition of hydrogen peroxide-induced PARylation by cell-based assay, IC50 = 0.004 μM. | 25761096 | |||
| Cytotoxicity assay | MDA-MB-436 | Cytotoxicity against human MDA-MB-436 cells carrying BRCA1 mutant assessed as inhibition of cell proliferation, CC50 = 0.018 μM. | 25761096 | |||
| Cytotoxicity assay | HeLa | 5 to 7 days | Cytotoxicity against human HeLa cells transfected with BRCA1 shRNA assessed as reduction of cell viability after 5 to 7 days by CellTiter-Blue assay, CC50 = 0.034 μM. | 25761096 | ||
| Function assay | HeLa | Inhibition of PARP in human HeLa cells assessed as inhibition of hydrogen peroxide-induced PARylation by cell-based assay, IC90 = 0.046 μM. | 25761096 | |||
| Function assay | CAPAN-1 | Inhibition of PARP in BRCA2-deficient human CAPAN-1 cells assessed as inhibition of hydrogen peroxide-induced PARylation by cell-based assay, IC90 = 0.05 μM. | 25761096 | |||
| Function assay | A2780 | Inhibition of PARP in human A2780 cells assessed as inhibition of hydrogen peroxide-induced PARylation by cell-based assay, IC90 = 0.052 μM. | 25761096 | |||
| Cytotoxicity assay | HeLa | 5 to 7 days | Cytotoxicity against wild type human HeLa cells assessed as inhibition of cell proliferation after 5 to 7 days by CellTiter-Blue assay, CC50 = 0.852 μM. | 25761096 | ||
| Cytotoxicity assay | UWB1.289 | 5 to 7 days | Cytotoxicity against human UWB1.289 cells expressing BRCA1 assessed as inhibition of cell proliferation after 5 to 7 days by CellTiter-Blue assay, CC50 = 0.975 μM. | 25761096 | ||
| Cytotoxicity assay | A549 | 5 to 7 days | Cytotoxicity against wild type human A549 cells assessed as inhibition of cell proliferation after 5 to 7 days by CellTiter-Blue assay, CC50 = 1.76 μM. | 25761096 | ||
| Cytotoxicity assay | Capan1 | Cytotoxicity against BRCA2-deficient human Capan1 cells, EC50 = 0.65 μM. | 26652717 | |||
| Antitumor assay | MDA-MB-436 | 50 mg/kg | 33 days | Antitumor activity against human MDA-MB-436 cells expressing BRCA1 5396 + 1G>A mutant xenografted in CD1 mouse assessed as tumor regression at 50 mg/kg, po bid for 33 days | 19873981 | |
| Antitumor assay | MDA-MB-436 | 100 mg/kg | 33 days | Antitumor activity against human MDA-MB-436 cells expressing BRCA1 5396 + 1G>A mutant xenografted in CD1 mouse assessed as tumor regression at 100 mg/kg, po qd for 33 days | 19873981 | |
| Antitumor assay | MDA-MB-436 | 80 mg/kg | 1 to 2 weeks | Antitumor activity against human MDA-MB-436 cells harboring BRCA1 mutant xenografted in immunocompromised mouse assessed as tumor growth inhibition at 80 mg/kg, po qd for 1 to 2 weeks | 25761096 | |
| Antitumor assay | MDA-MB-436 | 80 mg/kg | 4 weeks | Antitumor activity against human MDA-MB-436 cells harboring BRCA1 mutant xenografted in immunocompromised mouse assessed as complete and sustained tumor regression at 80 mg/kg, po qd for 4 weeks | 25761096 | |
| Antitumor assay | MDA-MB-436 | 50 mg/kg | Antitumor activity against human MDA-MB-436 cells harboring BRCA1 mutant xenografted in immunocompromised mouse assessed as tumor growth inhibition at 50 mg/kg, po administered daily | 25761096 | ||
| Antitumor assay | MDA-MB-436 | 80 mg/kg | 3 weeks | Antitumor activity against human MDA-MB-436 cells harboring BRCA1 mutant xenografted in immunocompromised mouse assessed as tumor shrinkage at 80 mg/kg, po qd for 3 weeks | 25761096 | |
| qHTS assay | TC32 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for TC32 cells | 29435139 | |||
| qHTS assay | A673 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for A673 cells | 29435139 | |||
| qHTS assay | NB1643 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for NB1643 cells | 29435139 | |||
| qHTS assay | A673 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for A673 cells) | 29435139 | |||
| qHTS assay | BT-37 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for BT-37 cells | 29435139 | |||
| qHTS assay | SK-N-MC | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SK-N-MC cells | 29435139 | |||
| qHTS assay | NB-EBc1 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for NB-EBc1 cells | 29435139 | |||
| qHTS assay | LAN-5 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for LAN-5 cells | 29435139 | |||
| qHTS assay | SK-N-MC | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for SK-N-MC cells | 29435139 | |||
| qHTS assay | TC32 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for TC32 cells | 29435139 | |||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 320.39 | Formel | C19H20N4O |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1038915-60-4 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
Löslichkeit
|
In vitro |
DMSO
: 64 mg/mL
(199.75 mM)
Ethanol : 64 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
PARP2
(Cell-free assay) 2.1 nM
PARP1
(Cell-free assay) 3.8 nM
|
|---|---|
| In vitro |
In einem Ganzzell-Assay hemmte Niraparib (MK-4827) die PARP-Aktivität mit einer EC50 = 4 nM und hemmte die Proliferation von Krebszellen mit mutiertem BRCA-1 und BRCA-2 mit einer CC50 im Bereich von 10-100 nM. Es zeigte sich, dass es ein potenter und selektiver PARP-1- und PARP-2-Inhibitor mit IC50 = 3,8 bzw. 2,1 nM war. Darüber hinaus zeigte diese Verbindung eine mindestens 100-fache Selektivität gegenüber PARP-3, V-PARP und Tankyrase-1 mit IC50 = 1300, 330 bzw. 570 nM. Neben der Hemmung des Wachstums von HeLa-Zellen, denen BRCA-1 aufgrund der Silencing durch RNA-Interferenz fehlt, ist es in der Lage, die Proliferation von Krebszelllinien zu hemmen, die natürliche BRCA-1- oder BRCA-2-Mutationen tragen. In MDA-MB-436-Zellen des menschlichen Mammakarzinoms, die BRCA-1-Mutationen tragen, zeigte es eine CC50 = 18 nM, während es in CAPAN-1-Zellen des menschlichen Pankreaskarzinoms, die BRCA-2-mutiert sind, eine CC50 = 90 nM zeigte. Im Gegensatz dazu sind normale menschliche Prostata- und Brustepithelzellen resistent gegen MK-4827, zeigen antiproliferative Effekte im mikromolaren Bereich, wodurch die sehr hohe selektive Zytotoxizität dieser PARP-Inhibitoren in BRCA-1- und -2-mutierten Krebszellen im Vergleich zum umgebenden Gewebe demonstriert wird.
|
| In vivo |
Niraparib (MK-4827), ein neuartiger, oral bioverfügbarer PARP-1- und PARP-2-Inhibitor, verstärkte die Wirkung von Strahlung auf eine Vielzahl menschlicher Tumorzell-Xenografts, sowohl p53-Wildtyp als auch p53-Mutanten, stark. Es war in vivo gut verträglich und zeigte Wirksamkeit als Einzelwirkstoff in einem Xenograft-Modell von BRCA-1-defizientem Krebs.
|
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | c-PARP /c-caspase 3 / γ-H2AX |
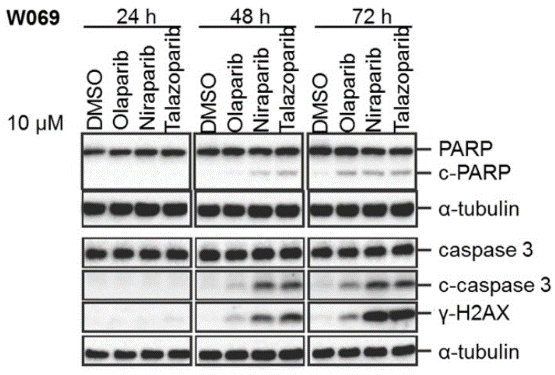
|
29158830 |
| Immunofluorescence | Rad51 / Geminin |
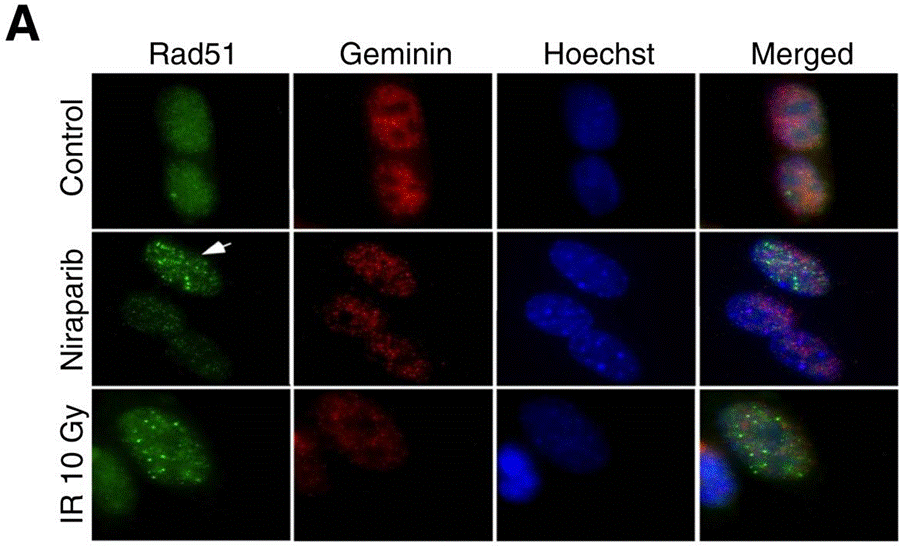
|
27614696 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT05289648 | Not yet recruiting | Endometrial Cancer|Serous Adenocarcinoma|Uterine Neoplasm |
Sir Mortimer B. Davis - Jewish General Hospital |
May 1 2024 | Early Phase 1 |
| NCT06077877 | Recruiting | Neoplasms |
GlaxoSmithKline |
October 24 2023 | Phase 1|Phase 2 |
| NCT05666349 | Withdrawn | Recurrent Glioblastoma |
University College London|GlaxoSmithKline |
October 13 2023 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
Häufig gestellte Fragen
Frage 1:
How to reconstitute it for in vivo studies?
Antwort:
It can be orally administered using the formulation 1% CMC-Na (suspension).
