nur für Forschungszwecke
XL388 mTOR Inhibitor
Kat.-Nr.S7035
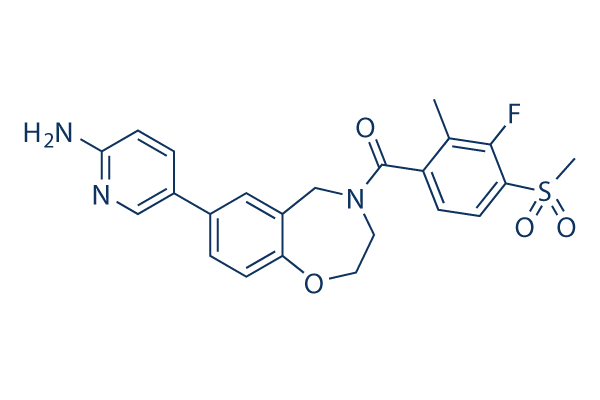
Chemische Struktur
Molekulargewicht: 455.5
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- HPLC
- SDS
- Datenblatt
| Verwandte Ziele | PI3K Akt GSK-3 ATM/ATR DNA-PK AMPK PDPK1 PTEN PP2A PDK |
|---|---|
| Weitere mTOR Inhibitoren | Torin 1 Torin 2 AZD8055 Ridaforolimus (Deforolimus, MK-8669) Sapanisertib (MLN0128, INK-128) Torkinib (PP242) MHY1485 Vistusertib (AZD2014) KU-0063794 OSI-027 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 455.5 | Formel | C23H22FN3O4S |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1251156-08-7 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC1=C(C=CC(=C1F)S(=O)(=O)C)C(=O)N2CCOC3=C(C2)C=C(C=C3)C4=CN=C(C=C4)N | ||
Löslichkeit
|
In vitro |
DMSO
: 1.25 mg/mL
(2.74 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
mTORC1
8 nM
mTOR
9.9 nM
mTORC2
166 nM
|
|---|---|
| In vitro |
In MCF-7-Zellen blockiert XL388 die mTORC1-Phosphorylierung von p70S6K (T389) mit einem IC50-Wert von 94 nM und die mTORC2-Phosphorylierung von AKT (S473) mit einem IC50-Wert von 350 nM. In vitro hemmt diese Verbindung die Viabilität solider und hämatopoetischer Tumorzelllinien. Die Proliferations-IC50 beträgt 1,37 μM in der MCF-7-Zelllinie. Es wirkt auch synergistisch mit Chemotherapeutika in zellbasierten Assays, um die Zellviabilität zu blockieren.
|
| In vivo |
Bei einmal täglicher oraler Verabreichung an Mäuse zeigt XL388 eine robuste Antitumoraktivität in mehreren Xenograft-Modellen, einschließlich einer > 100%igen Tumorzellwachstumshemmung im MCF-7-Xenograft-Modell. Diese Verbindung weist gute pharmakokinetische Eigenschaften und eine gute orale Exposition in mehreren Spezies mit moderater Bioverfügbarkeit auf. Die mittlere Plasmaproteinbindung dieser Chemikalie in menschlichem, Affen-, Hunde-, Ratten- und Mäuseplasma wird bei 5 μM evaluiert und beträgt 86 %, 90 %, 89 %, 85 % bzw. 84 %. Die orale Verabreichung dieses Wirkstoffs an athymische Nacktmäuse, denen menschliche Tumorxenografts implantiert wurden, führte zu einer signifikanten und dosisabhängigen Antitumoraktivität. Eine starke Hemmung sowohl von mTORC1 als auch von mTORC2 wird 4–8 h nach oraler Verabreichung von 100 mg/kg erreicht. Eine moderate Hemmung (39–45 %) der Phosphorylierung des PI3K-Ziels AKT (T308) wird ebenfalls 4–8 h nach der Dosis beobachtet.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
