nur für Forschungszwecke
6-Gingerol Apoptosis related chemisch
Kat.-Nr.S3836
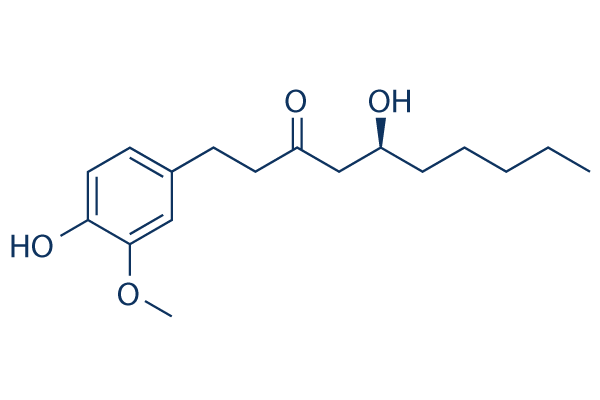
Chemische Struktur
Molekulargewicht: 294.39
Qualitätskontrolle
| Verwandte Ziele | Bcl-2 Caspase PD-1/PD-L1 Ferroptosis p53 Synthetic Lethality STAT TNF-alpha Ras KRas |
|---|---|
| Weitere Apoptosis related Inhibitoren | Importazole Pitstop 2 Genipin Plumbagin Crocin Bisdemethoxycurcumin (BDMC) Sophoridine Flavone Protocatechuic acid Euphorbia factor L3 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 294.39 | Formel | C17H26O4 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 23513-14-6 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CCCCCC(CC(=O)CCC1=CC(=C(C=C1)O)OC)O | ||
Löslichkeit
|
In vitro |
DMSO
: 58 mg/mL
(197.01 mM)
|
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| In vitro |
Die 6-Gingerol-Behandlung reduziert die Zellviabilität menschlicher Darmkrebszellen, LoVo, dosisabhängig signifikant. 6-Gingerol induziert einen signifikanten G2/M-Phasen-Arrest und hat einen leichten Einfluss auf die Sub-G1-Phase in LoVo-Zellen. Die Spiegel von Cyclin A, Cyclin B1 und CDK1 sind vermindert; im Gegensatz dazu sind die Spiegel der negativen Zellzyklusregulatoren p27Kip1 und p21Cip1 als Reaktion auf die 6-Gingerol-Behandlung erhöht. Darüber hinaus erhöht die 6-Gingerol-Behandlung intrazelluläre reaktive Sauerstoffspezies (ROS) und den Phosphorylierungsgrad von p53. 6-Gingerol ist wirksam bei der Unterdrückung der Transformation, Hyperproliferation und entzündlichen Prozesse, die die Karzinogenese initiieren und fördern, sowie der späteren Schritte der Karzinogenese, nämlich Angiogenese und Metastasierung. 6-Gingerol hat direkte zytotoxische Wirkungen auf Kulturen von Tumorzellen, wie z.B. Darmkrebszellen, HL-60-Zellen und Brustkrebszellen.
|
|---|---|
| In vivo |
6-Gingerol hemmt das Tumorwachstum bei verschiedenen Arten von murinen Tumoren, wie B16F1-Melanomen, Renca-Nierenzellkarzinomen und CT26-Kolonkarzinomen, die durch Inokulation von Tumorzellen an den Flanken von Mäusen etabliert wurden, obwohl es nicht zu einer vollständigen Ausrottung der Tumoren führt. Die 6-Gingerol-Behandlung von tumortragenden Mäusen verursacht eine massive Infiltration von CD4- und CD8-T-Zellen sowie B220+-B-Zellen, reduziert jedoch die Anzahl der CD4+Foxp3+-regulatorischen T-Zellen. Die CD8-Tumor-infiltrierenden T-Lymphozyten in 6-Gingerol-behandelten Mäusen exprimieren stark IFN-γ, einen Marker für die Aktivierung von CTL-CD107a-Zellen, und Chemokinrezeptoren, die auf TH1-Zellen exprimiert werden, wie CXCR3 und CCR5.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
