nur für Forschungszwecke
JNJ-7706621 Aurora Kinase/CDK Inhibitor
Kat.-Nr.S1249
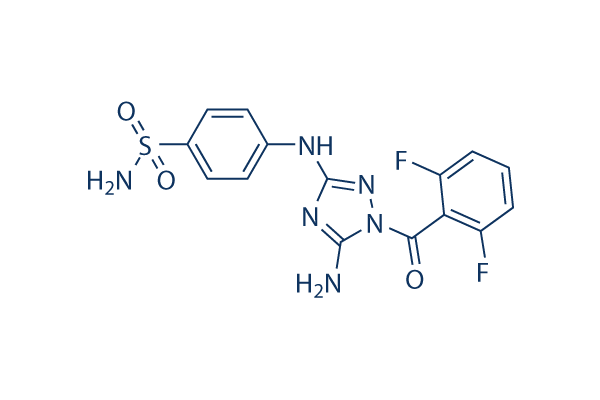
Chemische Struktur
Molekulargewicht: 394.36
Qualitätskontrolle
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| PC3 cells | Function assay | In vitro inhibitory concentration against cell proliferation in human PC-3 (prostate adenocarcinoma) tumor cells, IC50=0.12 μM | ||||
| HCT116 cells | Function assay | In vitro inhibitory concentration against cell proliferation in human HCT116 (colon carcinoma) tumor cells, IC50=0.25 μM | ||||
| human HeLa cells | Function assay | In vitro inhibitory concentration against cell proliferation in human HeLa (cervical adenocarcinoma) tumor cells, IC50=0.28 μM | ||||
| human A375 cells | Proliferation assay | Antiproliferative activity against human A375 cells, IC50=0.447 μM | ||||
| MDA-MB-231 cells | Function assay | In vitro inhibitory concentration against cell proliferation in various human MDA-MB-231 (breast carcinoma) tumor cells, IC50=0.59 μM | ||||
| SK-OV-3 cells | Function assay | In vitro inhibitory concentration against cell proliferation in human SK-OV-3 (ovarian adenocarcinoma) tumor cells, IC50=0.75 μM | ||||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 394.36 | Formel | C15H12F2N6O3S |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 443797-96-4 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | C1=CC(=C(C(=C1)F)C(=O)N2C(=NC(=N2)NC3=CC=C(C=C3)S(=O)(=O)N)N)F | ||
Löslichkeit
|
In vitro |
DMSO
: 79 mg/mL
(200.32 mM)
Ethanol : 3 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
A broad-spectrum inhibitor.
|
|---|---|
| Targets/IC50/Ki |
CDK2/CyclinE
(Cell-free assay) 3 nM
CDK2/CyclinA
(Cell-free assay) 4 nM
CDK1/CyclinB
(Cell-free assay) 9 nM
Aurora A
(Cell-free assay) 11 nM
Aurora B
(Cell-free assay) 15 nM
CDK3/CyclinE
(Cell-free assay) 58 nM
VEGFR2
(Cell-free assay) 154 nM
CDK6/CyclinD1
(Cell-free assay) 175 nM
FGFR2
(Cell-free assay) 226 nM
CDK4/CyclinD1
(Cell-free assay) 253 nM
GSK-3β
(Cell-free assay) 254 nM
Tie-2
(Cell-free assay) 465 nM
FGFR1
(Cell-free assay) 575 nM
VEGFR3
(Cell-free assay) 735 nM
|
| In vitro |
JNJ-7706621 zeigt auch eine gewisse Hemmung von VEGF-R2, FGF-R2 und GSK3β mit einem IC50 von 154-254 nM. Diese Verbindung zeigt eine hemmende Wirkung auf eine Reihe menschlicher Krebszelltypen, einschließlich HeLa, HCT-116, SK-OV-3, PC3, DU145, A375, MDA-MB-231, MES-SA und MES-SA/Dx5, mit einem IC50 von 112-514 nM, unabhängig vom p53-, Retinoblastom- oder P-Glykoprotein-Status. Es ist um ein Vielfaches weniger potent bei der Hemmung des Wachstums normaler Zelltypen, einschließlich MRC-5, HASMC, HUVEC und HMVEC, mit einem IC50 von 3,67-5,42 μM. In HeLa- oder U937-Zellen verzögert diese Chemikalie (0,5-3 μM) den Austritt aus der G1-Phase, arretiert Zellen in der G2-M-Phase, induziert Endoreduplikation, aktiviert Apoptose und reduziert die Koloniebildung. In einer HeLa-Zelllinie führt eine inkrementelle Behandlung mit steigenden Konzentrationen dieser Verbindung zu einer 16-fachen Resistenz, die durch ABCG2 vermittelt werden kann.
|
| Kinase-Assay |
In-vitro-Kinase-Assay für CDK1- und Aurora Kinase
|
|
Für die CDK1-Kinaseaktivität wird eine Methode entwickelt, bei der der aus Baculovirus gereinigte CDK1/Cyclin-B-Komplex verwendet wird, um ein biotinyliertes Peptidsubstrat zu phosphorylieren, das die Konsensus-Phosphorylierungsstelle für Histon H1 enthält, das in vivo durch CDK1 phosphoryliert wird. Die Hemmung der CDK1-Aktivität wird durch die Beobachtung einer reduzierten Menge an 33P-γ-ATP-Einbau in das immobilisierte Substrat in mit Streptavidin beschichteten 96-Well-Szintillationsmikroplatten gemessen. Das CDK1-Enzym wird in 50 mM Tris-HCl (pH 8), 10 mM MgCl2, 0,1 mM Na3VO4, 1 mM DTT, 1% DMSO, 0,25 μM Peptid, 0,1 μCi pro Well 33P-γ-ATP und 5 μM ATP in Gegenwart oder Abwesenheit verschiedener Konzentrationen dieser Verbindung verdünnt und 1 Stunde bei 30 °C inkubiert. Die Reaktion wird durch Waschen mit PBS, das 100 mM EDTA enthält, beendet und die Platten werden in einem Szintillationszähler gezählt. Eine lineare Regressionsanalyse der prozentualen Hemmung durch diese Chemikalie wird verwendet, um den IC50 zu bestimmen. Die Aurora Kinase-Assays werden mit 10 μM ATP und einem Peptid durchgeführt, das eine duale Wiederholung des Kemptid-Phosphorylierungsmotivs enthält.
|
|
| In vivo |
Im Maus-Xenograft-Modell des A375-Melanom-Menschentumors verursacht JNJ-7706621 (100 oder 125 mg/kg) eine Tumorrückbildung.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
