nur für Forschungszwecke
Mubritinib (TAK 165) HER2 Inhibitor
Kat.-Nr.S2216
Chemische Struktur
Molekulargewicht: 468.47
Qualitätskontrolle
| Verwandte Ziele | EGFR VEGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 c-Kit |
|---|---|
| Weitere HER2 Inhibitoren | CP-724714 Sapitinib (AZD8931) AC480 (BMS-599626) Tyrphostin AG 879 HER2-Inhibitor-1 TAS0728 Zongertinib |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 468.47 | Formel | C25H23F3N4O2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 366017-09-6 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | C1=CC(=CC=C1CCCCN2C=CN=N2)OCC3=COC(=N3)C=CC4=CC=C(C=C4)C(F)(F)F | ||
Löslichkeit
|
In vitro |
DMSO
: 13 mg/mL
(27.74 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
HER2/ErbB2
(BT-474 cells) 6.0 nM
|
|---|---|
| In vitro |
Mubritinib (TAK 165) zeigt eine > 4000-fache Selektivität gegenüber anderen Tyrosinkinasen wie EGFR, FGFR, PDGFR, Jak1, Src und Blk. Selbst bei einer geringen Konzentration von 0,1 μM blockiert es die HER2-Phosphorylierung signifikant, was zu einer Herunterregulierung des PI3K-Akt- und MAPK-Signalwegs in der Zelllinie BT474 mit hohem HER2-Spiegel führt. Diese Verbindung zeigt nicht nur eine hochpotente antiproliferative Wirkung in der ErbB2-überexprimierenden Krebszelllinie BT474 mit einer IC50 von 5 nM, sondern auch ausgeprägte antiproliferative Wirkungen in Zelllinien mit schwach exprimiertem HER2 mit IC50-Werten von 53 nM, 90 nM und 91 nM für LNCaP, LN-REC4 bzw. T24. Es zeigt keine hemmenden Aktivitäten gegen PC-3-Zellen mit sehr schwach exprimiertem HER2 mit einer IC50 von 4,62 μM sowie gegen EGFR-überexprimierende HT1376- und ACHN-Zelllinien mit einer IC50 von >25 μM. |
| Kinase-Assay |
Inhibition der HER2/erbB2 Protein Tyrosine Kinase-Aktivität
|
|
BT-474-Zellen werden auf 24-Well-Platten ausgesät und über Nacht kultiviert. Mubritinib (TAK 165) wird dann in verschiedenen Konzentrationen hinzugefügt. Nach 2 Stunden Inkubation werden die Zellen direkt in Natriumdodecylsulfat (SDS)-Probenpuffer (200 μL) geerntet. Aliquots, die gleiche Mengen an Gesamtzellextrakt enthalten, werden auf 7,5% bis 15% Gradienten-SDS-Polyacrylamid-Gelelektrophorese (PAGE) aufgetragen. Nach der Elektrophorese werden Proteine für die Western-Blot-Analyse unter Verwendung eines relevanten primären Antikörpers auf eine Polyvinylidenfluorid (PVDF)-Membran übertragen. Der Proteinnachweis erfolgt durch eine verstärkte chemilumineszente (ECL)-Nachweismethode. Das Ausmaß der Tyrosinphosphorylierung von HER2/erbB2 wird mit dem Lumino-Image-Analyser LAS-1000 plus gemessen. Die Konzentration dieser Verbindung, die die HER2/erbB2-Phosphorylierung um 50% (IC50) hemmt, wird aus einer Dosis-Wirkungs-Kurve berechnet, die mittels linearer Regression nach der Methode der kleinsten Quadrate mit der SAS-Software erstellt wurde.
|
|
| In vivo |
Mubritinib (TAK 165) hemmt signifikant das LN-REC4-Xenograft mit einem Verhältnis des Tumorvolumens von Behandlung/Kontrolle von 26,5 %. Obwohl in vitro unwirksam zur Hemmung des Wachstums von UMUC-3- und ACHN-Zellen (IC50-Werte von 1,812 bzw. >25 μM), hemmt die orale Verabreichung dieser Verbindung (10 oder 20 mg/kg pro Tag) das Wachstum von UMUC-3- und ACHN-Xenografts signifikant mit einem Verhältnis des Tumorvolumens von Behandlung/Kontrolle von 22,9 % bzw. 26 %, verglichen mit 20 mg/kg, was für das UMUC-3-Tumorwachstum unwirksam ist. |
Literatur |
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
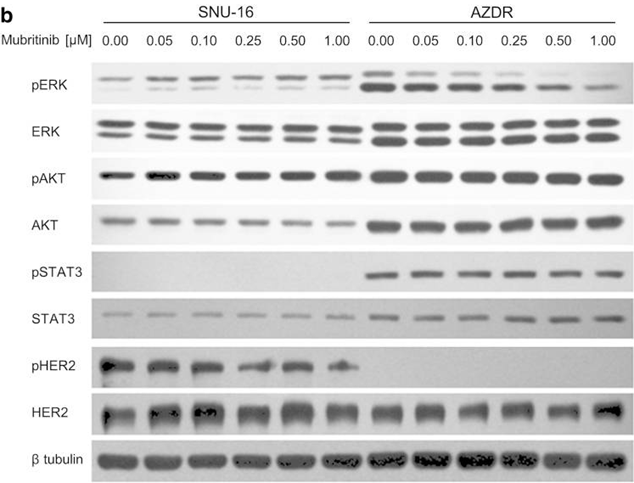
| Western blot | pERK / ERK / pAKT / AKT / p-STAT3 / STAT3 / pHER2 / HER2 c-myc / p21 / p27 |
|
25407459 |
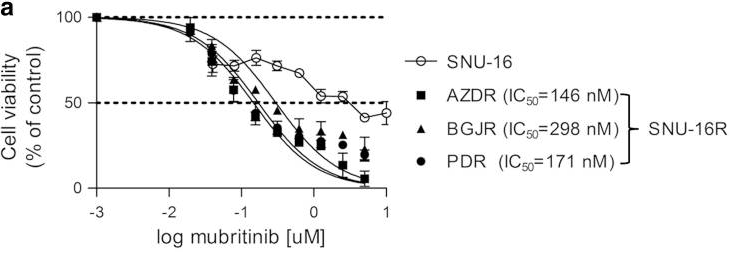
| Growth inhibition assay | Cell viability |
|
25407459 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT00034281 | Completed | Breast Neoplasm|Pancreatic Neoplasm|Lung Neoplasm|Ovarian Neoplasm|Renal Neoplasm |
Takeda |
June 2002 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
