nur für Forschungszwecke
Rufinamide Sodium Channel Inhibitor
Kat.-Nr.S1256
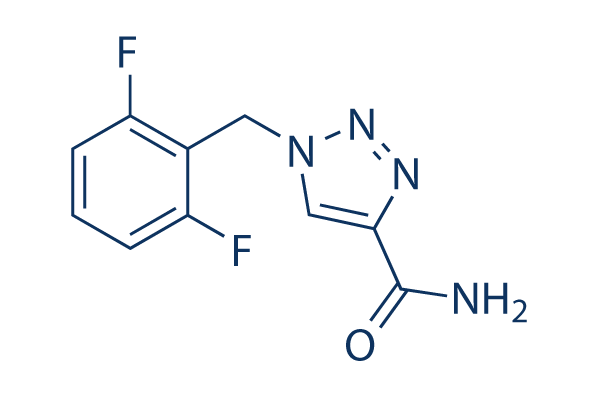
Chemische Struktur
Molekulargewicht: 238.19
Qualitätskontrolle
| Verwandte Ziele | CFTR CRM1 CD markers AChR Calcium Channel Potassium Channel GABA Receptor TRP Channel ATPase GluR |
|---|---|
| Weitere Sodium Channel Inhibitoren | Camostat Mesilate A-803467 cariporide Tolperisone HCl Vinpocetine Veratramine Bulleyaconi cine A Ambroxol HCl Benzocaine Nefopam HCl |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 238.19 | Formel | C10H8F2N4O |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 106308-44-5 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | CGP 33101,E 2080,RUF 331,Banzel | Smiles | C1=CC(=C(C(=C1)F)CN2C=C(N=N2)C(=O)N)F | ||
Löslichkeit
|
In vitro |
DMSO
: 47 mg/mL
(197.32 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Sodium channel
|
|---|---|
| In vitro |
Rufinamide wird ausgiebig durch Nicht-CYP450-Systeme mit einer Halbwertszeit von 8-12 Stunden metabolisiert. Es wird angenommen, dass sein Wirkmechanismus die Hemmung natriumabhängiger Aktionspotentiale in Neuronen ist, mit möglichen membraninstabilisierenden Effekten. Diese Verbindungshydrolyse wird hauptsächlich durch die humane Carboxylesterase (hCE) 1 vermittelt und ist bis zu 500 μM nicht sättigbar. |
| In vivo |
Rufinamide, das gesunden Hunden oral in einer Dosis von 20 mg/kg alle 12 Stunden verabreicht wird, sollte zu einer Plasmakonzentration und Halbwertszeit führen, die ausreichen, um das vom Menschen extrapolierte therapeutische Niveau ohne kurzfristige Nebenwirkungen bei erwachsenen Hunden zu erreichen. Diese Verbindung lindert verletzungsbedingte mechanische Allodynie für 4 Stunden. Sie reduziert den Spitzenstrom und stabilisiert den inaktivierten Zustand des spannungsgesteuerten sodium channel Nav1.7, mit ähnlichen Effekten in Neuronen des dorsalen Wurzelganglions im Neuropathischen Schmerzmodell der Spared Nerve Injury bei Mäusen. Diese Chemikalie unterdrückt Pentylentetrazol-induzierte Anfälle bei Mäusen (ED(50) 45,8 mg/kg), aber nicht bei Ratten, und ist aktiv gegen MES-induzierte tonische Anfälle bei Mäusen (ED(50) 23,9 mg/kg) und Ratten (ED(50) 6,1 mg/kg). Sie unterdrückt Pentylentetrazol-, Bicucullin- und Picrotoxin-induzierten Klonus bei Mäusen (ED(50) 54,0, 50,5 bzw. 76,3 mg/kg). Diese Verbindung ist im Mäuse-Strychnin-Test teilweise wirksam. |
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT01151540 | Completed | Lennox-Gastaut Syndrome |
Eisai Co. Ltd.|Eisai Inc. |
November 2010 | Phase 3 |
| NCT01991041 | Completed | Lennox-Gastaut Syndrome |
Eisai Limited|Eisai Inc. |
June 2008 | -- |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
