nur für Forschungszwecke
BMS-986142 BTK Inhibitor
Kat.-Nr.S8381
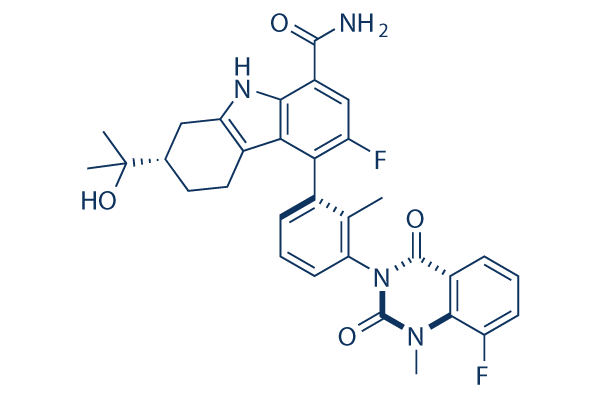
Chemische Struktur
Molekulargewicht: 572.60
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- HPLC
- SDS
- Datenblatt
| Verwandte Ziele | EGFR VEGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 |
|---|---|
| Weitere BTK Inhibitoren | Catadegbrutinib (BGB-16673) Spebrutinib (AVL-292) tirabrutinib(ONO-4059) hydrochloride CGI1746 LFM-A13 CNX-774 Evobrutinib BMS-935177 Fenebrutinib (GDC-0853) Branebrutinib (BMS-986195) |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 572.60 | Formel | C32H30F2N4O4 |
Lagerung (Ab dem Eingangsdatum) | 3 years -20°C powder |
|---|---|---|---|---|---|
| CAS-Nr. | 1643368-58-4 | -- | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC1=C(C=CC=C1N2C(=O)C3=C(C(=CC=C3)F)N(C2=O)C)C4=C(C=C(C5=C4C6=C(N5)CC(CC6)C(C)(C)O)C(=O)N)F | ||
Löslichkeit
|
In vitro |
DMSO
: 100 mg/mL
(174.64 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
BTK
(Cell-free assay) 0.5 nM
|
|---|---|
| In vitro |
In B-Zellen, die über den B-Zell-Rezeptor (BCR) stimuliert wurden, hemmt BMS-986142 stark die Signalgebung und funktionelle Endpunkte, einschließlich Kalziumfluss (IC50 = 9 nM), Produktion von Zytokinen, Proliferation und Oberflächenexpression des kostimulatorischen Moleküls CD86 (IC50 = 3–4 nM). In T-Zellen wird die ITK-katalysierte Phosphorylierung von PLCγ1, die über den T-Zell-Rezeptor (TCR) stimuliert wird, durch diese Verbindung mindestens 45-mal weniger stark gehemmt als BTK-abhängige Signalendpunkte in B-Zellen, wie aufgrund der 30-fachen Selektivität für BTK gegenüber ITK in den enzymatischen Assays erwartet. |
| Kinase-Assay |
Humaner rekombinanter BTK-Enzymtest
|
|
Zu 384-Well-Platten mit V-Boden wurden Testverbindungen, humane rekombinante BTK (1 nM), fluoreszeiniertes Peptid (1,5 μM), ATP (20 μM) und Assay-Puffer (20 mM HEPES bei pH 7,4, 10 mM MgCl2, 0,015 % Brij 35-Tensid und 4 mM DTT in 1,6 % DMSO) mit einem Endvolumen von 30 μL gegeben. Nach Inkubation bei Raumtemperatur für 60 Minuten wurde die Reaktion durch Zugabe von 45 μL 35 mM EDTA zu jeder Probe beendet. Das Reaktionsgemisch wurde durch elektrophoretische Trennung des fluoreszierenden Substrats und des phosphorylierten Produkts analysiert. Die Hemmdaten wurden durch Vergleich mit Kontrollreaktionen ohne Enzym (für 100 % Hemmung) und Kontrollen ohne Inhibitor (für 0 % Hemmung) berechnet. Dosis-Wirkungs-Kurven wurden erstellt, um die Konzentration zu bestimmen, die zur Hemmung von 50 % der BTK-Aktivität (IC50) erforderlich ist. Diese Verbindung wurde in 10 mM DMSO gelöst und bei 11 Konzentrationen bewertet.
|
|
| In vivo |
In pharmakokinetischen Studien an mehreren Spezies beträgt die absolute orale Bioverfügbarkeit von BMS-986142 93 % bei Mäusen, 67 % bei Ratten, 33 % bei Javaneraffen und 100 % bei Hunden. Die Gesamtplasma-Clearance dieser Verbindung ist bei allen Spezies gering. Das beobachtete große Verteilungsvolumen im Steady-State ist trotz der hohen Proteinbindung ein Hinweis auf eine extravaskuläre Verteilung. Die Hirnpenetration ist jedoch bei Ratten sehr gering (<5 % der Plasmakonzentration). Diese Verbindung blockiert die Zunahme einer schweren Proteinurie in einem weiblichen NZB/W Lupus-anfälligen Mausmodell in vivo. Die Behandlung mit dieser Chemikalie bietet einen robusten Schutz vor tubulo-interstitieller und glomerulärer Nephritis sowie entzündlicher Infiltration. |
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT02638948 | Completed | Rheumatoid Arthritis |
Bristol-Myers Squibb |
February 16 2016 | Phase 2 |
| NCT02257151 | Completed | Healthy Adult |
Bristol-Myers Squibb |
September 2014 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
