nur für Forschungszwecke
BTSA1 Bcl-2 Aktivator
Kat.-Nr.S8650
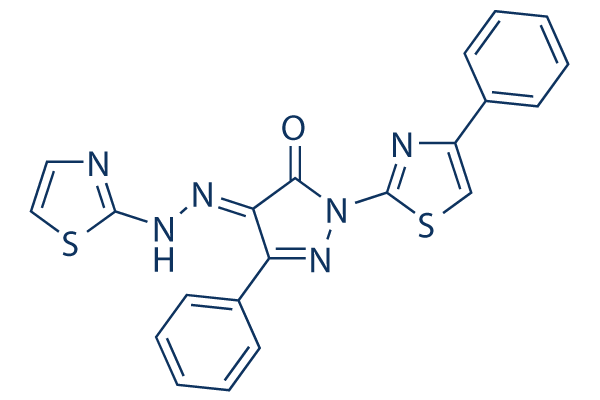
Chemische Struktur
Molekulargewicht: 430.51
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- HPLC
- SDS
- Datenblatt
| Verwandte Ziele | Caspase PD-1/PD-L1 Ferroptosis p53 Apoptosis related Synthetic Lethality STAT TNF-alpha Ras KRas |
|---|---|
| Weitere Bcl-2 Inhibitoren | Navitoclax (ABT-263) S63845 ABT-737 Obatoclax Mesylate (GX15-070) A-1331852 A-1210477 TW-37 A-1155463 Dihydrochloride AZD5991 UMI-77 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 430.51 | Formel | C21H14N6OS2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 314761-14-3 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | C1=CC=C(C=C1)C2=CSC(=N2)N3C(=O)C(=C(N3)C4=CC=CC=C4)N=NC5=NC=CS5 | ||
Löslichkeit
|
In vitro |
DMSO
: 81 mg/mL
(188.14 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Bax
|
|---|---|
| In vitro |
BTSA1 hat keine Kapazität, den pro-apoptotischen Homolog BAK direkt zu aktivieren. Diese Verbindung induziert potent und dosisabhängig die Membrantranslokation von rekombinantem löslichem BAX zur mitochondrialen Membran, gefolgt von der Induktion der BAX-Oligomerisierung. Diese chemisch-induzierte BAX-Aktivierung fördert die Apoptose in Krebszellen. Es reduziert die Lebensfähigkeit aller AML-Zelllinien dosisabhängig mit IC50-Werten zwischen 1 und 4 μM, was innerhalb von 24 Stunden Behandlungszeit zu einem vollständigen Effekt führt. Es induziert eine dosisabhängige Caspase-3/7-Aktivierung in allen fünf AML-Zelllinien.
|
| In vivo |
BTSA1 unterdrückt potent menschliche Xenografts der akuten myeloischen Leukämie (AML) und erhöht das Überleben des Wirts ohne Toxizität. Es wird in Mäusen gut vertragen, ohne toxische Effekte auf die gesunde Hämatopoese, einschließlich gesunder stammzellangereicherter (LSK) Zellen, gemeinsamer myeloischer Vorläuferzellen, Granulozyten-Monozyten-Vorläuferzellen und Megakaryozyten-Erythrozyten-Vorläuferzellen. Diese Verbindung hat eine beträchtliche Halbwertszeit im Mausplasma (T1/2 = 15 Std.) und orale Bioverfügbarkeit (%F = 51), während eine Dosis von 10 mg/kg ausreichende Spiegel (~15 μM) der Verbindung erreicht, um die BAX-Aktivierung und Apoptosis in Leukämiezellen zu induzieren. Somit ist es oral bioverfügbar mit ausgezeichneter Pharmakokinetik, hat eine signifikante Anti-Tumor-Aktivität in Leukämie-Xenografts durch Förderung der Apoptosis und zeigt bei therapeutisch wirksamen Dosen keine nachweisbare Toxizität im hämatopoetischen System oder anderen Geweben.
|
Literatur |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
