nur für Forschungszwecke
C646 Histonacetyltransferase p300 Inhibitor
Kat.-Nr.S7152
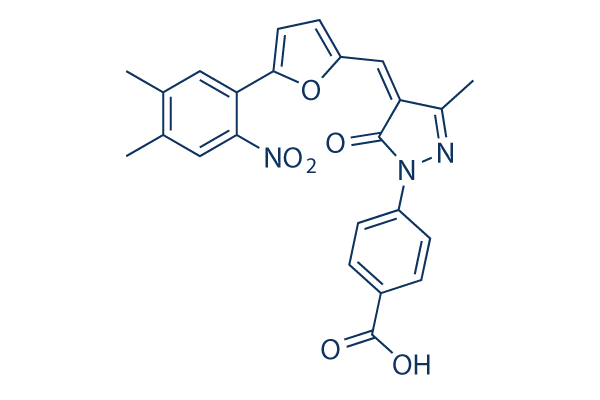
Chemische Struktur
Molekulargewicht: 445.42
Qualitätskontrolle
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| NE-4C cells | Function assay | 0-5 μM | high glucose induced increases of H4K5ac and H4K5/8/12/16ac levels in NE-4C cells are inhibited by addition of a selective CBP/p300 inhibitor C646 in a dose-dependent way (from 0 to 5 μM) | 30114346 | ||
| SH-SY5Y | Function assay | 20 μM | 24 h | Co-treatment with 20 µM C646 suppressed the effect of TSA treatment on Alox15 mRNA expression by 65.7% | 29235036 | |
| GES-1 | Function assay | 10 μM | 6 h | C646 treatment significantly reduced the levels of histone H3 acetylation in both GC cells and normal gastric epithelial cells (P<0.05) | 29075795 | |
| SGC-7901 | Function assay | 10 μM | 6 h | C646 treatment significantly reduced the levels of histone H3 acetylation in both GC cells and normal gastric epithelial cells (P<0.05) | 29075795 | |
| MKN45 | Function assay | 10 μM | 6 h | C646 treatment significantly reduced the levels of histone H3 acetylation in both GC cells and normal gastric epithelial cells (P<0.05) | 29075795 | |
| MGC-803 | Function assay | 10 μM | 6 h | C646 treatment significantly reduced the levels of histone H3 acetylation in both GC cells and normal gastric epithelial cells (P<0.05) | 29075795 | |
| BGC-823 | Function assay | 10 μM | 6 h | C646 treatment significantly reduced the levels of histone H3 acetylation in both GC cells and normal gastric epithelial cells (P<0.05) | 29075795 | |
| KATO III | Function assay | 10 μM | 6 h | C646 treatment significantly reduced the levels of histone H3 acetylation in both GC cells and normal gastric epithelial cells (P<0.05) | 29075795 | |
| Raw246.7 | Function assay | 1, 5, 10, 15, 20, 25, or 30 μM | 16 h | results in significant inhibition of LPS and IFNγ induced NF-κB promoter activity at 15 μM or higher concentrations | 26718586 | |
| WM35 | Function assay | 10 μM and 20 μM | 24 h | a dose-dependent decrease in the protein levels of cyclins A and E, accompanied by an increased expression of p53 and its downstream effector p21 | 23698071 | |
| 1205Lu | Function assay | 10 μM and 20 μM | 24 h | a dose-dependent decrease in the protein levels of cyclins A and E, accompanied by an increased expression of p53 and its downstream effector p21 | 23698071 | |
| WM983B | Function assay | 10 μM and 20 μM | 24 h | a dose-dependent decrease in the protein levels of cyclins A and E, accompanied by an increased expression of p53 and its downstream effector p21 | 23698071 | |
| Kasumi-1 | Growth inhibition assay | 10, 25 and 50 μM | 0, 24, 48, 72 h | cellular growth and colony formation were dramatically suppressed upon C646 treatment. | 23390536 | |
| SKNO-1 | Growth inhibition assay | 10, 25 and 50 μM | 0, 24, 48, 72 h | cellular growth and colony formation were dramatically suppressed upon C646 treatment. | 23390536 | |
| BL21(RIL)-DE3 | Function assay | 10 mins | Inhibition of synthetic VMA-tagged p300 (1287 to 1652 residues) (unknown origin) expressed in Escherichia coli BL21(RIL)-DE3 cells using H4-15 peptide substrate incubated for 10 mins by radiometric filter binding assay in presence of [14C]acetyl-CoA, Ki = 0.4 μM. | 26701186 | ||
| BL21(RIL)-DE3 | Function assay | 10 mins | Inhibition of synthetic VMA-tagged p300 (1287 to 1652 residues) (unknown origin) expressed in Escherichia coli BL21(RIL)-DE3 cells using H4-15 peptide substrate incubated for 10 mins by radiometric filter binding assay in presence of [14C]acetyl-CoA, IC50 = 1.6 μM. | 26701186 | ||
| BL21-CodonPlus(DE3)-RIL | Function assay | 10 mins | Inhibition of FLAG-tagged p300 (1195 to 1673 residues) (unknown origin) expressed in competent Escherichia coli BL21-CodonPlus(DE3)-RIL cells using histone H4 substrate incubated for 10 mins by scintillation counting method in presence of [14C]acetyl-CoA, IC50 = 9 μM. | 26701186 | ||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 445.42 | Formel | C24H19N3O6 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 328968-36-1 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC1=CC(=C(C=C1C)[N+](=O)[O-])C2=CC=C(O2)C=C3C(=NN(C3=O)C4=CC=C(C=C4)C(=O)O)C | ||
Löslichkeit
|
In vitro |
DMSO
: 11 mg/mL
(24.69 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
Extensively used as a pharmacologic probe in cancer cells. Potential use for prostate and lung cancers.
|
|---|---|
| Targets/IC50/Ki |
p300/CBP
(Cell-free assay) 400 nM(Ki)
|
| In vitro |
C646 ist ein Inhibitor der Histone Acetyltransferase, hemmt p300 mit einem Ki von 400 nM und ist selektiv gegenüber anderen Acetyltransferasen. Diese Verbindung bewirkt in vitro bei 10 μM eine 86%ige Hemmung von p300. Es handelt sich um einen klassischen reversiblen p300-Inhibitor. Diese chemische Behandlung (25μM) reduziert die Acetylierungslevel von Histon H3 und H4 und hebt die TSA-induzierte Acetylierung in Zellen auf. Es (20μM) induziert Apoptose in androgenempfindlichen und kastrationsresistenten Prostatakrebszelllinien, indem es die AR- und NF-kB-Signalwege beeinflusst. Diese Verbindung blockiert die dynamische Acetylierung von H3K4me3 global in Maus- und Fliegenzellen sowie lokal über den Promotor und die Startstelle induzierbarer Gene in der Maus, wodurch die Assoziation von RNA-Polymerase II und die Aktivierung dieser Gene gestört werden.
|
| Kinase-Assay |
Radioaktiver Assay
|
|
IC50-Werte für die putativen p300 HAT-Inhibitoren werden unter Verwendung des oben beschriebenen direkten radioaktiven Assays bestimmt. Die Reaktionen werden in 20 mM HEPES (pH 7,9) durchgeführt und enthielten 5 mM DTT, 80 μM EDTA, 40 μg/ml BSA, 100 μM H4-15 und 5 nM p300. Putative Inhibitoren werden über einen Konzentrationsbereich hinzugefügt, wobei die DMSO-Konzentration konstant (<5%) gehalten wird. Die Reaktionen werden 10 Minuten bei 30 °C inkubiert und dann mit der Zugabe einer 1:1-Mischung aus 12C-Acetyl-CoA und 14C-Acetyl-CoA zu 20 mM gestartet. Nach 10 Minuten bei 30 °C werden die Reaktionen mit 14% SDS (w/v) abgeschreckt. Alle Konzentrationen werden doppelt gescreent. Gele werden gelaufen, gewaschen, getrocknet und einer PhosphorImager-Platte ausgesetzt, und die Produktion von Ac-H4-15 wird quantifiziert, um IC50-Werte zu erhalten.
|
|
| In vivo |
C646, infundiert in den ILPFC unmittelbar nach einem schwachen Extinktionstraining, verstärkt die Konsolidierung des Furchtextinktionsgedächtnisses. Diese Verbindung mildert die mechanische Allodynie und die thermische Hyperalgesie, begleitet von einer unterdrückten COX-2-Expression im Rückenmark.
|
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | α-c-Myc Cyclin A1/2 / Cyclin E2 / p53 / p21 H3K27Ac |
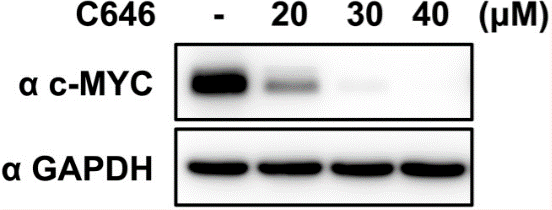
|
28630312 |
| Immunofluorescence | BRD4 / p300 |
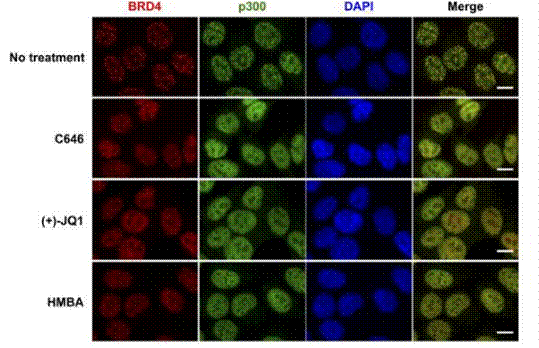
|
28630312 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
Häufig gestellte Fragen
Frage 1:
I am planning to conduct IP studies in mice with it, any specific vehicle that you can recommend to me?
Antwort:
It can be dissolved in 5% DMSO+30% PEG 300+ddH2O at 1 mg/ml as a clear solution, and should be ok for i.p. injection.
