nur für Forschungszwecke
H3B-6527 FGFR Inhibitor
Kat.-Nr.S8675
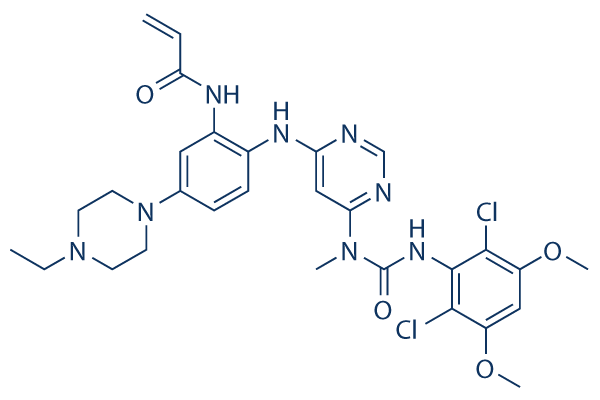
Chemische Struktur
Molekulargewicht: 629.54
Qualitätskontrolle
| Verwandte Ziele | EGFR VEGFR PDGFR c-Met Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Weitere FGFR Inhibitoren | PD173074 AZD4547 (Fexagratinib) BLU9931 Futibatinib (TAS-120) LY2874455 PD-166866 Zoligratinib (Debio-1347) Fisogatinib (BLU-554) SSR128129E Ferulic Acid |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 629.54 | Formel | C29H34Cl2N8O4 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1702259-66-2 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CCN1CCN(CC1)C2=CC(=C(C=C2)NC3=CC(=NC=N3)N(C)C(=O)NC4=C(C(=CC(=C4Cl)OC)OC)Cl)NC(=O)C=C | ||
Löslichkeit
|
In vitro |
DMSO
: 50 mg/mL
(79.42 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
FGFR4
(Cell-free assay) <1.2 nM
|
|---|---|
| In vitro |
H3B-6527 zeigt eine robuste Hemmung der Zielkinase FGFR4 mit einem IC50-Wert von <1,2 nmol/L und einer mindestens 250-fachen Selektivität gegenüber FGFR1-3 (IC50-Werte von 320, 1.290 bzw. 1.060 nmol/L). TAOK2, JNK2 und CSF1R sind ebenfalls weniger empfindlich gegenüber dieser Verbindung mit IC50-Werten von 690, >10.000 bzw. >10.000 nmol/L. Diese Chemikalie hemmt die FGFR4-Signalübertragung, Proliferation und führt zur Apoptose in einer HCC-Zelllinie (hepatozelluläres Karzinom). Die Behandlung von Hep3B-Zellen führt zu einer robusten Aktivierung von Caspase-3/7, einem apoptotischen Marker, in einer konzentrationsabhängigen Weise, was darauf hinweist, dass die FGFR4-Hemmung durch diese Verbindung zum Zelltod in HCC-Zelllinien führt. Es weist die Selektivität und die selektive Abhängigkeit von FGFR4 über verschiedene Krebsarten hinweg auf. |
| In vivo |
Im humanen HCC-Xenotransplantat-Mausmodell Hep3B zeigt H3B-6527 dosisproportionale Plasmaexpositionen und eine überproportionale Tumorexposition innerhalb des evaluierten Dosisbereichs (30, 100 und 300 mg/kg). Die pharmakodynamische Reaktion dieser Verbindung, gemessen an CYP7A1-mRNA- und pERK1/2-Proteinspiegeln, ist dosisabhängig, wobei höhere Dosen zu anhaltenden Reaktionen führen. Die orale Behandlung dieser Chemikalie zweimal täglich hemmt das Xenotransplantatwachstum dosisabhängig bei Nacktmäusen, wobei 300 oder 100 mg/kg zweimal täglich das Tumorwachstum sowohl im subkutanen als auch im orthotopen Hep3B-Xenotransplantatmodell signifikant hemmt und im subkutanen Xenotransplantatmodell zu Tumorregressionen führt. |
Literatur |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT03424577 | Completed | Healthy Participants |
Eisai Inc.|H3 Biomedicine Inc. |
December 27 2017 | Phase 1 |
| NCT02834780 | Completed | Advanced Hepatocellular Carcinoma|Hepatocellular Carcinoma|Liver Cancer|Liver Neoplasms|Hepatic Cancer|Hepatic Carcinoma |
H3 Biomedicine Inc.|Eisai Inc. |
December 28 2016 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
