nur für Forschungszwecke
HPI-4 (Ciliobrevin A) Hedgehog/Smoothened Inhibitor
Kat.-Nr.S8249
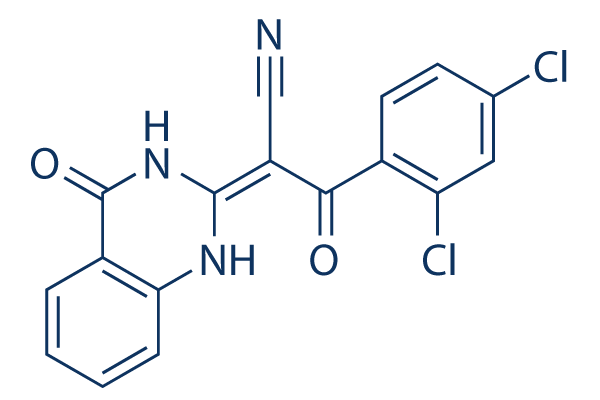
Chemische Struktur
Molekulargewicht: 358.18
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- HPLC
- SDS
- Datenblatt
| Verwandte Ziele | JAK TGF-beta/Smad Wnt/beta-catenin ERK GSK-3 ROCK PKA Secretase STAT Casein Kinase |
|---|---|
| Weitere Hedgehog/Smoothened Inhibitoren | SAG (Smoothened Agonist) Hydrochloride Purmorphamine Cyclopamine (11-Deoxojervine) GANT61 SAG (Smoothened Agonist) SANT-1 BMS-833923 Taladegib (LY2940680) Ciliobrevin D PF-5274857 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 358.18 | Formel | C17H9Cl2N3O2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 302803-72-1 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | Hedgehog Pathway Inhibitor 4 | Smiles | C1=CC=C2C(=C1)C(=O)NC(=N2)C(=C(C3=C(C=C(C=C3)Cl)Cl)O)C#N | ||
Löslichkeit
|
In vitro |
DMSO
: 71 mg/mL
(198.22 mM)
Ethanol : 1 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Hedgehog
|
|---|---|
| In vitro |
HPI-4 (Ciliobrevin A) zielt nicht direkt auf Smo ab. Es wirkt den Aktivitäten von endogenem Gli1 und Gli2 entgegen, wirkt aber nicht direkt auf die Transkriptionsfaktor-GLIs. Diese Verbindung hemmte signifikant die Proliferation dieser neuronalen Vorläuferzellen, gemessen an den Histon-H3-Phosphorylierungs-(pH3)-Spiegeln. Es reduzierte auch die zellulären Spiegel von Cyclin-D1-Protein und Gli1-, Gli2- und N-Myc-Transkripten in den zerebellären Granulozyten-Vorläuferzellen. Es wirkt durch Störung der Ziliogenese. Die Behandlung mit diesem Inhibitor könnte die Proliferation, Invasion und Migrationsfähigkeit menschlicher Chondrosarkomzellen signifikant verringern. Ferner könnte es die HH-Signalweg-vermittelte Ziliogenese deutlich stören und die Expression des primären zilienbezogenen Proteins intraflagellärer Transportprotein IFT88 unterdrücken. Das HH-nachgeschaltete Effektorprotein GLI2 wurde eingeschränkt, um das Parathormon-verwandte Protein zu blockieren und MAPK/ERK-regulierte Matrixmetalloproteinasen (MMP2 und MMP9) zu beeinflussen. Es ist auch ein niedermolekularer Inhibitor der katalytischen schweren Kettensubunit des zytoplasmatischen Dyneins.
|
| In vivo |
In einem Zebrafischmodell verhinderte die Behandlung mit HPI-4 (Ciliobrevin A), einem Ziliogenese-Inhibitor, effektiv die Pankreasfibrose und -zerstörung.
|
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | β-catenin |
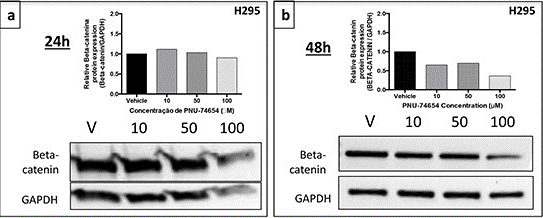
|
26515592 |
| Growth inhibition assay | Cell viability |
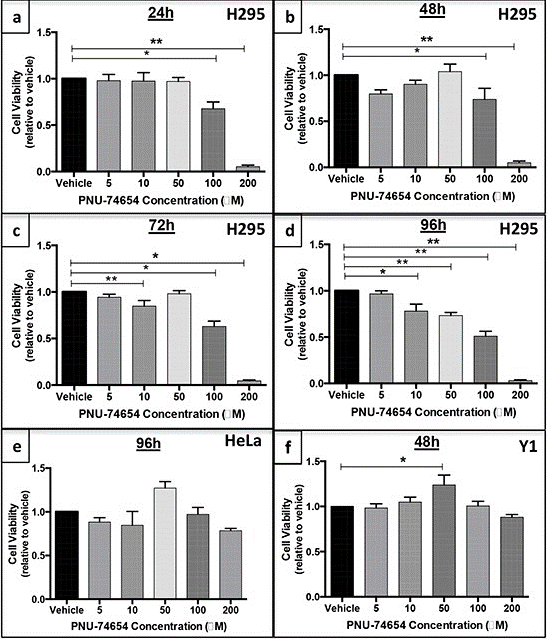
|
26515592 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
