nur für Forschungszwecke
PF-5274857 Hedgehog/Smoothened Antagonist
Kat.-Nr.S2777
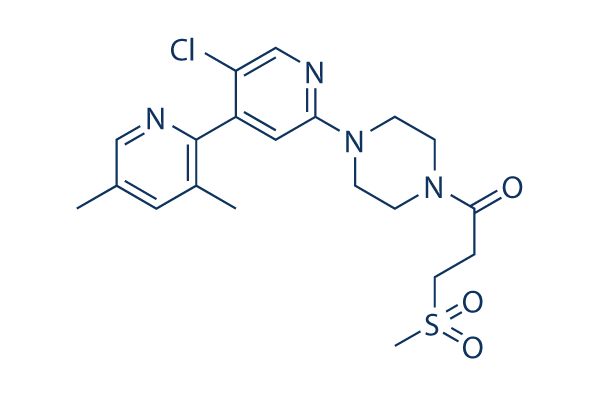
Chemische Struktur
Molekulargewicht: 436.96
Qualitätskontrolle
| Verwandte Ziele | JAK TGF-beta/Smad Wnt/beta-catenin ERK GSK-3 ROCK PKA Secretase STAT Casein Kinase |
|---|---|
| Weitere Hedgehog/Smoothened Inhibitoren | SAG (Smoothened Agonist) Hydrochloride Purmorphamine Cyclopamine (11-Deoxojervine) GANT61 SAG (Smoothened Agonist) SANT-1 HPI-4 (Ciliobrevin A) BMS-833923 Taladegib (LY2940680) Ciliobrevin D |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 436.96 | Formel | C20H25ClN4O3S |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1373615-35-0 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC1=CC(=C(N=C1)C2=CC(=NC=C2Cl)N3CCN(CC3)C(=O)CCS(=O)(=O)C)C | ||
Löslichkeit
|
In vitro |
DMSO
: 93 mg/mL
(212.83 mM)
Water : 93 mg/mL Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Smoothened
4.6 nM(Ki)
Smoothened
5.8 nM
|
|---|---|
| In vitro |
PF-5274857 hemmt die Shh-induzierte Hh-Signalwegaktivität vollständig mit einer IC50 von 2,7 nM, gemessen an der transkriptionellen Aktivität des Smo-nachgeschalteten Gens Gli1 in MEF-Zellen. Der μ-Opioidrezeptor wird durch diese Verbindung schwach gehemmt, wobei eine Dissoziationskonstante von 36 μM anschließend in einem funktionellen Assay bestimmt wurde.
|
| Kinase-Assay |
Biochemische Assays
|
|
HEK293-Zellen, die humanes Smo (Aminosäuren 181-787) überexprimieren, werden in Dulbecco's Modified Eagle's Media (DMEM) mit 10 % FBS, Pen–Strep und 0,1 mg/mL Hygromycin bis zu 90 % Konfluenz kultiviert. Nach dem Waschen mit kaltem Dulbecco's PBS wird das Zellpellet in Membranpräparationspuffer (50 mM Tris-HCl, pH 7,5, 250 mM Saccharose mit Roche kompletter Proteasecocktail) resuspendiert und homogenisiert. Das Homogenat wird zentrifugiert und das Zellpellet in Assaypuffer (50 mM Tris-HCl, pH 7,5, 100 mM NaCl, 25 mM MgCl2, 1 mM EDTA und 0,1 % proteasfreies Rinderserumalbumin) resuspendiert und in einem Gewebemörser aus Glas homogenisiert. Das Gesamtprotein in der Smo enthaltenden Membranpräparation wird mit dem Pierce BCA-Proteinassay bestimmt. Für den kompetitiven Bindungsassay werden 100 μL Assaypuffer 10 Minuten lang in eine 96-Well-GF/B-Filterplatte gegeben, um den Filter vorzufeuchten, und dann entfernt. Anschließend werden folgende Reagenzien hinzugefügt: 20 μL Assaypuffer, 10 μL serielle Verdünnungen dieser Verbindung, 20 μL 3H-Smo-Antagonist (3 nM Endkonzentration) und 50 μL Membranpräparation (40 μg Gesamtprotein). Die Platten werden 2 Stunden lang bei Raumtemperatur inkubiert, dann gewaschen und vakuumgetrocknet. Die Platten werden dann 1 Stunde lang in einem 60 °C Ofen getrocknet, bevor 45 μL Microscint 20 hinzugefügt und 30 Minuten bis 1 Stunde bei Raumtemperatur inkubiert werden, danach in einem TopCount-Szintillationszähler gezählt werden. Die Daten werden mit der GraphPad Prism-Software analysiert.
|
|
| In vivo |
PF-5274857 zeigt eine signifikante dosisabhängige Tumorwachstumsinhibition (TGI) und induziert bei hohen Dosen (>10 mg/kg) eine Tumorrückbildung. Diese Verbindung reguliert die Genexpressionsniveaus von Gli1, Gli2, Ptch1 und Ptch2 in unterschiedlichem Maße herunter, wobei die maximalen Effekte zwischen 6 und 12 Stunden nach der Dosis erreicht werden (Gli1 ist das empfindlichste Gen), während sie nur geringe Auswirkungen auf die Smo-Spiegel hat. Im Hautgewebe wird auch eine Herunterregulierung von Gli1 und Gli2 mit einem ähnlichen Zeitverlauf durch diese Chemikalie beobachtet. Die modellabgeleitete Wirkstoffkonzentration für die halbmaximale Hemmung der Gli1-mRNA-Produktionsrate im Tumor (IC50) durch diese Verbindung wird in Ptch+/−p53+/−-Medulloblastom-Allograft-Mäusen auf 8,9 nM bestimmt, was mathematisch einer Tumorrückbildung von 119 % TGI nach 6 Tagen Plasmaexposition bei dieser Konzentration entspricht. In Ptch+/−p53−/−-Medulloblastom-Allograft-Mäusen wird der IC50-Wert auf 3,5 nM geschätzt, was mit den Ptch+/−p53+/−-Ergebnissen übereinstimmt. Es ist auch in der Lage, die Blut-Hirn-Schranke bei Ratten innerhalb von 4 Stunden nach der Dosis zu passieren.
|
Literatur |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
