nur für Forschungszwecke
Lycorine hydrochloride ADC Cytotoxin Inhibitor
Kat.-Nr.S3800
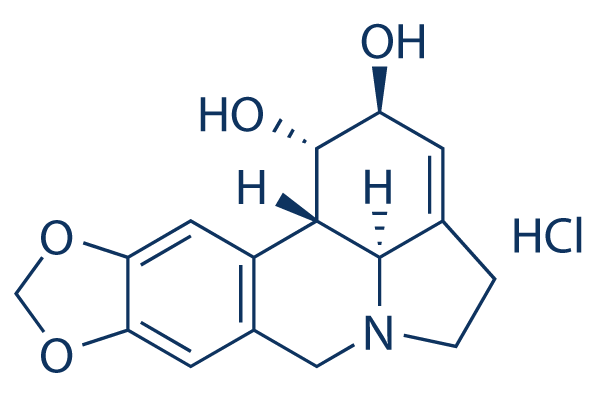
Chemische Struktur
Molekulargewicht: 323.77
Qualitätskontrolle
| Verwandte Ziele | HDAC Caspase Proteasome Secretase MMP HCV Protease Cysteine Protease DPP Tyrosinase HIV Protease |
|---|---|
| Weitere ADC Cytotoxin Inhibitoren | Triptolide SN-38 Luteolin (+)-Bicuculline Rutin Artemisinin BHQ Pinocembrin Harmine hydrochloride Luteoloside |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 323.77 | Formel | C16H17NO4.HCl |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 2188-68-3 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | Galanthidine hydrochloride, Amarylline hydrochloride, Narcissine hydrochloride, Licorine hydrochloride | Smiles | C1CN2CC3=CC4=C(C=C3C5C2C1=CC(C5O)O)OCO4.Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 65 mg/mL
(200.75 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| In vitro |
Lycorine besitzt nicht nur starke pharmakologische Wirkungen bei vielen Krankheiten, einschließlich Anti-Leukämie, Anti-Tumor, Anti-Angiogenese, Anti-Virus, Anti-Bakterien, Anti-Entzündungen und Anti-Malaria, sondern übt auch viele andere biologische Funktionen aus, wie die Hemmung von Acetylcholinesterase und Topoisomerase, die Unterdrückung der Ascorbinsäurebiosynthese und die Kontrolle der zirkadianen Periodenlänge. Lycorine hemmt die Zellproliferation und induziert die Zellapoptose in der akuten myeloischen Leukämie (AML)-Zelllinie HL-60, der Monozytenleukämie-Zelllinie U937 und der T-Zell-Leukämie-Zelllinie Jurkat. Lycorine blockiert auch den KM3-Zellzyklus des multiplen Myeloms, induziert den K562-Zellzyklus-Arrest in der G0/G1-Phase und unterdrückt die Tumorentstehung und das Wachstum verschiedener Tumorzellen, einschließlich Melanom C8161, Ovarialkarzinom Hey1B, Lungenkrebs A549, Glioblastom U373 und Ösophaguskarzinom OE21. Lycorine kann die Proteinsynthese in eukaryotischen Zellen und die Acetylcholinesterase-Aktivität hemmen.
|
|---|---|
| In vivo |
Lycorine zeigt seine zahlreichen pharmakologischen Wirkungen bei verschiedenen Krankheiten mit sehr geringer Toxizität und milden Nebenwirkungen. In In-vivo-Studien hemmt Lycorine das Tumorwachstum in mehreren Maus-Xenograft-Modellen wirksam. Es hemmt effektiv die Tumor-Neovaskularisierung. Lycorine hat eine geringe Toxizität für normale Zellen und normale Körper. Die tiertoxikologischen Experimente zeigen, dass die 50%ige letale Dosis (LD50) von Lycorine bei Mäusen 112,2 ± 0,024 mg/kg bei intraperitonealer Injektion beträgt. Die LD50 von Lycorine bei Mäusen beträgt 344 mg/kg bei Magenspülungs-Injektion, was darauf hindeutet, dass Lycorine bei gastrointestinaler Verabreichung eine sehr geringe Toxizität aufweist. In-vivo-Studien zeigen, dass Lycorine eine lineare Plasmakinetik mit einer mittleren Eliminationshalbwertszeit von 0,67 bzw. 0,3 h nach einmaliger s.c.- und i.v.-Verabreichung aufweist. Die mittlere orale Bioverfügbarkeit wird auf etwa 40% geschätzt. Biochemische und hämatologische Parameter von Sicherheitsstudien zeigen keine pathologischen Anzeichen.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
