nur für Forschungszwecke
SUN11602 FGFR Aktivator
Kat.-Nr.S8192
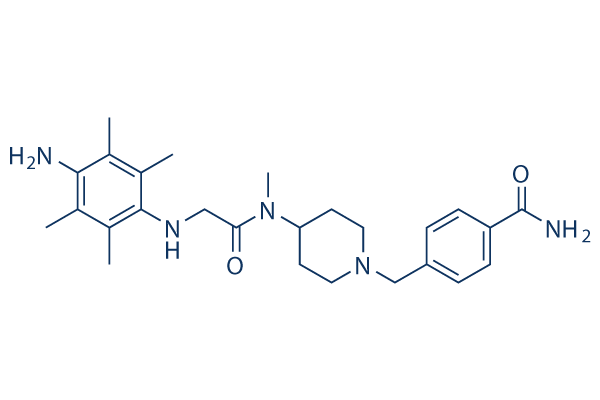
Chemische Struktur
Molekulargewicht: 451.60
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- SDS
- Datenblatt
| Verwandte Ziele | EGFR VEGFR JAK PDGFR Src HIF FLT FLT3 HER2 Bcr-Abl |
|---|---|
| Weitere FGFR Inhibitoren | PD173074 AZD4547 (Fexagratinib) BLU9931 Futibatinib (TAS-120) LY2874455 PD-166866 Zoligratinib (Debio-1347) H3B-6527 Fisogatinib (BLU-554) SSR128129E |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 451.60 | Formel | C26H37N5O2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 704869-38-5 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC1=C(C(=C(C(=C1N)C)C)NCC(=O)N(C)C2CCN(CC2)CC3=CC=C(C=C3)C(=O)N)C | ||
Löslichkeit
|
In vitro |
DMSO
: 90 mg/mL
(199.29 mM)
Ethanol : 31 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
bFGF
|
|---|---|
| In vitro |
Die physiologischen Wirkungen von SUN11602 ahmen verschiedene Phänomene des durch bFGF induzierten Neuroschutzes nach. Diese Verbindung spielt eine entscheidende Rolle dabei, primär kultivierten Neuronen das Überleben in widrigen Umgebungen von Glutamat-Toxizität zu ermöglichen und intrazelluläre Schlüsselmoleküle zu aktivieren, die an den neuroprotektiven Mechanismen beteiligt sind. Diese Wirkungen sind denen von bFGF sehr ähnlich. Solche neuroprotektiven Mechanismen sind spezifisch und charakteristisch für diese Verbindung und bFGF und unterscheiden sich deutlich von denen der anderen untersuchten Wachstumsfaktoren. Aber im Gegensatz zu bFGF kann es die Phosphorylierung der zytosolischen Domäne des FGFR direkt oder indirekt auslösen, ohne an die extrazelluläre Domäne des FGFR-1 zu binden. Diese Chemikalie zeigt im Gegensatz zu bFGF keine zellproliferative Aktivität somatischer Zellen. Sie beeinflusst die neuronale Überlebensfähigkeit unter widrigen Bedingungen signifikant über einen FGFR1-Mitogen-aktivierten Proteinkinase/extrazellulären Signal-regulierten Kinase-1/2-Kinase (FGFR-1–MEK/ERK)-Signalweg.
|
| In vivo |
Bei WT-Mäusen erhöhen SUN11602 und bFGF die Spiegel des neu synthetisierten Calb in zerebrokortikalen Neuronen und unterdrücken den Glutamat-induzierten Anstieg von intrazellulärem Ca2+. Diese Ca2+-Einfangfähigkeit von Calb ermöglicht es den Neuronen, schwere toxische Glutamat-Bedingungen zu überleben. Im Gegensatz dazu bleiben die Calb-Spiegel bei Calb-/- Mäusen nach Exposition gegenüber dieser Verbindung oder bFGF unverändert, und aufgrund eines Funktionsverlusts des Gens sind diese Neuronen nicht mehr resistent gegenüber toxischen Glutamat-Bedingungen. Neuroprotektive Aktivitäten dieser Chemikalie und FGF-2 sind auf eine exogen induzierte Hyperexpression von CalB in Hippocampus-Neuronen zurückzuführen. Die pharmakokinetischen Eigenschaften dieser Verbindung scheinen im Hinblick auf die Bioverfügbarkeit (>65%) nach oraler Verabreichung bei Nagetieren (Ratten und Mäusen) und Hunden (Beagles) vielversprechend zu sein.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
