nur für Forschungszwecke
Dubermatinib(TP-0903) Axl Inhibitor
Kat.-Nr.S7846
Chemische Struktur
Molekulargewicht: 516.06
Qualitätskontrolle
| Verwandte Ziele | EGFR VEGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 |
|---|---|
| Weitere Axl Inhibitoren | Bemcentinib (R428) LDC1267 UNC2025 HCl CEP-40783 (RXDX-106) SGI-7079 Tamnorzatinib (ONO-7475) PF-07265807 RU-301 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 516.06 | Formel | C24H30ClN7O2S |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1341200-45-0 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CN1CCN(CC1)CC2=CC=C(C=C2)NC3=NC=C(C(=N3)NC4=CC=CC=C4S(=O)(=O)N(C)C)Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 3 mg/mL
(5.81 mM)
Ethanol : 2 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Axl
(Cell-free assay) 27 nM
|
|---|---|
| In vitro |
In Bauchspeicheldrüsenkrebszellen (PSN-1) zeigt Dubermatinib (TP-0903) eine starke antiproliferative Aktivität mit einer IC50 von 6 M. Es induziert auch einen starken G2/M-Arrest durch potente Hemmung von Aurora A und B. [1] In CLL-B-Zellen von allen Patienten mit CLL verursacht diese Verbindung eine dosisabhängige Induktion massiver Apoptose durch Targeting von phosphoryliertem Axl und überwindet den CLL-BMSC-vermittelten Schutz von CLL-B-Zellen vor Apoptose. |
| Kinase-Assay |
Axl-Kinase-Aktivitätstest
|
|
Testverbindungen werden in Kinase-Reaktionspuffer (50 mM HEPES pH 7,5, 10 mM MgCl2, 1 mM EGTA, 2 mM DTT und 0,01 % v/v Tween-20) auf die gewünschten Konzentrationen verdünnt und kurz mit Axl-Kinase inkubiert. Die verwendete Axl-Kinase ist rekombinante humane Axl-Kinase (katalytische Domäne, Aminosäuren 473-894) mit einem Histidin-Tag. Die Reaktion wird durch Zugabe von ATP und markiertem Poly-GT-Substrat (Poly Glu:Tyr, 4:1 Polymer) initiiert. Die Konzentration der verschiedenen Komponenten im Assay (10 µL Reaktionsvolumen) beträgt: 1 % DMSO, 93 ng/mL Axl-Kinase, 20 µM ATP und 200 nM Poly-GT-Substrat. Nach Zugabe von ATP und Poly-GT-Substrat erfolgt die Inkubation für 60 Minuten bei Raumtemperatur. Die Enzymreaktion wird durch Zugabe von 10 µL Terbium-markiertem Anti-Phosphotyrosin-PY20-Antikörper in EDTA-haltigem Puffer gestoppt. Die Endkonzentration von EDTA und Antikörper nach Zugabe zur Reaktion beträgt 10 mM bzw. 2 nM. Der Terbium-konjugierte Antikörper erzeugt ein zeitaufgelöstes FRET-Signal mit dem Molekül (gebunden an das Poly-GT-Substrat), wenn das Substrat phosphoryliert ist. Nach einer Stunde Inkubation bei Raumtemperatur wird die Fluoreszenz mit einer Anregung von 320 nm und einer dualen Emission von 495 und 520 nm auf einem EnVision-Mikroplattenlesegerät gemessen. Das Signal wird als TR-FRET-Verhältnis (Fluoreszenzintensität bei 520 nm zu 495 nm) ausgedrückt.
|
|
| In vivo |
Im Hippocampus erwachsener Ratten erhöht die intrazerebroventrikuläre Verabreichung von Dubermatinib (TP-0903) (2,5 nM) die Anzahl der neu gebildeten Zellen signifikant und verlängert das Überleben der Hippocampuszellen. Bei Mäusen verhindert diese Verbindung (20 μg/g, i.p.) effektiv GC-induzierte neonatale zerebellare Entwicklungsanomalien. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | p-AKT / AKT / p-SFK / Lyn / Bcl-2 / XIAP / Mcl-1 |
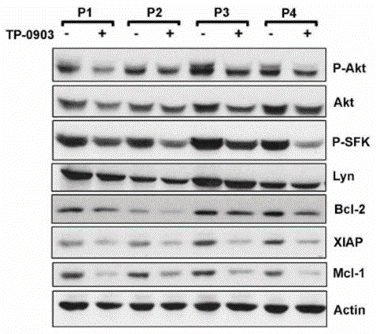
|
25673699 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT04518345 | Completed | Acute Myeloid Leukemia|Secondary Acute Myeloid Leukemia|Therapy-Related Acute Myeloid Leukemia |
Uma Borate|Sumitomo Pharma America Inc.|Ohio State University Comprehensive Cancer Center |
November 5 2020 | Early Phase 1 |
| NCT02729298 | Completed | Advanced Solid Tumors|EGFR Positive Non-small Cell Lung Cancer|Colorectal Carcinoma|Recurrent Ovarian Carcinoma|BRAF-Mutated Melanoma |
Sumitomo Pharma America Inc. |
December 14 2016 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
