nur für Forschungszwecke
AEE788 (NVP-AEE788) EGFR Inhibitor
Kat.-Nr.S1486
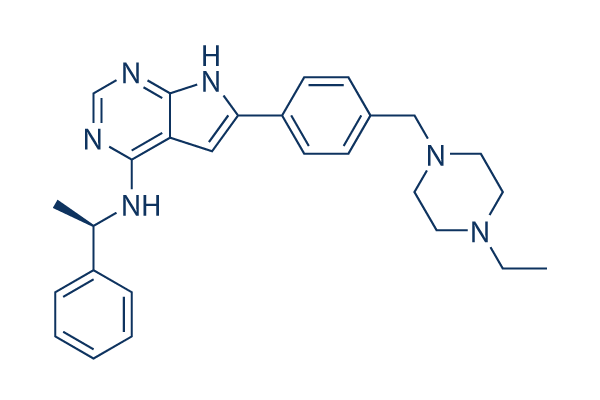
Chemische Struktur
Molekulargewicht: 440.58
Qualitätskontrolle
| Verwandte Ziele | VEGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Weitere EGFR Inhibitoren | Lazertinib (YH25448) Icotinib Hydrochloride Sunvozertinib AG-490 AG-1478 Canertinib (CI-1033) WZ4002 Rociletinib (CO-1686) Poziotinib (NOV120101, HM781-36B) Genistein |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| Huh7 | Cytotoxicity assay | Cytotoxicity against human hepatocellular carcinoma cell line (Huh7), CC50=27.83 Μm | ||||
| Jeko B cells | Function assay | 2 h | Inhibition of PI3Kdelta in human Jeko B cells assessed as inhibition of Akt phosphorylation after 2 hrs, IC50=0.017 μM | |||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 440.58 | Formel | C27H32N6 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 497839-62-0 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CCN1CCN(CC1)CC2=CC=C(C=C2)C3=CC4=C(N3)N=CN=C4NC(C)C5=CC=CC=C5 | ||
Löslichkeit
|
In vitro |
DMSO
: 88 mg/mL
(199.73 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
EGFR
(Cell-free assay) 2 nM
HER2/ErbB2
(Cell-free assay) 6 nM
c-Abl
(Cell-free assay) 52 nM
FLT1
(Cell-free assay) 59 nM
c-Fms
(Cell-free assay) 60 nM
c-Src
(Cell-free assay) 61 nM
KDR
(Cell-free assay) 77 nM
HER4/ErbB4
(Cell-free assay) 160 nM
|
|---|---|
| In vitro |
AEE788 (NVP-AEE788) hemmt auch KDR, c-abl, c-Src und Flt-1 mit einer IC50 von 50-80 nM. Es ist nicht empfindlich gegenüber ErbB-4, PDGFR-β, Flt-3, Flt-4, RET und c-Kit und hat keine hemmende Wirkung auf Ins-R, IGF-1R, PKC-α und PKA. Diese Verbindung hemmt potent die EGFR-Phosphorylierung in A431-Zellen mit einer IC50 von 11 nM. Es hemmt auch die Phosphorylierung von KDR in CHO-Zellen und erbB2 in BT-474-Zellen, ohne Auswirkungen auf die PDGF-induzierte Phosphorylierung in A31-Zellen. Es hemmt die Proliferation von NCI-H596-, MK-, BT-474- und SK-BR-3-Zellen mit einer IC50 von 78, 56, 49 bzw. 381 nM. Darüber hinaus besitzt es die zusätzliche Eigenschaft, die durch EGFR-Mutanten, einschließlich 32D/EGFR und 32D/EGFRvIII, verursachte Zellproliferation zu hemmen. Es hemmt weiterhin sowohl die EGF- als auch die VEGF-induzierte HUVEC-Proliferation mit einer IC50 von 43 bzw. 155 nM. Es hemmt die Phosphorylierung von EGFR, VEGFR2, Akt und MAPK in humanen kutanen SCC-Zelllinien (Colo16-, HaCaT-, SRB1- und SRB12-Zellen), was zu Wachstumshemmung und Apoptose-Induktion führt. Es hemmt die Phosphorylierung von EGFR und Akt in HT29-Zellen bei 0,2 bis 1,0 μM. Es hemmt die Zellproliferation und verhindert die EGF- und Neuregulin-induzierte HER1-, HER2- und HER3-Aktivierung in Medulloblastom-Zelllinien. Es zeigt wachstumsunterdrückende Aktivitäten in chemosensiblen und chemoresistenten Medulloblastom-Zellen.
|
| Kinase-Assay |
Protein Kinase Assays
|
|
Die In-vitro-Kinase-Assays für AEE788 (NVP-AEE788) werden in 96-Well-Platten (30 μL) bei Raumtemperatur für 15–45 min unter Verwendung der rekombinanten Glutathion-S-Transferase-fusionierten Kinasedomänen (4-100 ng, je nach spezifischer Aktivität) durchgeführt. [γ33P]ATP wird als Phosphatdonor und PolyGluTyr-(4:1)-Peptid als Akzeptor verwendet. Mit Ausnahme der Protein Kinase C-α, Cyclin-dependent Kinase 1/cycB und Protein Kinase A werden Protaminsulfat (200 μg/mL), Histon H1 (100 μg/mL) und das Heptapeptid Leu-Arg-Arg-Ala-Ser-Leu-Gly (bekannt als Kemptid Bachem) jeweils als Peptidsubstrate verwendet. Die Assays werden für jede Kinase unter Verwendung der folgenden ATP-Konzentrationen optimiert: 1,0 μM (c-Kit, c-Met, c-Fms, c-Raf-1 und RET), 2,0 μM (EGFR, erbB2, ErbB3 und ErbB4), 5,0 μM (c-abl), 8,0 μM (Flt-1, Flt-3, Flt-4, Flk, KDR, FGFR-1 und Tek), 10,0 μM (PDGFR-β, Protein Kinase C-α und Cyclin-dependent Kinase 1) und 20,0 μM (c-Src und Protein Kinase A). Die Reaktion wird durch Zugabe von 20 μL 125 mM EDTA beendet. Dreißig μL (c-abl, c-Src, Insulin-like Growth Factor-1R, RET-Men2A und RET-Men2B) oder 40 μL (alle anderen Kinasen) des Reaktionsgemisches werden auf eine Immobilon-Polyvinylidenfluoridmembran übertragen, die mit 0,5 % H3PO4 vorgetränkt und auf ein Vakuum-Manifold montiert ist. Anschließend wird Vakuum angelegt und jede Vertiefung mit 200 μL 0,5 % H3PO4 gespült. Die Membranen werden entfernt und viermal mit 1,0 % H3PO4 und einmal mit Ethanol gewaschen. Getrocknete Membranen werden nach dem Einsetzen in einen Packard TopCount 96-Well-Rahmen und der Zugabe von 10 μL/Well Microscint gezählt. IC50-Werte (±SE) werden durch lineare Regressionsanalyse des prozentualen Hemmungsgrades berechnet und sind Mittelwerte von mindestens drei Bestimmungen.
|
|
| In vivo |
AEE788 (NVP-AEE788) bewirkt eine dosisabhängige Hemmung des Tumorwachstums in NCI-H596- oder DU145-Xenograft-Modellen, mit nur geringfügigen Veränderungen des Körpergewichts. Es induziert eine Tumorregression um 57 % bei 50 mg/kg im NeuT/erbB2 GeMag-Modell und hemmt potent die EGF-induzierte EGFR-Phosphorylierung in A431-Tumoren und die erbB2-Phosphorylierung in GeMag-Tumoren. Diese Verbindung hemmte dosisabhängig die durch VEGF induzierte Angiogenese und hemmt nicht die durch bFGF induzierte Angiogenese. Es unterdrückt das Wachstum des Tumorvolumens um 54 % in Colo16-Xenografts bei 50 mg/kg, was auf die Hemmung der Phosphorylierung von EGFR, VEGFR, Akt und MAPK zurückzuführen ist. Bei 50 mg/kg hemmt es auch das Wachstum von Tumoren im Blinddarm und Peritoneum (>50 %) und reduziert die Inzidenz von Lymphknotenmetastasen auf 70 % in HT29-Zellen, die in den Blinddarm von Nacktmäusen implantiert wurden, ohne Verlust des Körpergewichts und grobe Anzeichen von Neovaskularisation. Es senkt signifikant die Expressionsniveaus von pEGFR und pVEGFR in HT29-Blinddarmtumoren und verändert nicht die von EGF, VEGF, EGFR oder VEGFR. In Kombination mit CPT-11 führt es zu signifikant kleineren Tumoren und einer vollständigen Hemmung der Lymphknotenmetastasierung. Diese Verbindung hemmt das Wachstum von Daoy-, DaoyPt- und DaoyHER2-Xenografts um 51 %, 45 % bzw. 72 %. Es könnte die LBH589-vermittelte Produktion reaktiver Sauerstoffspezies in K562-Tumorzellen fördern, was wiederum die Apoptose erhöht.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT00107237 | Completed | Brain and Central Nervous System Tumors |
Novartis Pharmaceuticals|Novartis |
October 2003 | Phase 1|Phase 2 |
| NCT00118456 | Completed | Cancer |
Novartis Pharmaceuticals|Novartis |
July 2003 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
