nur für Forschungszwecke
AZD8330 MEK Inhibitor
Kat.-Nr.S2134
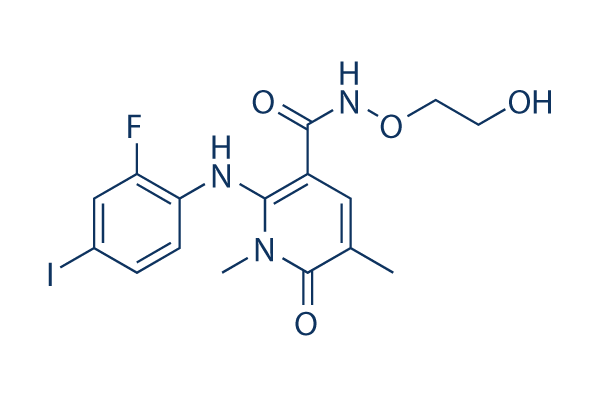
Chemische Struktur
Molekulargewicht: 461.23
Qualitätskontrolle
| Verwandte Ziele | ERK p38 MAPK Raf JNK Ras KRas S6 Kinase MAP4K TAK1 Mixed Lineage Kinase |
|---|---|
| Weitere MEK Inhibitoren | PD0325901 (Mirdametinib) U0126-EtOH PD 98059 PD184352 (CI-1040) BIX 02189 Pimasertib (AS-703026) Refametinib (RDEA119) TAK-733 SL-327 BIX 02188 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 461.23 | Formel | C16H17FIN3O4 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 869357-68-6 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | ARRY704 | Smiles | CC1=CC(=C(N(C1=O)C)NC2=C(C=C(C=C2)I)F)C(=O)NOCCO | ||
Löslichkeit
|
In vitro |
DMSO
: 92 mg/mL
(199.46 mM)
Ethanol : 92 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
ERK phosphorylation
0.4 nM
MEK1/2
7 nM
|
|---|---|
| In vitro |
AZD8330 hemmt MEK 1/2 potent und stark. Diese Verbindung hat keine hemmende Aktivität gegenüber über 200 anderen Kinasen, selbst bei Konzentrationen bis zu 10 μM. Sie zeigt eine sub-nanomolare Potenz in mechanistischen (pERK) und eine niedrige bis sub-nanomolare Potenz in funktionellen (Proliferation) Assays in MEK 1/2-Inhibitor-empfindlichen Zelllinien.
|
| Kinase-Assay |
MEK1 enzymatische Assays
|
|
NH2-terminal mit Hexahistidin markiertes, konstitutiv aktives MEK1 (S218D, S222D ΔR4F) wird in Baculovirus-infizierten Hi5-Insektenzellen exprimiert und mittels immobilisierter Metallaffinitätschromatographie, Ionenaustausch und Gelfiltration gereinigt. Die Aktivität von MEK1 wird durch Messung der Inkorporation von [γ- 33P]phosphat aus [γ-33P]ATP auf ERK2 bestimmt. Der Assay wird in einer 96-Well-Polypropylenplatte mit einer Inkubationsmischung (100 μL) durchgeführt, die aus 25 mM HEPES (pH 7,4), 10 mM MgCl2, 5 mM β-Glycerophosphat, 100 μM Natriumorthovanadat, 5 mM DTT, 5 nM MEK1, 1 μM ERK2 und 0 bis 80 nM AZD8330 (Endkonzentration von 1% DMSO) besteht. Die Reaktionen werden durch Zugabe von 10 μM ATP (mit 0,5 μC k[γ-33P]ATP/Well) gestartet und bei Raumtemperatur 45 min inkubiert. Ein gleiches Volumen von 25% Trichloressigsäure wird hinzugefügt, um die Reaktion zu stoppen und die Proteine zu präzipitieren. Präzipitierte Proteine werden auf Glasfaser-B-Filterplatten gesammelt, überschüssiges markiertes ATP wird mit 0,5%iger Phosphorsäure abgewaschen, und die Radioaktivität wird in einem Flüssigszintillationszähler gemessen. Die ATP-Abhängigkeit wird durch Variieren der ATP-Menge in der Reaktionsmischung bestimmt. Die Daten werden global gefittet.
|
|
| In vivo |
In einem Calu-6-Ratten-Xenograft-Pharmakokinetik/Pharmakodynamik (PK/PD)-Modell hemmt eine einzelne orale Dosis von 1,25 mg/kg AZD8330 die ERK-Phosphorylierung um > 90% für 4 bis 8 Stunden. Dosen von nur 0,4 mg/kg einmal täglich reichen aus, um eine Tumorzellwachstumshemmung von > 80% im Calu-6 Nacktratten-Xenograft-Modell zu erreichen. Im Calu-6-Modell hemmt diese Verbindung das Tumorwachstum dosisabhängig bei 0,3 mg/kg und 1,0 mg/kg einmal täglich.
|
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | pERK / ERK / Myc / RPIA |
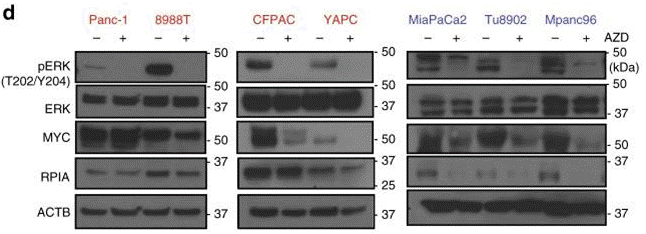
|
30470748 |
| Growth inhibition assay | IC50 |
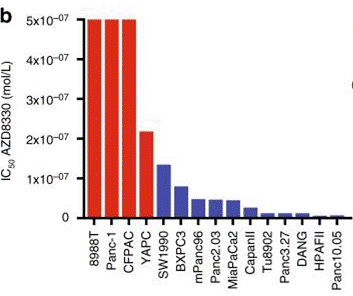
|
30470748 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT00454090 | Completed | Cancer |
AstraZeneca |
March 2007 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
