nur für Forschungszwecke
Mycophenolate mofetil Dehydrogenase Inhibitor
Kat.-Nr.S1501
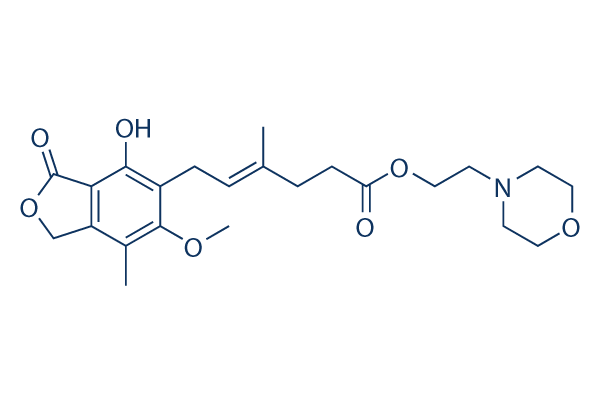
Chemische Struktur
Molekulargewicht: 433.49
Qualitätskontrolle
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 433.49 | Formel | C23H31NO7 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 128794-94-5 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | Mycophenolic acid morpholinoethyl ester, CellCept, RS-61443, TM-MMF | Smiles | CC1=C2COC(=O)C2=C(C(=C1OC)CC=C(C)CCC(=O)OCCN3CCOCC3)O | ||
Löslichkeit
|
In vitro |
DMSO
: 87 mg/mL
(200.69 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Inosine monophosphate dehydrogenase II
(Cell-free assay) 27 nM
Inosine monophosphate dehydrogenase I
(Cell-free assay) 39 nM
|
|---|---|
| In vitro |
Mycophenolate mofetil ist ein Ester-Prodrug des aktiven Immunsuppressivums Mycophenolsäure (MPA). Letztere zeigt eine nicht-kompetitive, selektive und reversible Hemmaktivität gegen inosine monophosphate dehydrogenase Typ I/II mit IC50 von 39 nM bzw. 27 nM. Darüber hinaus bewirkt MPA auch eine konzentrationsabhängige Hemmung der Proliferation von ConA-stimulierten T-Zellen, LPS-stimulierten B-Zellen und Alloantigen-spezifischen T-Zellen mit IC50 von 100 nM, 120 nM bzw. 51 nM. Diese Verbindung in hoher Konzentration von 10 μg/mL induziert eine starke Apoptose in Mikrogliazellkulturen und erhöht die Anzahl aktivierter Caspase-3-immunreaktiver apoptotischer Zellen. Darüber hinaus hemmt sie (1 μg/mL) stark die Proliferation sowohl von Mikrogliazellen als auch von Astrozyten. Eine aktuelle Studie zeigt, dass diese Chemikalie das Ausmaß des neuronalen Zelltods von organotypischen Hippocampus-Schnittkulturen nach neuronaler Verletzung zeitabhängig signifikant abschwächt. |
| Kinase-Assay |
IMP dehydrogenase Typen I und II enzymatische Aktivität
|
|
IMP dehydrogenase Typen I und II werden aus E. coli, die menschliche Enzyme exprimieren, gereinigt. Der Assay wird in einer flachen, UV-transparenten 96-Well-Platte durchgeführt. Die endgültige 200 μL Reaktionsmischung enthielt 0,1 M Tris, 0,1 M KCl, 3 mM EDTA pH 8,0, 2 mM DTT und 40 nM entweder IMP dehydrogenase Typ I oder Typ II. Die Reaktion wird durch Zugabe von 400 μM NAD und 400 μM IMP initiiert, gefolgt von einer Inkubation bei 37 °C für 2,5 Stunden. Die Reaktionsrate der Umwandlung von NAD zu NADH wird dann basierend auf dem Anstieg der Absorption bei 340 nm gemessen. Die Assays werden auch in Gegenwart von 50 % menschlichem Serum durchgeführt, um die Serumproteinbindung durch verschiedene IMP dehydrogenase Inhibitoren abzuschätzen.
|
|
| In vivo |
In einem heterotopen kardialen Transplantationsmodell von ACI-zu-Lewis-Ratten führt die Behandlung mit Mycophenolate mofetil in Dosen von 20 mg/kg und 40 mg/kg zu einer Verlängerung des Transplantatüberlebens mit einer mittleren Überlebenszeit (MST) von 14,5 Tagen bzw. 18,5 Tagen. In einem Bleomycin (BLM)-induzierten Sklerodermie-Mausmodell reduziert diese Verbindung die Infiltration von Entzündungszellen, den Gewebe-Hydroxyprolingehalt und die Hautdicke. |
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT05702931 | Not yet recruiting | Hyperglycemia|Renal Transplant Complication Primary Non-Function|Diabetes |
Rigshospitalet Denmark|Aarhus University Hospital|Odense University Hospital |
April 1 2024 | Phase 4 |
| NCT05859191 | Recruiting | Systemic Lupus Erythematosus|Physiopathology |
University Hospital Tours|Research Center for Respiratory Diseases Inserm U1100 |
July 21 2023 | -- |
| NCT05120570 | Recruiting | Acute Leukemia|Myelodysplastic Syndromes|Myeloproliferative Neoplasm|Lymphoma |
Masonic Cancer Center University of Minnesota |
March 17 2022 | Phase 1|Phase 2 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
