nur für Forschungszwecke
Sodium Dichloroacetate (DCA) PDK-Inhibitor
Kat.-Nr.S8615
Chemische Struktur
Molekulargewicht: 150.92
Qualitätskontrolle
| Verwandte Ziele | HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism Drug Metabolite |
|---|---|
| Weitere Dehydrogenase Inhibitoren | Vorasidenib (AG-881) (R)-GNE-140 CPI-613 (Devimistat) Glycyrrhizin (Glycyrrhizic Acid, NSC 167409) AGI-5198 Gossypol Acetate AGI-6780 Emodin NCT-503 Brequinar |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| MCF7 | Function assay | 10 mM | 12 hrs | Inhibition of PDK1 in human MCF7 cells assessed as increase in oxygen consumption rate at 10 mM after 12 hrs | 27006991 | |
| MCF7 | Function assay | 10 mM | 12 hrs | Inhibition of PDK1 in human MCF7 cells assessed as decrease in extracellular acidification rate at 10 mM after 12 hrs | 27006991 | |
| MCF7 | Function assay | 10 mM | 12 hrs | Inhibition of PDK1 in human MCF7 cells assessed as decrease in proton production rate at 10 mM after 12 hrs | 27006991 | |
| MCF7 | Function assay | 10 mM | 12 hrs | Inhibition of PDK1 in human MCF7 cells assessed as increase in ratio of oxygen consumption rate to extracellular acidification rate at 10 mM after 12 hrs | 27006991 | |
| MCF7 | Function assay | 10 mM | 12 hrs | Inhibition of PDK1 in human MCF7 cells assessed as decrease in lactate production at 10 mM after 12 hrs | 27006991 | |
| NCI-H1975 | Antiproliferative assay | 20 mM | 72 hrs | Antiproliferative activity against human NCI-H1975 cells assessed as reduction in cell viability at 20 mM after 72 hrs by MTT assay | 30470491 | |
| MCF7 | Function assay | 90 mins | Inhibition of PDK1 (unknown origin) expressed in human MCF7 cells using PDK tide as substrate measured after 90 mins in presence of ATP by ADP-Glo luminescent kinase assay | 31509699 | ||
| MCF7 | Antitumor assay | 30 mg/kg | two weeks | Antitumor activity against human MCF7 cells xenografted in BALB/c nude mouse assessed as tumor growth inhibition at 30 mg/kg, iv administered every two days for two weeks measured after 14 days | 31509699 | |
| MCF7 | Function assay | 30 uM | 4 hrs | Induction of metabolic reversal from aerobic glycolysis to oxidative phosphorylation in human MCF7 cells assessed as increase in extracellular acidification rate at 30 uM pretreated for 4 hrs followed by glucose addition after 25 mins by seahorse XF24 ext | 31509699 | |
| MCF7 | Function assay | 30 uM | 4 hrs | Induction of metabolic reversal from aerobic glycolysis to oxidative phosphorylation in human MCF7 cells assessed as increase in extracellular acidification rate at 30 uM pretreated for 4 hrs followed by glucose addition after 25 mins followed by subsequent assay | 31509699 | |
| MCF7 | Function assay | 30 uM | 4 hrs | Induction of metabolic reversal from aerobic glycolysis to oxidative phosphorylation in human MCF7 cells assessed as decline in extracellular acidification rate at 30 uM pretreated for 4 hrs followed by glucose addition after 25 mins followed by subsequent assay | 31509699 | |
| MCF7 | Function assay | 30 uM | 6 hrs | Induction of metabolic reversal from aerobic glycolysis to oxidative phosphorylation in human MCF7 cells assessed as decrease in oxygen consumption rate at 30 uM pretreated for 6 hrs followed by oligomycin A addition after 25 mins followed by subsequent assay | 31509699 | |
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 150.92 | Formel | C2HCl2O2.Na |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 2156-56-1 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | Dichloroacetic acid, bichloroacetic acid, BCA | Smiles | C(C(=O)[O-])(Cl)Cl.[Na+] | ||
Löslichkeit
|
In vitro |
|
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
PDK4
(Cell-free assay) 80 μM
PDK2
(Cell-free assay) 183 μM
|
|---|---|
| In vitro |
Sodium Dichloroacetate (DCA) kann die Apoptose von menschlichen Lungen-, Brust- und Hirnkrebszellen auslösen. Nach der Behandlung mit dieser Verbindung zeigen Krebszellen erhöhte ROS-Spiegel, Depolarisation des MMP in vitro und erhöhte Apoptose sowohl in vitro als auch in vivo. Es hemmt die Aktivität der Pyruvat-Dehydrogenase-Kinase (PDK) und stimuliert dadurch das mitochondriale Enzym Pyruvat-Dehydrogenase (PDH). Wenn ausgeschaltet, wandelt PDH Pyruvat nicht mehr in Acetyl-CoA um, das für die mitochondriale Atmung und die glucoseabhängige oxidative Phosphorylierung erforderlich ist. DCA verschiebt somit den zellulären Metabolism von Glykolyse zur Glucoseoxidation, wodurch der mitochondriale Membranpotentialgradient verringert und die Öffnung mitochondrialer Übergangsporen unterstützt wird. Dieser metabolische Schalter erleichtert die Translokation pro-apoptotischer Mediatoren wie Cytochrom c (cyt c) und Apoptosis Inducing Factor (AIF), die beide die Apoptose stimulieren. Dadurch treibt es Krebszellen dazu, durch Apoptose Selbstmord zu begehen.
|
| In vivo |
Sodium Dichloroacetate (DCA) kann in vitro und in vivo als zytostatisches Mittel wirken, ohne Apoptosis (programmierten Zelltod) zu verursachen. Es wurde als sicheres Medikament ohne Herz-, Lungen-, Nieren- oder Knochenmarktoxizität entdeckt. Die schwerwiegendste häufige Nebenwirkung ist periphere Neuropathie, die reversibel ist. Diese Verbindung hat eine Antikrebsaktivität bei verschiedenen Krebsarten, einschließlich Darm-, Prostata-, Eierstock-, Neuroblastom-, Lungenkarzinoid-, Gebärmutterhals-, Endometrium-, Cholangiokarzinom-, Sarkom- und T-Zell-Lymphom. Andere antineoplastische Wirkungen wurden ebenfalls vorgeschlagen. Dazu gehören Angiogenese-Blockade, Änderungen in der Expression von HIF1-α, Veränderung der pH-Regulatoren V-ATPase und MCT1 sowie anderer Zellüberlebensregulatoren wie PUMA, GLUT1, Bcl2 und p53. Es ist in der Lage, die metastatische Belastung in den Lungen von Ratten in einem hochmetastatischen In-vivo-Modell von Brustkrebs signifikant zu reduzieren. In vivo induziert die DCA-Na-Behandlung eine 20%ige Überlebensrate und verringerte den Tumordurchmesser, das Volumen und das Gewicht, ohne das Körpergewicht zu beeinflussen und Metastasen bei C57BL/6-Mäusen zu vermeiden.
|
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | pPDH E1α / PDH E1α |
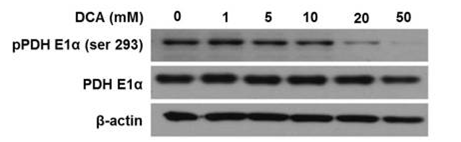
|
25630799 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT06073106 | Not yet recruiting | Stroke|Traumatic Brain Injury|Knee Osteoarthritis|Breast Cancer |
Tan Tock Seng Hospital|Rehabilitation Research Institute of Singapore (RRIS)|Woodlands Health (WH) |
December 2023 | -- |
| NCT05810623 | Not yet recruiting | Upper Urinary Tract Urothelial Carcinoma|Bladder Cancer |
David D''Andrea|Medical University of Vienna |
June 1 2023 | Phase 3 |
| NCT05646485 | Recruiting | Bladder Cancer|Urothelial Carcinoma|Hematuria|Smoking Cessation |
University of Texas Southwestern Medical Center |
May 5 2023 | Not Applicable |
| NCT05460533 | Recruiting | B-cell Acute Lymphoblastic Leukemia |
Memorial Sloan Kettering Cancer Center|Novartis Pharmaceuticals |
July 12 2022 | Phase 2 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
