nur für Forschungszwecke
WZ3146 EGFR Inhibitor
Kat.-Nr.S1170
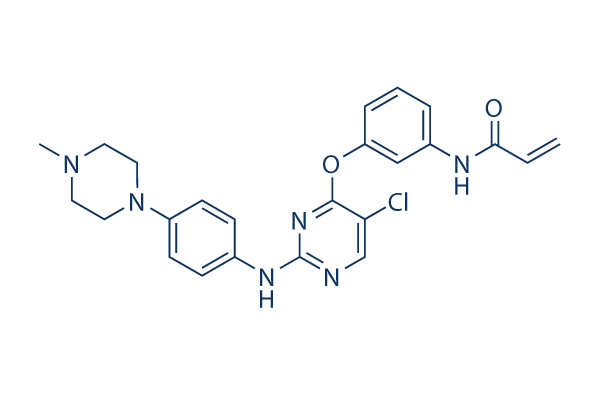
Chemische Struktur
Molekulargewicht: 464.95
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- SDS
- Datenblatt
| Verwandte Ziele | VEGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Weitere EGFR Inhibitoren | Lazertinib (YH25448) Icotinib Hydrochloride Sunvozertinib AG-490 AG-1478 Canertinib (CI-1033) WZ4002 Rociletinib (CO-1686) Poziotinib (NOV120101, HM781-36B) Genistein |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 464.95 | Formel | C24H25ClN6O2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1214265-56-1 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CN1CCN(CC1)C2=CC=C(C=C2)NC3=NC=C(C(=N3)OC4=CC=CC(=C4)NC(=O)C=C)Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 93 mg/mL
(200.02 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
Mutant-selective, irreversible.
|
|---|---|
| Targets/IC50/Ki |
EGFR (L858R)
2 nM
EGFR (E746_A750)
2 nM
EGFR (L858R/T790M)
5 nM
EGFR (E746_A750/T790M)
14 nM
|
| In vitro |
WZ3146 unterdrückt signifikant das Wachstum von EGFR-Mutations-enthaltenden Zelllinien mit einer IC50 von 3 nM in EGFR Del E746_A750-enthaltenden HCC827-Zellen, 15 nM in EGFR Del E746_A750-enthaltenden PC9-Zellen, 29 nM in EGFR L858R/T790M-enthaltenden H1975-Zellen und 3 nM in EGFR Del E746_A750/T790M-enthaltenden PC9 GR-Zellen.
|
| Kinase-Assay |
In-vitro-hemmende enzymkinetische Assays
|
|
Die Assays werden in Dreifachbestimmung unter Verwendung des ATP/NADH-gekoppelten Assay-Systems in einem 96-Well-Format durchgeführt. Die endgültige Reaktionsmischung enthält 0,5 mg/mL Rinderserumalbumin (BSA), 2 mM MnCl2, 1 mM Phospho(enol)brenztraubensäure (PEP), 1 mM TCEP, 0,1 M Hepes 7,4, 2,5 mM Poly-[Glu4Tyr1]-Peptid, 1/50 des Endreaktionsvolumens an Pyruvatkinase/Laktatdehydrogenase-Enzymen aus Kaninchenmuskel, 0,5 mM NADH, 0,5 μM EGFR-Kinase, 100 μM ATP und variierende Mengen von WZ3146. Diese Verbindung und ATP werden gemischt und getrennte Stammlösungen von der Mischung mit allen anderen Bestandteilen hergestellt und zuletzt zu letzterer hinzugefügt, um die Reaktion zu starten. Daten zur anfänglichen Geschwindigkeit im stationären Zustand werden aus den Steigungen der A340-Kurven gewonnen.
|
Literatur |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
