nur für Forschungszwecke
GW9662 PPARγ Antagonist
Kat.-Nr.S2915
Chemische Struktur
Molekulargewicht: 276.68
Qualitätskontrolle
| Verwandte Ziele | HDAC PARP ATM/ATR DNA-PK WRN DNA/RNA Synthesis Topoisomerase Sirtuin Casein Kinase eIF |
|---|---|
| Weitere PPAR Inhibitoren | T0070907 GW6471 WY-14643 (Pirinixic Acid) GSK3787 GW0742 AZ6102 Harmine Astaxanthin Eupatilin GSK0660 |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| 293H | Function assay | 30 mins | Antagonist activity at human PPARgamma expressed in 293H cells assessed as reduction in transcriptional response preincubated for 30 mins followed by addition and measured after 16 hrs by reporter gene-based FRET assay, EC50=0.002μM | 31294974 | ||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 276.68 | Formel | C13H9ClN2O3 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 22978-25-2 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | C1=CC=C(C=C1)NC(=O)C2=C(C=CC(=C2)[N+](=O)[O-])Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 55 mg/mL
(198.78 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
PPARγ
(Cell-free assay) 3.3 nM
PPARα
(Cell-free assay) 32 nM
|
|---|---|
| In vitro |
GW9662 bindet an Cys(285) auf PPARgamma, das unter allen drei PPARs konserviert ist. Diese Verbindung wirkt als Antagonist von PPARgamma, was in einem Assay zur Hemmung der Adipozytendifferenzierung bestätigt wird. Es verhindert die Aktivierung von PPARγ und hemmt das Wachstum von menschlichen Mammakarzinomzelllinien (MCF7, MDA-MB-468, MDA-MB-231) mit einer IC50 von 20 μM-30 μM, was entweder die Existenz von PPARγ-agonistischen Eigenschaften dieser Chemikalie oder wachstumshemmende Mechanismen, die unabhängig von PPARγ sind, nahelegt. Eine Co-Behandlung mit dieser Verbindung (10 μM) führt nach 7 Tagen in MDA-MB-231-Zellen zu statistisch geringeren Zellzahlen. PPARγ1-Liganden könnten die RANKL-induzierte Osteoklastenbildung in primären murinen myeloischen (BMs) und RAW264.7-Zellen unterdrücken. Wichtig ist, dass die Unterdrückung durch diese Liganden dosisabhängig mit dieser Chemikalie (2 μM) aufgehoben wird. Es (2 μM) blockiert die IL-4-Unterdrückung der Osteoklastenbildung in BMs. Diese Verbindung (1 μM) blockiert die RANKL-Aktivierung von NF-κB in RAW264.7-Zellen. GW9662 (10 μM) hemmt die Hormon- und Agonist-induzierte Adipogenese von primären Präadipozyten von Patienten mit Schilddrüsenaugenerkrankung. |
| Kinase-Assay |
Bindungsassay
|
|
Die humanen PPARα-, PPARγ- und PPARδ-Ligandenbindungsdomänen (LBDs) werden in E. coli als polyhistidin-markierte Fusionsproteine exprimiert. Rezeptoren werden durch Zugabe des gewünschten Rezeptors (15 nM) zu einer Suspension von Streptavidin-modifizierten SPA-Beads (0,5 mg/mL) in Assay-Puffer auf SPA-Beads immobilisiert. Die Mischung wird mindestens 1 Stunde bei Raumtemperatur äquilibrieren gelassen, und die Beads werden durch Zentrifugation bei 1×103 g pelletiert. Der Überstand wird verworfen, und die Beads werden im ursprünglichen Volumen frischen Assay-Puffers unter sanftem Mischen resuspendiert. Das Zentrifugations-/Resuspensionsverfahren wird wiederholt, und die resultierende Suspension von Rezeptor-beschichteten Beads wird sofort verwendet oder bei 4 ℃ für bis zu 1 Woche vor Gebrauch gelagert. [3H]GW2443 werden als Radioliganden zur Bestimmung der Kompetitionbindung an PPARα, PPARγ bzw. PPARδ verwendet. Sofern nicht anders angegeben, ist der für alle Assays verwendete Puffer 50 mM HEPES (pH 7), 50 mM NaCl, 5 mM CHAPS, 0,1 mg/mL BSA und 10 mM DTT. Für einige Experimente wird das HEPES (pH 7) durch 50 mM Tris (pH 8) ersetzt.
|
|
| In vivo |
Eine Vorbehandlung mit LPS (1 mg/kg i.p.) attenuierte signifikant alle Marker für Nierenverletzung und -dysfunktion, die durch Ischämie/Reperfusion (I/R)-Verletzung bei Ratten verursacht wurden. Insbesondere hob diese Verbindung (1 mg/kg i.p.) die schützenden Effekte von LPS auf. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | Vimentin / Slug / MMP9 / MMP2 |
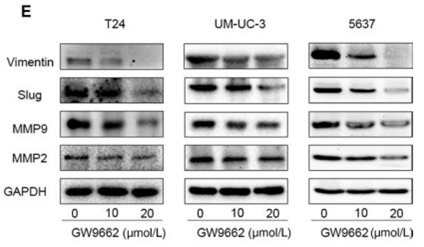
|
30912275 |
| Growth inhibition assay | Cell proliferation |
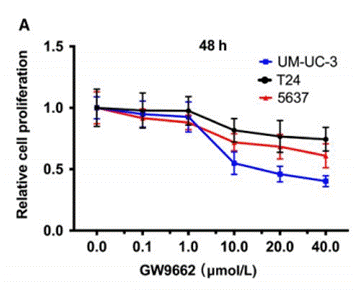
|
30912275 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
