nur für Forschungszwecke
GSK3787 PPAR Antagonist
Kat.-Nr.S8025
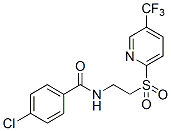
Chemische Struktur
Molekulargewicht: 392.78
Qualitätskontrolle
| Verwandte Ziele | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase Vitamin Carbohydrate Metabolism Mitochondrial Metabolism Drug Metabolite |
|---|---|
| Weitere PPAR Inhibitoren | T0070907 GW9662 GW6471 WY-14643 (Pirinixic Acid) GW0742 AZ6102 Harmine Astaxanthin Eupatilin GSK0660 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 392.78 | Formel | C15H12ClF3N2O3S |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 188591-46-0 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | C1=CC(=CC=C1C(=O)NCCS(=O)(=O)C2=NC=C(C=C2)C(F)(F)F)Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 79 mg/mL
(201.13 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
PPARδ
6.6(pIC50)
|
|---|---|
| In vitro |
GSK3787 antagonisiert irreversibel menschliches und Maus-PPARδ, das kovalent Cys249 innerhalb der Ligandenbindungsstelle modifiziert. Diese Verbindung (1 μM) antagonisiert effektiv die durch den Agonisten GW0742 stimulierte Transkription von CPT1a und PDK4 in menschlichen Skelettmuskelzellen und antagonisiert effektiv die basale Genexpression von CPT1a. Sie zeigt keine wirksame antiproliferative Aktivität gegen Darmkrebszellen. Diese Chemikalie (1 μM) antagonisiert vollständig die durch 50 nM GW0742 induzierte PPARβ/δ-abhängige Angptl4-Genexpression in Wildtyp-Fibroblasten und in Keratinozyten. Sie (1 μM) antagonisiert weitgehend die durch 50 nM GW0742 induzierte Angptl4- und Adrp-mRNA-Expression in Hautkrebszelle A341. Diese Verbindung (1 μM) antagonisiert weitgehend die durch GW0742 induzierte Angptl4-mRNA-Expression in den Krebszelllinien MCF7 (Brust), Huh7 (Leber) und HepG2 (Leber), jedoch nicht in H1838- oder A549-Zellen (Lunge). Sie (1 μM) antagonisiert weitgehend den durch GW0742 induzierten Anstieg der Adrp-mRNA in Huh7- und HepG2-Zellen, jedoch nicht in H1838-Zellen. Diese Chemikalie antagonisiert die basale Expression keiner dieser beiden PPARβ/δ-Zielgene in diesen Zellen. Weder GW0742 noch diese Verbindung haben bei Konzentrationen von 0,1 bis 10 μM eine Wirkung auf die Zellproliferation dieser Zellen. Sie ist in der Lage, die Assoziation von sowohl PPARβ/δ- als auch PPARγ-Koregulatorpeptiden als Reaktion auf die Ligandenaktivierung zu modulieren. Die Wirksamkeit dieser Chemikalie zur Modulation der PPARγ-Aktivität ist deutlich geringer als ihre Wirksamkeit als PPARβ/δ-Antagonist. |
| Kinase-Assay |
Sättigungsbindungsassay
|
|
Unter Verwendung von 96-Well-Kulturplatten werden 50 nM gereinigtes humanes PPARG-LBD und die gewünschte Konzentration von [3H]GW3738 auf ein Gesamtvolumen von 100 μL mit einem Puffer verdünnt, der 50 mM KCl, 5 mM EDTA, 10 mM Dithiothreitol (DTT), 50 mM HEPES bei pH 7 enthält. Sättigungsbindungsassays werden mit Konzentrationen dieser Verbindung im Bereich von 1 bis 250 nM durchgeführt. Die unspezifische Bindung bei jeder Konzentration von [3H]GW3738 wird in parallelen Inkubationen mit 50 μM unmarkiertem GW 3738 geschätzt. Die Platten werden 2 Stunden bei Raumtemperatur inkubiert. Freier Ligand wird durch Größenausschlusschromatographie unter Verwendung handelsüblicher 96-Well-Format-Spinsäulen von Rezeptor-gebundenem Liganden getrennt. Proben (50 μL) aus jeder Vertiefung einer einzelnen Testplatte werden auf einen Puffer- und Temperatur-äquilibrierten 96-Well-Gelfiltrationsblock geladen. Der Block wird auf eine saubere Mikrotiterplatte gestellt und 4 Minuten bei 1100 g zentrifugiert. Szintillationsflüssigkeit (180 μL) wird zu jeder Vertiefung der Platte mit dem Eluenten gegeben, und die Platten werden versiegelt und mindestens 4 Stunden äquilibrieren gelassen, bevor sie in einem Zähler gezählt werden. Die Menge der unspezifischen Bindung bei jeder Konzentration von [3H]GW3738 wird von allen Vertiefungen subtrahiert, und es werden Diagramme der Konzentration dieser Chemikalie gegen gebundene Counts per Minute (cpm) erstellt. Die Kd-Werte für [3H]GW3738 werden aus einer nichtlinearen Kleinste-Quadrate-Anpassung der Daten an ein einfaches Bindungsmodell bestimmt.
|
|
| In vivo |
GSK3787 antagonisiert die Liganden-induzierte PPARβ/δ-abhängige Genexpression in vivo. Die orale Verabreichung dieser Verbindung hat keine Wirkung auf die Expression von Angptl4- und Adrp-mRNA im Mausepithel des Dickdarms. Die Koadministration dieser Chemikalie (10 mg/kg) verhindert effektiv die GW0742-induzierte Expression sowohl von Angptl4- als auch von Adrp-mRNA im Dickdarmepithel von Wildtyp-Mäusen, was mit einer reduzierten Promotorbesetzung von PPARβ/δ an den Angptl4- und Adrp-Genen korreliert ist. Die Verabreichung dieser Verbindung hatte keine Auswirkung auf die Glukosetoleranz. |
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
