nur für Forschungszwecke
LY2510924 CXCR Antagonist
Kat.-Nr.S8505
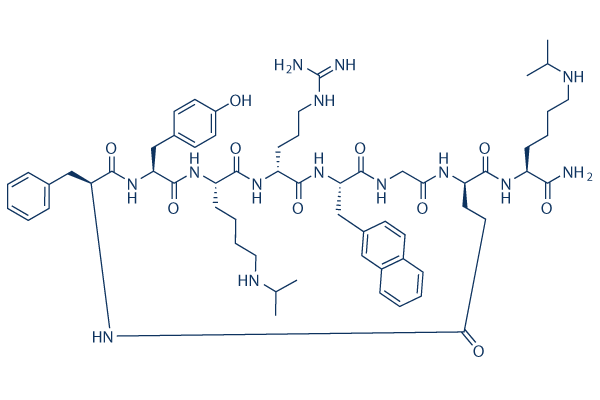
Chemische Struktur
Molekulargewicht: 1189.45
Qualitätskontrolle
| Verwandte Ziele | PD-1/PD-L1 STING AhR Immunology & Inflammation related CD markers Interleukins Anti-infection Antioxidant COX Histamine Receptor |
|---|---|
| Weitere CXCR Inhibitoren | AZD5069 SB 225002 Reparixin (Repertaxin) WZ811 Navarixin (SCH-527123) LIT-927 AMG 487 SX-682 Danirixin (GSK1325756) SB 265610 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 1189.45 | Formel | C62H88N14O10 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1088715-84-7 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC(C)NCCCCC1C(=O)NC(C(=O)NC(C(=O)NCC(=O)NC(CCC(=O)NC(C(=O)NC(C(=O)N1)CC2=CC=C(C=C2)O)CC3=CC=CC=C3)C(=O)NC(CCCCNC(C)C)C(=O)N)CC4=CC5=CC=CC=C5C=C4)CCCN=C(N)N | ||
Löslichkeit
|
In vitro |
Water : 100 mg/mL |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
CXCR4
(Cell-free) 0.079 nM
|
|---|---|
| In vitro |
In menschlichen Lymphom-U937-Zellen, die endogenes CXCR4 exprimieren, hemmt LY2510924 die SDF-1-induzierte Zellmigration mit einem IC50-Wert von 0,26 nmol/L und hemmt die SDF-1/CXCR4-vermittelte intrazelluläre Signalübertragung. Diese Verbindung zeigt eine konzentrationsabhängige Hemmung von SDF-1-stimuliertem Phospho-ERK und Phospho-Akt in Tumorzellen. Biochemische und zelluläre Analysen zeigen, dass es keine offensichtliche Agonistenaktivität besitzt. Es hat keine hemmenden Aktivitäten gegen andere Chemokinrezeptoren, einschließlich CCR1, CCR2, CXCR2 und CXCR3, bei den getesteten Konzentrationen. Ähnlich wurde keine Aktivität bei Serotonin-, Dopamin- und Opioidrezeptoren beobachtet.
|
| In vivo |
LY2510924 weist eine akzeptable In-vivo-Stabilität und ein pharmakokinetisches Profil auf, das dem eines typischen niedermolekularen Inhibitors bei präklinischen Spezies ähnelt. Diese Verbindung zeigt eine dosisabhängige Hemmung des Tumorwachstums in humanen Xenograft-Modellen, die mit Non-Hodgkin-Lymphom-, Nierenzellkarzinom-, Lungen- und Darmkrebszellen, die funktionelles CXCR4 exprimieren, entwickelt wurden. In MDA-MB-231, einem Brustkrebs-Metastasierungsmodell, hemmt es die Tumormetastasierung, indem es den Migrations-/Homing-Prozess von Tumorzellen zur Lunge blockiert und die Zellproliferation nach dem Homing der Tumorzellen hemmt. Diese Chemikalie weist eine dramatisch verbesserte In-vivo-Stabilität mit einer Halbwertszeit von 3 bis 5 Stunden bei präklinischen Spezies und 9,16 Stunden beim Menschen bei der empfohlenen Phase-II-Dosis auf.
|
Literatur |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT02737072 | Terminated | Solid Tumor |
Eli Lilly and Company|AstraZeneca |
September 2016 | Phase 1 |
| NCT02652871 | Completed | Leukemia |
M.D. Anderson Cancer Center|Eli Lilly and Company|High Impact Clinical Research Support Program |
May 9 2016 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
