nur für Forschungszwecke
MEK162 (Binimetinib, ARRY-162) MEK Inhibitor
Kat.-Nr.S7007
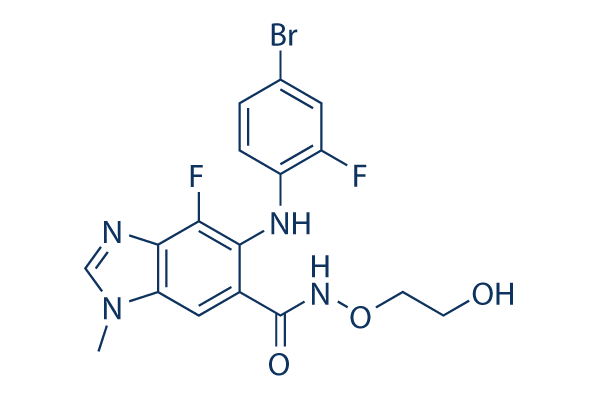
Chemische Struktur
Molekulargewicht: 441.23
Qualitätskontrolle
| Verwandte Ziele | ERK p38 MAPK Raf JNK Ras KRas S6 Kinase MAP4K TAK1 Mixed Lineage Kinase |
|---|---|
| Weitere MEK Inhibitoren | PD0325901 (Mirdametinib) U0126-EtOH PD 98059 PD184352 (CI-1040) BIX 02189 Pimasertib (AS-703026) Refametinib (RDEA119) TAK-733 AZD8330 SL-327 |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| NCI-H727 | Function assay | IC50=115 nM | 30352565 | |||
| Mel IL | Cytotoxicity assay | IC50=3.7 ± 0.2 μM | 30551515 | |||
| Mel IL/R | Cytotoxicity assay | IC50=2.7 ± 0.3 μM | 30551515 | |||
| Mel Z | Cytotoxicity assay | IC50=3.8 ± 0.2 μM | 30551515 | |||
| A375 | Cytotoxicity assay | IC50=9.8 ± 0.1 μM | 30551515 | |||
| Mel Me | Cytotoxicity assay | IC50=13.3 ± 0.3 μM | 30551515 | |||
| Mel MTP | Cytotoxicity assay | IC50=10.2 ± 0.4 μM | 30551515 | |||
| U2OS cells | Function assay | 1 μM | MEK162 blocked ERK activation (p-ERK1/2) in CZ415-treated U2OS cells | 29137241 | ||
| CHP-212 | Cell viability assay | 120 h | IC50=0.0083 μM | 26925841 | ||
| SK-N-AS | Cell viability assay | 120 h | IC50=0.067 μM | 26925841 | ||
| SK-N-BE(2) | Cell viability assay | 120 h | IC50=0.28 μM | 26925841 | ||
| SJ-NB-10 | Cell viability assay | 120 h | IC50=1.16 μM | 26925841 | ||
| CHP-134 | Cell viability assay | 120 h | IC50>15 μM | 26925841 | ||
| Kelly | Cell viability assay | 120 h | IC50>15 μM | 26925841 | ||
| LAN-5 | Cell viability assay | 120 h | IC50>15 μM | 26925841 | ||
| NGP | Cell viability assay | 120 h | IC50>15 μM | 26925841 | ||
| SK-N-DZ | Cell viability assay | 120 h | IC50>15 μM | 26925841 | ||
| A549 | Cell cycle assay | 0, 0.5, 1 μM | 48h | at relatively low concentration ranges ≤ 1 μM (e.g., 0.5 and 1 μM) induced G1 arrest | 25937299 | |
| H157 | Cell cycle assay | 0, 0.5, 1 μM | 48h | at relatively low concentration ranges ≤ 1 μM (e.g., 0.5 and 1 μM) induced G1 arrest | 25937299 | |
| H522 | Cell cycle assay | 0, 0.5, 1 μM | 48h | at relatively low concentration ranges ≤ 1 μM (e.g., 0.5 and 1 μM) induced G1 arrest | 25937299 | |
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 441.23 | Formel | C17H15BrF2N4O3 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 606143-89-9 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | ARRY-162,ARRY-438162 | Smiles | CN1C=NC2=C1C=C(C(=C2F)NC3=C(C=C(C=C3)Br)F)C(=O)NOCCO | ||
Löslichkeit
|
In vitro |
DMSO
: 88 mg/mL
(199.44 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
MEK
(Cell-free assay) 12 nM
|
|---|---|
| In vitro |
Binimetinib (MEK162) ist ein kürzlich entdeckter potenter und selektiver ATP-nicht-kompetitiver MEK1/2-Inhibitor, der pERK in Zellen mit einer IC50 von 11 nM hemmt. Diese Verbindung (625 nM) hemmt die In-vitro-Osteoklastendifferenzierung mit einer IC50 von 39 nM. Sie (10 μM) hemmt die In-vitro-Osteoklastenresorption mit einer IC50 von 625 nM. Sie (2 μM) beeinflusst die Osteoblastendifferenzierung schwach. Sie (1 μM) in Kombination mit MK-2206 (2 μM) kehrt die Resistenz von RSK-exprimierenden MCF7-Zellen vollständig um. |
| In vivo |
Binimetinib (MEK162) zeigt eine dosisabhängige Hemmung der Knöchelschwellung in Rattenmodellen für Adjuvans-induzierte Arthritis (AIA), signifikant bei 10 mg/kg und 30 mg/kg im Vergleich zur Vehikelkontrolle. Diese Verbindung zeigt auch eine dosisabhängige Hemmung der Serum-IL-6-Konzentration in Rattenmodellen für Adjuvans-induzierte Arthritis (AIA), mit vollständiger Hemmung bei 10 mg/kg im Vergleich zur Vehikelkontrolle. Bei 30 mg/kg zeigt es eine dosisabhängige Hemmung der relativen Milzgewichte in Rattenmodellen für Adjuvans-induzierte Arthritis (AIA). Zusätzlich hemmt es signifikant die Knochenresorption und Entzündung bei verzögerter Dosierung im Vergleich zum Vehikel in Rattenmodellen für Adjuvans-induzierte Arthritis (AIA). ARRY-438162 (10 mg/kg, po, bid) reduziert die Krankheitsintensität dosisabhängig in Rattenmodellen für Kollagen-induzierte Arthritis (CIA) und Adjuvans-induzierte Arthritis (AIA). Es (po, bid) hemmt die Zunahme des Knöcheldurchmessers um 27% und 50% bei 1 mg/kg und 3 mg/kg im Rattenmodell für Kollagen-induzierte Arthritis (CIA), während Ibuprofen eine 46%ige Hemmung aufweist. ARRY-438162 (10 mg/kg, po, bid) hemmt signifikant Läsionen (Entzündung, Knorpelschaden, Pannusbildung und Knochenresorption) um 32% und 60% bei 1 mg/kg und 3 mg/kg im Rattenmodell für Kollagen-induzierte Arthritis (CIA). Es hemmt den AIA-Knöcheldurchmesser um 11% und 34% bei 3 mg/kg und 10 mg/kg in Rattenmodellen für Adjuvans-induzierte Arthritis (AIA). In Kombination mit BEZ235 (6 mg/kg, BID) führt es zu einer signifikanten Reduktion des Tumorwachstums in immundefizienten Mäusen, die mit MCF7-Zellen injiziert wurden. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | MEK / p-MEK / ERK / p-ERK p-KIT / KIT / ETV1 |
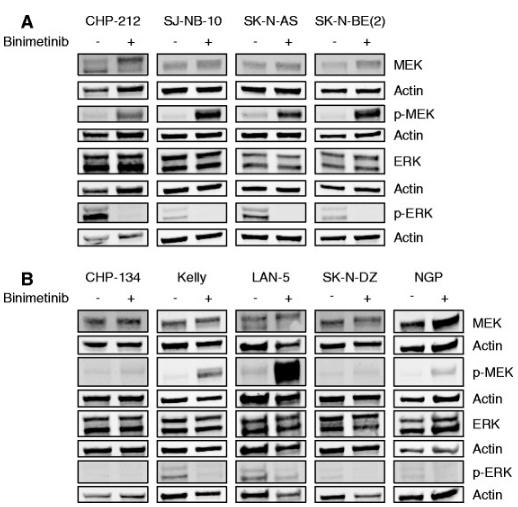
|
26925841 |
| Growth inhibition assay | Cell viability |

|
26925841 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT06207656 | Not yet recruiting | Colorectal Cancer |
Spanish Cooperative Group for the Treatment of Digestive Tumours (TTD)|Merck S.L. Spain|Pierre Fabre Ibérica S.A. |
January 19 2024 | Phase 2 |
| NCT05286788 | Recruiting | Adamantinous Craniopharyngioma|Recurrent Adamantinomatous Craniopharyngioma |
Nationwide Children''s Hospital|Children''s Hospital Colorado |
April 10 2023 | Phase 2 |
| NCT05810740 | Completed | Melanoma|BRAF V600 Mutation|Unresectable Melanoma|Metastatic Melanoma |
Pierre Fabre Medicament|Biotrial |
August 31 2022 | Phase 1 |
| NCT05195632 | Active not recruiting | Non-Small Cell Lung Cancer |
Pierre Fabre Medicament |
June 2 2022 | Phase 2 |
| NCT05767879 | Recruiting | Melanoma Stage III|In-Transit Metastasis of Cutaneous Melanoma |
Leiden University Medical Center|Pierre Fabre Laboratories |
January 1 2022 | Phase 2 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
Häufig gestellte Fragen
Frage 1:
Could you please clarify whether the formulation in vivo for S7007 is clear or not?
Antwort:
It can be dissolved in 5% DMSO+45% PEG 300+ddH2O at 5 mg/ml clearly for injection.
