nur für Forschungszwecke
Plerixafor (AMD3100) 8HCl CXCR Antagonist
Kat.-Nr.S3013
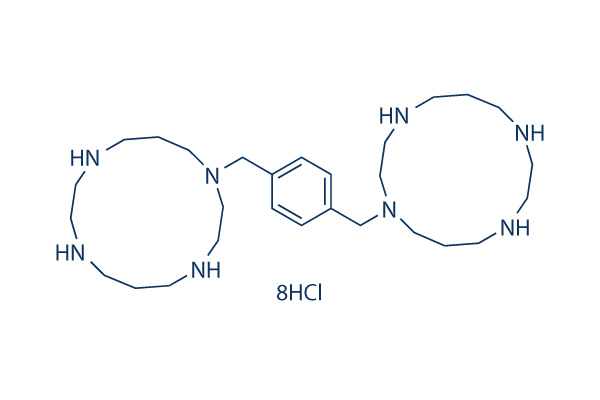
Chemische Struktur
Molekulargewicht: 794.47
Qualitätskontrolle
| Verwandte Ziele | Hedgehog/Smoothened PKA Adrenergic Receptor AChR 5-HT Receptor Histamine Receptor Dopamine Receptor Ras KRas GPR |
|---|---|
| Weitere CXCR Inhibitoren | AZD5069 SB 225002 Reparixin (Repertaxin) WZ811 Navarixin (SCH-527123) LIT-927 AMG 487 SX-682 LY2510924 Danirixin (GSK1325756) |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| CHOK1 cells | Function assay | Displacement of [125I]SDF1alpha from CXCR4 expressed in CHOK1 cells, IC50=0.81 nM | 17715128 | |||
| GHOST CXCR4 cell line | Function assay | Inhibitory concentration of compound against HIV-1 LAI strain in GHOST CXCR4 cell line, IC50=0.95 nM | 14698189 | |||
| HEK293 cells | Function assay | 2 days | Antiviral activity against T20-resistant HIV1 NL4-3 infected in HEK293 cells assessed as inhibition of viral replication after 2 days, IC50=2.3 nM | 19451305 | ||
| PBMC cells | Function assay | Effective concentration of compound against HIV-1 89.6 strain in PBMC cells, EC50=3.8 nM | 14698189 | |||
| human MT4 cells | Function assay | 4 days | Antiviral activity against HIV1 3B infected in human MT4 cells assessed as inhibition of virus replication after 4 days by MTT assay, EC50=4 nM | 20043638 | ||
| human Jurkat cells | Function assay | Antagonist activity at CXCR4 in human Jurkat cells assessed as inhibition of SDF1-induced cell migration, IC50=27.4 nM | 19188071 | |||
| MT-4 cells | Function assay | Effective concentration of compound against HIV-1 IIIB strain in MT-4 cells, EC50=65 nM | 14698189 | |||
| rat IR983F cells | Function assay | Displacement of [125I]CXCL12 from CXCR4 in rat IR983F cells, IC50=108 nM | 19053768 | |||
| CEM-SS cells | Function assay | Effective concentration of compound against HIV-1 LAI strain in CEM-SS cells, EC50=127 nM | 14698189 | |||
| human HL60 cells | Function assay | Displacement of [125I]SDF1alpha from CXCR4 in human HL60 cells, IC50=15.2 μM | 19188071 | |||
| human MOLT4 cells | Function assay | 1000 nM | Inhibition of Mab 12G5 binding to CXCR4 expressed in human MOLT4 cells at 1000 nM by FACS analysis | 19451305 | ||
| human MT2 cells | Function assay | 1 ug/mL | 4 days | Antiviral activity against HIV1 3B infected in human MT2 cells assessed as inhibition of viral p24 antigen production at 1 ug/mL after 4 days by ELISA | 21168336 | |
| human U87 cells | Function assay | 1000 nM | Antagonist activity at CXCR4 in human U87 cells assessed as inhibition of SDF1-induced modulation of cAMP production at 1000 nM by TR-FRET assay | 17958344 | ||
| MT4 | Antiviral assay | Antiviral activity against HIV1 3B assessed as reduction in cytopathic effect in MT4 cells, EC50=0.011μM | 17034122 | |||
| U87 | Function assay | 15 mins | Antagonist activity at human CXCR4 expressed in human U87 cells expressing CD4 assessed as inhibition of CXCL12-induced cAMP production pretreated for 15 mins before forskolin challenge by TR-FRET analysis, IC50=0.695μM | 21105715 | ||
| MT4 | Antiviral assay | Antiviral activity against X4-tropic HIV1 NL4.3 infected in human MT4 cells assessed as protection from virus-induced cytopathogenicity, EC50=0.062μM | 22579418 | |||
| MT4 | Antiviral assay | 5 days | Antiviral activity against HIV1 infected in MT4 cells expressing CXCR4 assessed as inhibition of virus-induced cytopathic effect after 5 days, EC50=0.002μM | 22909088 | ||
| CHO | Function assay | Binding affinity to human recombinant CXCR4 expressed in CHO cells, Kb=0.077μM | 22909088 | |||
| CHO | Function assay | Antagonist activity at human recombinant CXCR4 expressed in CHO cells assessed as inhibition of SDF1a-induced electrical impedance by dielectric spectroscopic analysis, IC50=0.26μM | 22909088 | |||
| CD44null | Function assay | 7 days | Effect on human GBM2 cell differentiation assessed as increase in CD44null cells after 7 days by flow cytometric analysis | 22909088 | ||
| CD44null | Function assay | 7 days | Effect on human GBM1 cell differentiation assessed as increase in CD44null cells after 7 days by flow cytometric analysis | 22909088 | ||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 794.47 | Formel | C28H54N8.8HCl |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 155148-31-5 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | JM 3100 8HCl,Plerixafor Octahydrochloride,AMD3100 octahydrochloride,SID791 octahydrochloride | Smiles | C1CNCCNCCCN(CCNC1)CC2=CC=C(C=C2)CN3CCCNCCNCCCNCC3.Cl.Cl.Cl.Cl.Cl.Cl.Cl.Cl | ||
Löslichkeit
|
In vitro |
Water : 100 mg/mL
DMSO
: Insoluble
Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
CXCL12
(Cell-free assay) 5.7 nM
CXCR4
(Cell-free assay) 44 nM
|
|---|---|
| In vitro |
Plerixafor hemmt die CXCL12-vermittelte Chemotaxis mit einer leicht besseren Potenz als seine Affinität für CXCR4. Plerixafor antagonisiert auch die SDF-1/CXCL12-Ligandenbindung mit einem IC50 von 651 nM. Plerixafor hemmt die SDF-1-vermittelte GTP-Bindung, den SDF-1-vermittelten Kalziumfluss und die SDF-1-stimulierte Chemotaxis mit IC50-Werten von 27 nM, 572 nM bzw. 51 nM. Plerixafor hemmt den Kalziumfluss nicht bei Zellen, die CXCR3, CCR1, CCR2b, CCR4, CCR5 oder CCR7 exprimieren, wenn sie mit ihren kognaten Liganden stimuliert werden, noch hemmt Plerixafor die Rezeptorbindung von LTB4. Plerixafor induziert von sich aus keinen Kalziumfluss in den CCRF–CEM-Zellen, die mehrere GPCRs, einschließlich CXCR4, CCR4 und CCR7, exprimieren. |
| In vivo |
Eine einzige topische Anwendung von Plerixafor fördert die Wundheilung bei diabetischen Mäusen, indem sie die Zytokinproduktion erhöht, EPCs aus dem Knochenmark mobilisiert und die Aktivität von Fibroblasten und Monozyten/Makrophagen steigert, wodurch sowohl Angiogenese als auch Vaskulogenese zunehmen. Kohorten von Mäusen werden fünf aufeinanderfolgende Tage mit PBS, IGF1, PDGF, SCF oder VEGF und am 5. Tag mit Plerixafor behandelt. Die Anzahl und Größe der Kolonien sind bei Mäusen, die mit IGF1 plus Plerixafor injiziert wurden, am höchsten im Vergleich zu den mit PDGF, SCF und VEGF behandelten Gruppen in Kombination mit Plerixafor. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Immunofluorescence | CXCR4 β-arrestin2 |
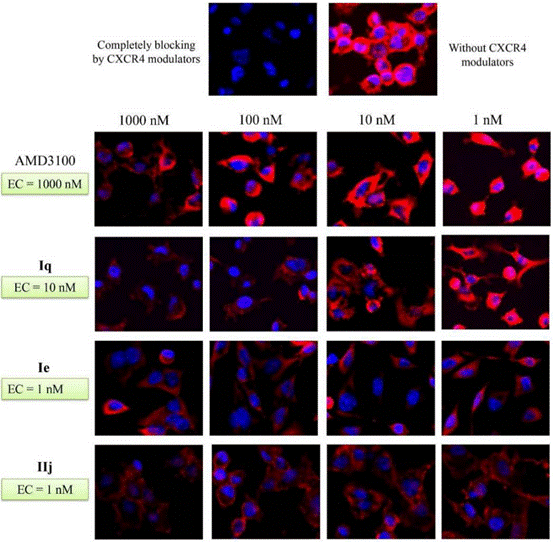
|
28521261 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT05421416 | Not yet recruiting | Stem Cell Transplant Complications |
AHS Cancer Control Alberta |
April 1 2024 | Phase 2 |
| NCT05343572 | Recruiting | Asherman Syndrome|Atrophic Endometrium|Recurrent Implantation Failure |
Hugh Taylor|Yale University |
November 1 2023 | Early Phase 1 |
| NCT05844527 | Recruiting | Wound of Skin|Abdominal Wound |
MedRegen LLC |
November 20 2023 | Phase 2 |
| NCT05411575 | Withdrawn | COVID-19 Acute Respiratory Distress Syndrome|COVID-19 |
4Living Biotech|4P-Pharma |
July 19 2022 | Phase 2 |
| NCT05445128 | Terminated | Sickle Cell Disease |
Ensoma|bluebird bio |
June 24 2022 | Phase 2 |
| NCT05835726 | Recruiting | Multiple Myeloma|Daratumumab|Autologous Stem Cell Transplantation|Leukapheresis |
Fondazione Policlinico Universitario Agostino Gemelli IRCCS |
January 1 2022 | -- |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
