nur für Forschungszwecke
PF-04217903 c-Met Inhibitor
Kat.-Nr.S1094
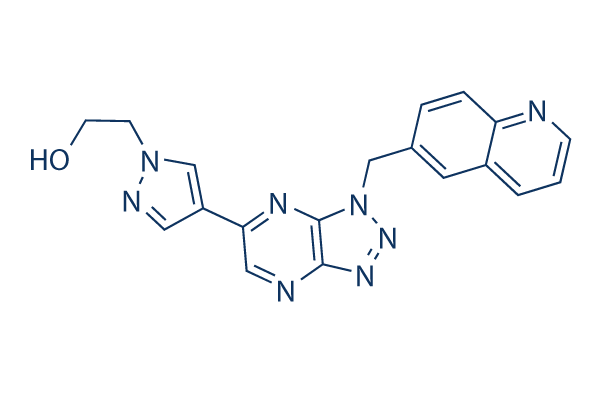
Chemische Struktur
Molekulargewicht: 372.38
Qualitätskontrolle
| Verwandte Ziele | EGFR VEGFR PDGFR FGFR Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Weitere c-Met Inhibitoren | Tepotinib Dihexa SGX-523 PHA-665752 Foretinib SU11274 BMS-777607 JNJ-38877605 Tivantinib Savolitinib (AZD6094) |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| human A549 cells | Function assay | 1 h | Antagonist activity at c-MET receptor in human A549 cells assessed as inhibition of autophosphorylation after 1 hr by ELISA, IC50=4 nM | |||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 372.38 | Formel | C19H16N8O |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 956905-27-4 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | C1=CC2=C(C=CC(=C2)CN3C4=NC(=CN=C4N=N3)C5=CN(N=C5)CCO)N=C1 | ||
Löslichkeit
|
In vitro |
DMSO
: 74 mg/mL
(198.72 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
c-Met
(A549 cells) 4.8 nM
|
|---|---|
| In vitro |
PF-04217903 ist selektiver als Staurosporin oder PF-02341066 und weist eine >1000-fache Selektivität für c-Met gegenüber einer Gruppe von 208 Kinasen auf, obwohl es anfälliger für onkogene Mutationen von c-Met ist, die die Wirksamkeit abschwächen, als PF-02341066. Zusätzlich zu WT c-Met zeigt diese Verbindung eine ähnliche Wirksamkeit bei der Hemmung der Aktivität von c-Met-H1094R, c-Met-R988C und c-Met-T1010I mit IC50-Werten von 3,1 nM, 6,4 nM bzw. 6,7 nM, hat aber keine hemmende Aktivität gegen c-Met-Y1230C mit einem IC50-Wert von >10 μM. Diese Chemikalie hemmt in Kombination mit Sunitinib signifikant Endothelzellen, aber nicht die Tumorzellen B16F1, Tib6, EL4 und LLC Sie hemmt signifikant das klonogene Wachstum von LXFA 526L und LXFA 1647L mit IC50-Werten von 16 nM bzw. 13 nM, was einen additiven Effekt ergibt, wenn sie in Kombination mit Cetuximab verwendet wird. Diese Verbindung hemmt potent c-Met-gesteuerte Prozesse wie Zellwachstum, Motilität, Invasion und Morphologie einer Vielzahl von Tumorzellen. Ihre Behandlung (2 μM) erhöhte den Zelltod von GTL-16-Zellen, was die Herunterregulierung von phosphoryliertem 4E-BP1, ERK/MAPK-assoziierten Proteinen und dem PI3K/AKT-Signalweg beinhaltet.
|
| Kinase-Assay |
Zelluläre c-Met-Phosphorylierung ELISA
|
|
A549-Zellen mit endogenem humanem WT c-Met werden in 96-Well-Platten in Wachstumsmedium ausgesät und über Nacht kultiviert. Am zweiten Tag des Assays wird das Wachstumsmedium durch serumfreies Medium (mit 0,04 % BSA) ersetzt. Serielle Verdünnungen dieser Verbindung werden zu jeder Vertiefung gegeben, und die Zellen werden 1 Stunde bei 37 °C inkubiert. Dann werden 40 ng/mL HGF zu den Zellen für 20 Minuten hinzugefügt. Die Zellen werden einmal mit HBSS gewaschen, das mit 1 mM Na3VO4 ergänzt ist, und Proteinlysate werden aus den Zellen mittels Lysepuffer hergestellt. Die Phosphorylierung von c-Met wird mittels einer ELISA-Methode bewertet, die Fängerantikörper spezifisch für c-Met und einen Detektionsantikörper spezifisch für phosphorylierte Tyrosinreste verwendet. Mit Antikörpern beschichtete Platten werden in Anwesenheit von Proteinlysaten über Nacht bei 4 °C inkubiert und siebenmal mit 1 % Tween 20 in PBS gewaschen. HRP-PY20 (Meerrettichperoxidase-konjugiertes Anti-Phosphotyrosin) wird 1:500 in Blockierungspuffer verdünnt und für 30 Minuten zu jeder Platte gegeben. Die Platten werden dann erneut gewaschen, und TMB-Peroxidase-Substrat wird hinzugefügt, um die HRP-abhängige kolorimetrische Reaktion einzuleiten, und die Reaktion wird durch Zugabe von 0,09 N H2SO4 gestoppt. ELISA-Endpunkte sind die bei 450 nm gemessene Absorption mittels eines Spektrophotometers. Der IC50-Wert wird durch Anpassung der Konzentrations-Antwort-Kurve unter Verwendung eines Microsoft Excel-basierten Vier-Parameter-Analysemet berechnet.
|
|
| In vivo |
Obwohl die Kombination von PF-04217903 und Sunitinib das Tumorwachstum in den Sunitinib-sensitiven Tumormodellen B16F1 und Tib6 nicht hemmen konnte, hemmte sie das Tumorwachstum in Sunitinib-resistenten EL4- und LLC-Tumormodellen im Vergleich zu Sunitinib oder dieser Verbindung allein signifikant, indem sie die Gefäßerweiterung signifikant blockierte, was auf eine funktionelle Rolle der HGF/c-Met-Achse in den Sunitinib-resistenten Tumoren hinweist.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT00706355 | Terminated | Neoplasms |
Pfizer |
August 2008 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
