nur für Forschungszwecke
Telatinib VEGFR Inhibitor
Kat.-Nr.S2231
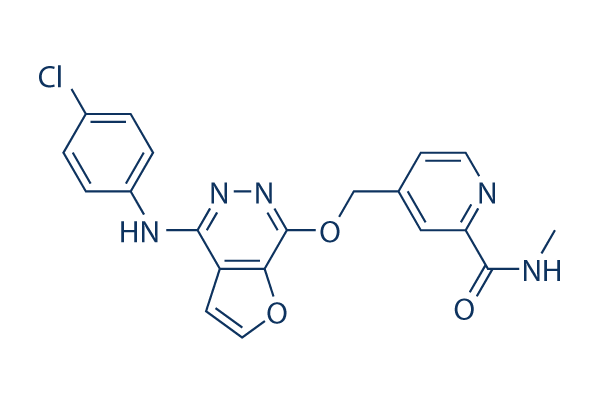
Chemische Struktur
Molekulargewicht: 409.83
Qualitätskontrolle
| Verwandte Ziele | EGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Weitere VEGFR Inhibitoren | SAR131675 SU 5402 Cediranib (AZD2171) Vatalanib (PTK787) 2HCl Anlotinib (AL3818) Dihydrochloride Linifanib (ABT-869) Apatinib (YN968D1) Apatinib (YN968D1) mesylate Ki8751 ZM 323881 HCl |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 409.83 | Formel | C20H16ClN5O3 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 332012-40-5 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | BAY 57-9352 | Smiles | CNC(=O)C1=NC=CC(=C1)COC2=NN=C(C3=C2OC=C3)NC4=CC=C(C=C4)Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 82 mg/mL
(200.08 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
c-Kit
1 nM
VEGFR3
4 nM
VEGFR2
6 nM
PDGFRα
15 nM
|
|---|---|
| In vitro |
Telatinib weist 0,66-, 0,17- bzw. 2,5-mal höhere IC50-Werte für VEGFR3, c-Kit und PDGFRβ auf als für VEGFR2, während Vatalanib 18-, 20- bzw. 16-mal höhere IC50-Werte aufweist, was darauf hindeutet, dass diese Verbindung einen potenziellen Vorteil gegenüber Vatalanib hat. Es hemmt die VEGFR2-Autophosphorylierung in einem Ganzzell-Assay mit einer IC50 von 19 nM, unterdrückt die VEGF-abhängige Proliferation menschlicher Nabelschnurvenen-Endothelzellen mit einer IC50 von 26 nM und blockiert das PDGF-stimulierte Wachstum menschlicher Aorten-Glatte-Muskelzellen mit einer IC50 von 249 nM. Diese Verbindung zeigt nur geringe hemmende Aktivität gegen den Raf-Kinase-Signalweg, die Familie der epidermalen Wachstumsfaktorrezeptoren, die Familie der Fibroblasten-Wachstumsfaktorrezeptoren (FGFR) und den Tie-2-Rezeptor.
|
| In vivo |
Angesichts der Tatsache, dass Tumorentwicklung und Metastasierung auf einen deregulierten VEGFR-Signalweg zurückgeführt werden, hemmt die Telatinib-Behandlung das Tumorwachstum und die Metastasierung signifikant, indem sie die VEGFR-Signalgebung und anschließend die Tumorangiogenese blockiert. Zusätzlich zur signifikanten Hemmung der Tumorangiogenese induziert diese Wirkstoffbehandlung eine signifikante Abnahme der Endothel-abhängigen und Endothel-unabhängigen Vasodilatation sowie eine Reduzierung der Kapillardichte, was zu einem Anstieg des systolischen und diastolischen Blutdrucks führt. Die Verabreichung dieses Mittels als Einzelwirkstoff zeigt eine potente Antitumoraktivität in verschiedenen menschlichen Tumor-Xenograft-Modellen, einschließlich MDA-MB-231-Brustkrebs, Colo-205-Darmkrebs, DLD-1-Darmkrebs und H460-nicht-kleinzelligem Lungenkrebs, sowie bei Pankreas- und Prostatakarzinomen in einer dosisabhängigen Weise.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
