
- Inhibitors
- Antikörper
- Substanzbibliotheken
- Beliebte Substanzbibliotheken
- Bibliothek anpassen
- Klinisch und FDA-zugelassen
- Bioaktive Substanzbibliotheken
- Inhibitorbezogen
- Related=Naturproduktbezogen
- Stoffwechselbezogen
- Zelltodbezogen
- Nach Signalweg
- Nach Krankheit
- Antiinfektiös und antiviral
- Neuronal und immunologisch
- Fragment- und kovalentbezogen
- FDA-approved Drug Library
- FDA-approved & Passed Phase I Drug Library
- Preclinical/Clinical Compound Library
- Bioactive Compound Library-I
- Bioactive Compound Library-Ⅱ
- Kinase Inhibitor Library
- Express-Pick Library
- Natural Product Library
- Human Endogenous Metabolite Compound Library
- Alkaloid Compound LibraryNeu
- Angiogenesis Related compound Library
- Anti-Aging Compound Library
- Anti-alzheimer Disease Compound Library
- Antibiotics compound Library
- Anti-cancer Compound Library
- Anti-cancer Compound Library-Ⅱ
- Anti-cancer Metabolism Compound Library
- Anti-Cardiovascular Disease Compound Library
- Anti-diabetic Compound Library
- Anti-infection Compound Library
- Antioxidant Compound Library
- Anti-parasitic Compound Library
- Antiviral Compound Library
- Apoptosis Compound Library
- Autophagy Compound Library
- Calcium Channel Blocker LibraryNeu
- Cambridge Cancer Compound Library
- Carbohydrate Metabolism Compound LibraryNeu
- Cell Cycle compound library
- CNS-Penetrant Compound Library
- Covalent Inhibitor Library
- Cytokine Inhibitor LibraryNeu
- Cytoskeletal Signaling Pathway Compound Library
- DNA Damage/DNA Repair compound Library
- Drug-like Compound Library
- Endoplasmic Reticulum Stress Compound Library
- Epigenetics Compound Library
- Exosome Secretion Related Compound LibraryNeu
- FDA-approved Anticancer Drug LibraryNeu
- Ferroptosis Compound Library
- Flavonoid Compound Library
- Fragment Library
- Glutamine Metabolism Compound Library
- Glycolysis Compound Library
- GPCR Compound Library
- Gut Microbial Metabolite Library
- HIF-1 Signaling Pathway Compound Library
- Highly Selective Inhibitor Library
- Histone modification compound library
- HTS Library for Drug Discovery
- Human Hormone Related Compound LibraryNeu
- Human Transcription Factor Compound LibraryNeu
- Immunology/Inflammation Compound Library
- Inhibitor Library
- Ion Channel Ligand Library
- JAK/STAT compound library
- Lipid Metabolism Compound LibraryNeu
- Macrocyclic Compound Library
- MAPK Inhibitor Library
- Medicine Food Homology Compound Library
- Metabolism Compound Library
- Methylation Compound Library
- Mouse Metabolite Compound LibraryNeu
- Natural Organic Compound Library
- Neuronal Signaling Compound Library
- NF-κB Signaling Compound Library
- Nucleoside Analogue Library
- Obesity Compound Library
- Oxidative Stress Compound LibraryNeu
- Plant Extract Library
- Phenotypic Screening Library
- PI3K/Akt Inhibitor Library
- Protease Inhibitor Library
- Protein-protein Interaction Inhibitor Library
- Pyroptosis Compound Library
- Small Molecule Immuno-Oncology Compound Library
- Mitochondria-Targeted Compound LibraryNeu
- Stem Cell Differentiation Compound LibraryNeu
- Stem Cell Signaling Compound Library
- Natural Phenol Compound LibraryNeu
- Natural Terpenoid Compound LibraryNeu
- TGF-beta/Smad compound library
- Traditional Chinese Medicine Library
- Tyrosine Kinase Inhibitor Library
- Ubiquitination Compound Library
-
Cherry Picking
Sie können Ihre Bibliothek mit Chemikalien aus dem Bestand von Selleck personalisieren. Erstellen Sie die richtige Bibliothek für Ihre Forschungszwecke, indem Sie aus Verbindungen in all unseren verfügbaren Bibliotheken wählen.
Bitte kontaktieren Sie uns unter info@selleckchem.com um Ihre Bibliothek anzupassen.
Sie könnten auswählen:
- Bioreagenzien
- qPCR
- 2x SYBR Green qPCR Master Mix
- 2x SYBR Green qPCR Master Mix (Low ROX)
- 2x SYBR Green qPCR Master Mix (High ROX)
- Protein-Assay
- Protein A/G Magnetkügelchen für IP
- Anti-Flag Magnetkügelchen
- Anti-Flag Affinitätsgel
- Anti-Myc Magnetkügelchen
- Anti-HA Magnetkügelchen
- Poly-DYKDDDDK-Tag-Peptid lyophilisiertes Pulver
- Protease-Inhibitor-Cocktail
- Protease-Inhibitor-Cocktail (EDTA-frei, 100X in DMSO)
- Phosphatase-Inhibitor-Cocktail (2 Röhrchen, 100X)
- Zellbiologie
- Zellzähl-Kit-8 (CCK-8)
- Tierexperiment
- Maus-Direkt-PCR-Kit (für Genotypisierung)
- Ausgewählte Produkte
- MRTX1133
- MRTX1133
- KP-457
- IAG933
- RMC-6236 (Daraxonrasib)
- RMC-7977
- Zoldonrasib (RMC-9805)
- GsMTx4
- Navitoclax (ABT-263)
- Y-27632 Dihydrochloride
- Y-27632 Dihydrochloride
- SB431542
- SB202190
- MK-2206 Dihydrochloride
- LY294002
- Alisertib (MLN8237)
- XAV-939
- CHIR-99021 (Laduviglusib)
- Bafilomycin A1 (Baf-A1)
- Thiazovivin (TZV)
- CP-673451
- Verteporfin
- DAPT
- Galunisertib (LY2157299)
- MG132
- SBE-β-CD
- Tween 80
- Bavdegalutamide (ARV-110)
- Z-VAD-FMK
- Wnt-C59 (C59)
- IWR-1-endo
- (+)-JQ1
- 3-Deazaneplanocin A (DZNep) Hydrochloride
- RepSox (E-616452)
- Erastin
- Q-VD-Oph
- Puromycin Dihydrochloride
- Cycloheximide
- Telaglenastat (CB-839)
- A-83-01
- Ceralasertib (AZD6738)
- Liproxstatin-1
- Emricasan (IDN-6556)
- PMA (Phorbol 12-myristate 13-acetate)
- Dibutyryl cAMP (Bucladesine) sodium
- Nedisertib (M3814)
- PLX5622
- IKE (Imidazole Ketone Erastin)
- STM2457
- Saruparib (AZD5305)
- Neue Produkte
- Kontakt
nur für Forschungszwecke
Bafilomycin A1 (Baf-A1) V-ATPase-Inhibitor
Kat.-Nr.S1413
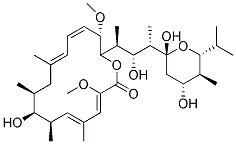
Chemische Struktur
Molekulargewicht: 622.83
Qualitätskontrolle
Charge:
Reinheit: >97%
97
Produkte, die oft zusammen verwendet werden mit Bafilomycin A1 (Baf-A1)
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| human H4 cells | Function assay | 0.4 μM | 24 h | Induction of light chain 3-GFP level in human H4 cells at 0.4 uM after 24 hrs by high throughput fluorescence microscopy relative to control | 18024584 | |
| RAW 264.7 cells | Function assay | 100 nM | Antimicrobial activity against Salmonella enterica Typhimurium 14028 infected in RAW 264.7 cells assessed as increased nitric oxide production in infected cells at 100 nM | 19307359 | ||
| mouse RAW264.7 cells | Apoptosis assay | 100 nM | 16 h | Induction of apoptosis in mouse RAW264.7 cells assessed as late apoptotic cells at 100 nM after 16 hrs using annexin V-propidium iodide staining by flow cytometry | 19307359 | |
| human HeLa cells | Function assay | 400 nM | Induction of autophagy in human HeLa cells expressing EGFP-LC3 assessed as increase in LC3-2 level at 400 nM | 18391949 | ||
| human MCF7 cells | Function assay | 4 h | Inhibition of rapamycin-induced autophagy in human MCF7 cells expressing EGFP-LC3 assessed as decrease in EGFP levels at 100 nM after 4 hrs by Western blotting relative to control | 20028134 | ||
| RAW 264.7 cells | Bactericidal activity assay | 100 nM | 16 h | Bactericidal activity against Salmonella enterica Typhimurium 14028 infected in RAW 264.7 cells assessed as decrease in bacterial growth yield at 100 nM after 16 hrs postinfection by flow cytometry in presence of 10 ug/ml of intracellular replication inhi | 19307359 | |
| RAW 264.7 cells | Antimicrobial activity assay | 100 nM | Antimicrobial activity against Salmonella enterica Typhimurium 14028 infected in RAW 264.7 cells assessed as increased nitric oxide production in infected cells at 100 nM | 19307359 | ||
| RAW 264.7 cells | Antimicrobial activity assay | 100 nM | 30 mins | Antimicrobial activity against Salmonella enterica Typhimurium 14028 infected in RAW 264.7 cells assessed as inhibition of bacterial replication at 100 nM treated 30 mins before infection measured after 2 to 16 hrs postinfection by flow cytometry | 19307359 | |
| rat 3Y1 cells | Function assay | Induction of morphological changes in rat 3Y1 cells assessed as elongation of cells | 29701963 | |||
| human Huh7.5.1 cells | Antiviral activity | 3 h | Antiviral activity against HCV genotype 2a JFH-1 in human Huh7.5.1 cells assessed as reduction of viral entry up to 3 hrs by luciferase assay | 26396683 | ||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 622.83 | Formel | C35H58O9 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 88899-55-2 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC1CC(=CC=CC(C(OC(=O)C(=CC(=CC(C1O)C)C)OC)C(C)C(C(C)C2(CC(C(C(O2)C(C)C)C)O)O)O)OC)C | ||
Löslichkeit
|
In vitro |
|
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
mg/kg
g
μL
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
% DMSO
%
% Tween 80
% ddH2O
%DMSO
%
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
H+-ATPase [1]
(Cell-free assay) 0.44 nM
|
|---|---|
| In vitro |
Bafilomycin A1 (Baf-A1) ist ein toxisches Makrolid-Antibiotikum, das aus Streptomyces griseus gewonnen wird und den durch das äußere Mantelepithel (OME) induzierten Kurzschlussstrom hemmt. Die IC50- und maximale Hemmdosis dieser Verbindung betragen 0,17 μM bzw. 0,5 μM.[2]Darüber hinaus hemmt sie den Säreeinstrom mit einem IC50-Wert von 0,4 nM. Sie hemmt auch die Säuerung dosisabhängig, was zu einer geringeren Löschung und damit zu einer höheren Fluoreszenz führt.[3] Es verhindert die durch H. pylori induzierte Vakuolisierung von Hela-Zellen mit einer Hemmkonzentration von 4 nM (ID50), die 50 % des Maximums entspricht, und ist sehr effizient bei der Wiederherstellung des normalen Aussehens vakuolisierter Zellen.[4] Es beeinflusst auch den Transport von endozytiertem Material von frühen zu späten endozytischen Kompartimenten, wodurch nicht nur der niedrige endosomale pH-Wert aufgehoben, sondern auch der Transport von frühen zu späten Endosomen in HeLa-Zellen blockiert wird.[5] Bei Konzentrationen von 0,1–1 μM hemmt es die Ansäuerung von Lysosomen vollständig, was durch Inkubation mit Acridinorange in BNL CL.2- und A431-Zellen nachgewiesen wurde.[6]Wird es zu Hanks' ausgewogener Salzlösung gegeben, wird der endogene Proteinabbau stark gehemmt und es sammeln sich zahlreiche Autophagosomen in H-4-II-E-Zellen an. Zudem verhindert es das Auftreten von endozytiertem HRP in autophagischen Vakuolen. [7]
|
| Kinase-Assay |
ATPase-Enzymaktivitätsassays
|
|
Das ATPase-Enzym-Assay-Medium enthält 6 mM MgSO4, 50 mM HEPES (pH 7,4), 200 mM Na2SO3 (V-ATPase-Aktivator), 0,5 mM Natriumorthovanadat (P-ATPase-Inhibitor), 0,5 mM Natriumazid (F-ATPase-Inhibitor) und 3 mM Na2ATP. Dieses Medium (1,0 ml) wird mit oder ohne Zugabe des V-Typ-ATPase-Inhibitors Bafilomycin A1 (Baf-A1) 60 Minuten lang bei 23–25 °C mit dem gefilterten Homogenat (0,1 ml) inkubiert. Die Reaktion wird durch Zugabe von 1 ml TCA 3 % gestoppt. Spektrometrische Blindproben werden wie für den Enzymtest vorbereitet, mit der Ausnahme, dass die Gewebeprobe nach der Säure hinzugefügt wird. Die Phosphatanalyse erfolgt durch Zugabe von 2 ml 1-Butanol und 0,2 ml Molybdatlösung (5 g Ammoniummolybdat, 22 ml H2SO4 auf 100 ml). Nach 15 Sekunden Vortexen wird die Lösung mit 0,5 ml Citratlösung (100 g/500 ml, pH 7,0) neutralisiert und erneut 15 Sekunden lang vortexiert. Die Lösung wird dann zentrifugiert (2000 × g; 3 Minuten), um die Butanolphase abzutrennen, und die Absorption dieser Phase wird bei 400 nm gemessen. Orthophosphat-Standards werden hergestellt (0,1 μM–2,0 μM) und auf die gleiche Weise wie die Enzymaktivitätstests behandelt. Die Enzymaktivität wird in μmol freigesetztem Orthophosphat pro Stunde und pro Milligramm Protein angegeben. Die V-ATPase-Aktivität wird als Differenz zwischen der gesamten ATPase-Aktivität, gemessen in Gegenwart von Na2SO3, Natriumorthovanadat und Natriumazid, und der ATPase-Aktivität, gemessen in Gegenwart dieser Reagenzien und dieser Verbindung, betrachtet.
|
|
| In vivo | Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
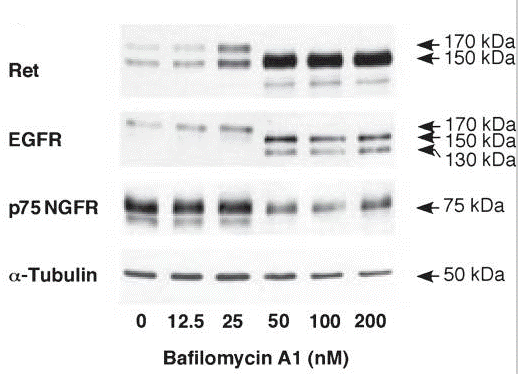
| Western blot | Ret / EGFR / p75 NGFR |
|
21559479 |
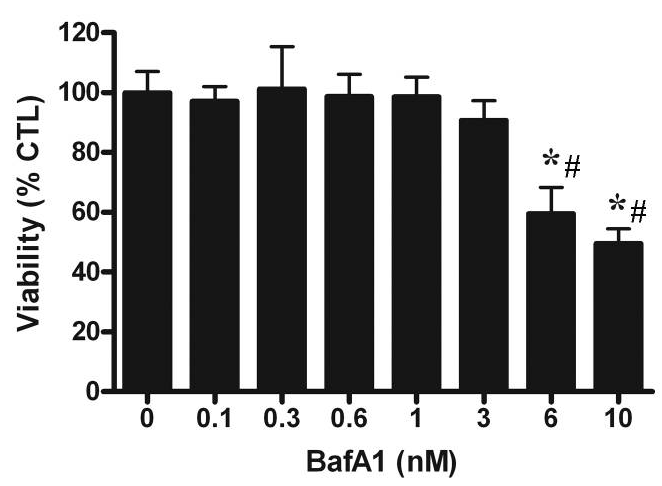
| Growth inhibition assay | Cell viability |
|
20534000 |
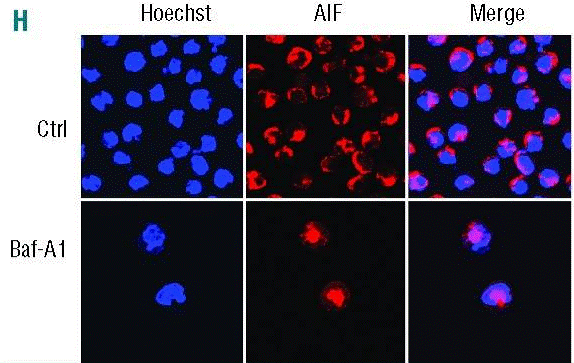
| Immunofluorescence | AIF LC3 |
|
25512644 |
| ELISA | TNF-alpha |
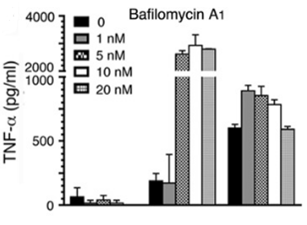
|
26240140 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
Häufig gestellte Fragen
Frage 1:
How to dissolve it?
Antwort:
S1413 is soluble in DMSO at 6 mg/ml. Please do not use alcohols as solvent, because this compound will degrade in alcohols.
