nur für Forschungszwecke
Crenolanib (CP-868596) PDGFR/FLT3 Inhibitor
Kat.-Nr.S2730
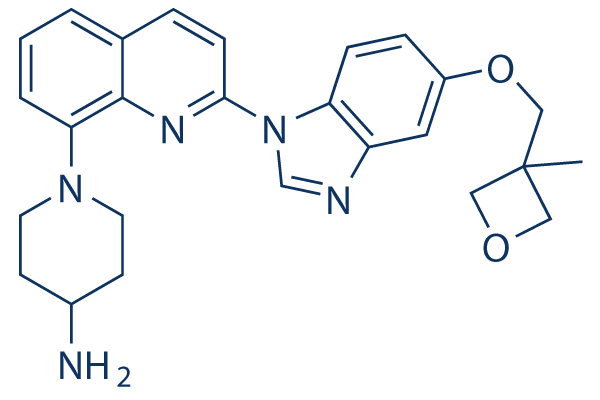
Chemische Struktur
Molekulargewicht: 443.54
Qualitätskontrolle
| Verwandte Ziele | EGFR VEGFR JAK PDGFR FGFR Src HIF FLT HER2 Bcr-Abl |
|---|---|
| Weitere FLT3 Inhibitoren | UNC2025 Dovitinib (TKI-258) Dovitinib (TKI258) Lactate monohydrate Tandutinib (MLN518) KW-2449 ENMD-2076 AST-487 (NVP-AST487) TCS 359 G-749 AMG 925 |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| A549 cells | Cell viability assay | 3.9-1000 nM | 72 h | a dose-dependent inhibition of cancer cell viability | 25328409 | |
| MV4-11 | Function assay | a decrease in mitochondrial matrix protein aconitase hydratase 2 (ACO2) | 25328409 | |||
| MV4-11 | Cytotoxicity assay | Cytotoxicity against human MV4-11 cells expressing FLT3 ITD mutant, IC50=0.0015μM | 31207462 | |||
| MOLM13 | Cytotoxicity assay | Cytotoxicity against human MOLM13 cells expressing FLT3 ITD mutant, IC50=0.0049μM | 31207462 | |||
| MV4-11 | Cytotoxicity assay | 72 hrs | Cytotoxicity in human MV4-11 cells assessed as inhibition of cellular viability incubated for 72 hrs by CellTiter-Blue assay, IC50=0.012μM | 30742435 | ||
| DAOY | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for DAOY cells | 29435139 | |||
| SJ-GBM2 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SJ-GBM2 cells | 29435139 | |||
| SK-N-MC | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SK-N-MC cells | 29435139 | |||
| BT-37 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for BT-37 cells | 29435139 | |||
| NB-EBc1 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for NB-EBc1 cells | 29435139 | |||
| U-2 OS | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for U-2 OS cells | 29435139 | |||
| Saos-2 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Saos-2 cells | 29435139 | |||
| LAN-5 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for LAN-5 cells | 29435139 | |||
| BT-12 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for BT-12 cells | 29435139 | |||
| Rh18 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Rh18 cells | 29435139 | |||
| OHS-50 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for OHS-50 cells | 29435139 | |||
| RD | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for RD cells | 29435139 | |||
| A673 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for A673 cells) | 29435139 | |||
| DAOY | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for DAOY cells | 29435139 | |||
| U-2 OS | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for U-2 OS cells | 29435139 | |||
| Rh41 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for Rh41 cells | 29435139 | |||
| SK-N-SH | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for SK-N-SH cells | 29435139 | |||
| MV4-11 | Cytotoxicity assay | 0.5 to 5000 nM | 2 to 8 hrs | Cytotoxicity in human MV4-11 cells assessed as inhibition of cellular viability at 0.5 to 5000 nM incubated for 2 to 8 hrs followed by compound washout by CellTiter-Glo luminescent assay | 30742435 | |
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 443.54 | Formel | C26H29N5O2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 670220-88-9 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | CP-868596, ARO 002 | Smiles | CC1(COC1)COC2=CC3=C(C=C2)N(C=N3)C4=NC5=C(C=CC=C5N6CCC(CC6)N)C=C4 | ||
Löslichkeit
|
In vitro |
DMSO
: 88 mg/mL
(198.4 mM)
Ethanol : 88 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
FLT3
(CHO cells) 0.74 nM(Kd)
PDGFRα
(CHO cells) 2.1 nM(Kd)
PDGFRβ
(CHO cells) 3.2 nM(Kd)
|
|---|---|
| In vitro |
Crenolanib ist signifikant potenter bei der Hemmung der Kinaseaktivität von resistenten PDGFRα-Kinasen (D842I, D842V, D842Y, D1842-843IM und Deletion I843). Diese Verbindung ist in dem isogenen Modellsystem mit einer IC50 von ungefähr 10 nM potenter gegen D842V. Es hemmt die Kinaseaktivität des Fusionsonkogens in der EOL-1-Zelllinie, die von einem Patienten mit chronischer eosinophiler Leukämie stammt und die konstitutiv aktivierte FIP1L1-PDGFRα-Fusionskinase exprimiert, mit IC50 = 21 nM. Diese Chemikalie hemmt auch die Proliferation von EOL-1-Zellen mit IC50 = 0,2 pM. Sie hemmt die Aktivierung von V561D- oder D842V-mutierten Kinasen, die in BaF3-Zellen exprimiert werden, mit IC50 von 85 nM bzw. 272 nM. Diese Verbindung hemmt die PDGFRα-Aktivierung in der H1703-Nicht-kleinzelligen Lungenkrebszelllinie, die eine 24-fache Amplifikation der 4q12-Region aufweist, die den PDGFRα-Locus enthält, mit IC50 von 26 nM. Es ist ein oral bioverfügbarer, hochpotenter und selektiver PDGFR TKI. Diese Benzimidazolverbindung hat IC50-Werte von 0,9 nM und 1,8 nM für PDGFRA bzw. PDGFRB. |
| Kinase-Assay |
Biochemische Bewertung der PDGFRα-Kinaseaktivität
|
|
Chinesische Hamster-Ovarialzellen (CHO) werden transient mit mutierten oder Wildtyp-PDGFRα-Konstrukten transfiziert und mit verschiedenen Konzentrationen von Crenolanib behandelt. Experimente mit rekombinanter DNA werden unter Biosicherheitsstufe 2 gemäß den Richtlinien durchgeführt. Proteinlysate aus Zelllinien werden hergestellt und einer Immunpräzipitation unterzogen, wobei Anti-PDGFRα-Antikörper verwendet werden, gefolgt von einem sequenziellen Immunblotting für PDGFRα. Die Densitometrie wird zur Quantifizierung des Arzneimitteleffekts mit Photoshop-Software durchgeführt, wobei der Phosphor-PDGFRα-Spiegel auf das Gesamtprotein normalisiert wird. Densitometrie- und Proliferationsexperimentergebnisse werden mit Calcusyn 2.1-Software analysiert, um die IC50-Werte mathematisch zu bestimmen. Der Wilcoxon-Rangsummentest wird verwendet, um die IC50-Werte dieser Verbindung für eine gegebene Mutation zu vergleichen.
|
|
| In vivo |
Diese Verbindung, ein PDGFR-Inhibitor, unterdrückt die Proliferation von Lungenkrebszellen und hemmt das Tumorwachstum in vivo |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | pKIT / KIT pFLT3 / FLT3 / pERK / ERK / pS6 / S6 pAKT / AKT / pMAPK / MAPK / pSTAT5 / STAT5 |

|
24623852 |
| Growth inhibition assay | Cell viability |
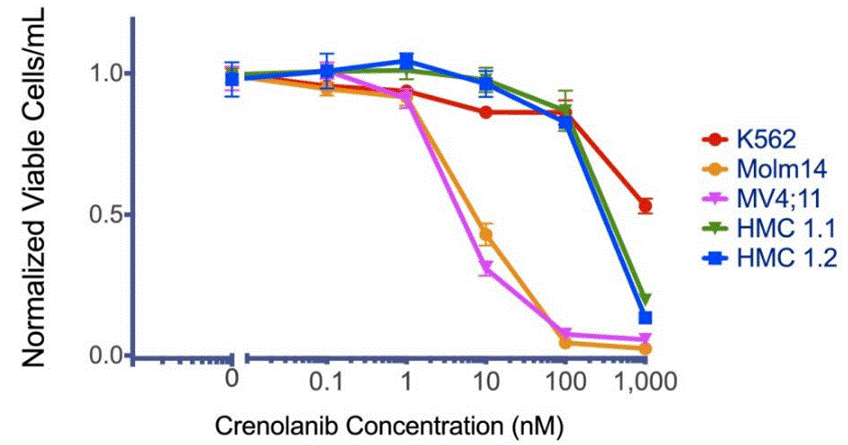
|
24623852 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT00949624 | Completed | Advanced Solid Tumors |
Arog Pharmaceuticals Inc. |
December 2005 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
