nur für Forschungszwecke
Donafenib (Sorafenib D3) Raf Inhibitor
Kat.-Nr.S9621
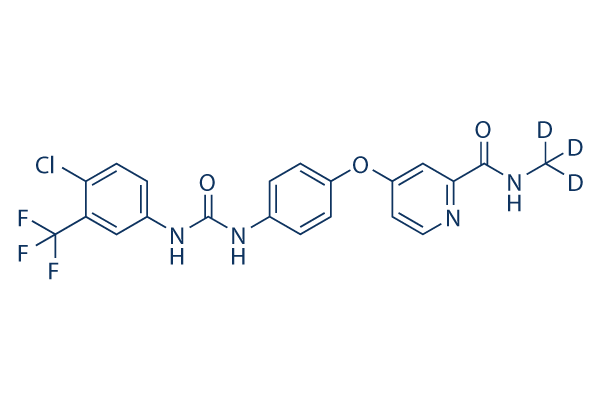
Chemische Struktur
Molekulargewicht: 467.84
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- HPLC
- SDS
- Datenblatt
| Verwandte Ziele | ERK p38 MAPK JNK MEK Ras KRas S6 Kinase MAP4K TAK1 Mixed Lineage Kinase |
|---|---|
| Weitere Raf Inhibitoren | LY3009120 Exarafenib (KIN-2787) GDC-0879 Avutometinib (Ro5126766, CH5126766) PLX-4720 AZ 628 SB590885 TAK-632 GW5074 RAF265 (CHIR-265) |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 467.84 | Formel | C21H13D3ClF3N4O3 |
Lagerung (Ab dem Eingangsdatum) | 3 years -20°C powder |
|---|---|---|---|---|---|
| CAS-Nr. | 1130115-44-4 | -- | Lagerung von Stammlösungen |
|
|
| Synonyme | Bay 43-9006 D3, CM-4307 | Smiles | CNC(=O)C1=NC=CC(=C1)OC2=CC=C(C=C2)NC(=O)NC3=CC(=C(C=C3)Cl)C(F)(F)F | ||
Löslichkeit
|
In vitro |
DMSO
: 94 mg/mL
(200.92 mM)
Ethanol : 6 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Raf-1
(Cell-free assay) 6 nM
mVEGFR-2
(Cell-free assay) 15 nM
mVEGFR-3
(Cell-free assay) 20 nM
B-Raf
(Cell-free assay) 22 nM
|
|---|---|
| In vitro |
BAY 43-9006 unterdrückt sowohl die Wildtyp- als auch die V599E-Mutante BRAF-Aktivität in vitro. Darüber hinaus zeigt BAY 43-9006 eine signifikante Aktivität gegen mehrere Rezeptor-Tyrosinkinasen, die an der Neovaskularisierung und Tumorprogression beteiligt sind, einschließlich des vaskulären endothelialen Wachstumsfaktorrezeptors (VEGFR)-2, VEGFR-3, des Platelet-Derived Growth Factor Receptor β, Flt-3 und c-KIT. In zellulären mechanistischen Assays zeigt BAY 43-9006 eine Hemmung des Mitogen-aktivierten Proteinkinase-Weges in Darm-, Pankreas- und Brusttumorzelllinien, die mutiertes KRAS oder Wildtyp- oder mutiertes BRAF exprimieren, während nicht-kleinzellige Lungenkrebszelllinien, die mutiertes KRAS exprimieren, unempfindlich gegenüber der Hemmung des Mitogen-aktivierten Proteinkinase-Weges durch BAY 43-9006 sind. Eine potente Hemmung der zellulären Rezeptor-Autophosphorylierung von VEGFR-2, Platelet-Derived Growth Factor Receptor β und VEGFR-3 wird ebenfalls für BAY 43-9006 beobachtet. |
| In vivo |
Die einmal tägliche orale Verabreichung von BAY 43-9006 zeigt eine breitgefächerte Antitumoraktivität in Xenograft-Modellen für Darm-, Brust- und nicht-kleinzelligen Lungenkrebs. Die Immunhistochemie zeigt eine enge Verbindung zwischen der Hemmung des Tumorwachstums und der Hemmung der extrazellulären signalregulierten Kinasen (ERKs) 1/2-Phosphorylierung in zwei von drei untersuchten Xenograft-Modellen, was mit der Hemmung des RAF/MEK/ERK-Weges in einigen, aber nicht allen Modellen übereinstimmt. Zusätzliche Analysen der Mikrovaskulardichte und der Mikrovaskularfläche in den gleichen Tumorschnitten unter Verwendung von antimurinen CD31-Antikörpern zeigen eine signifikante Hemmung der Neovaskularisierung in allen drei Xenograft-Modellen. |
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT04612712 | Recruiting | Advanced Gastrointestinal Tumors |
Suzhou Zelgen Biopharmaceuticals Co.Ltd|Jiangsu Alphamab Biopharmaceuticals Co. Ltd |
January 19 2021 | Phase 1|Phase 2 |
| NCT04816123 | Completed | Healthy Male Adult |
Suzhou Zelgen Biopharmaceuticals Co.Ltd |
October 9 2018 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
