nur für Forschungszwecke
TAK-632 Raf Inhibitor
Kat.-Nr.S7291
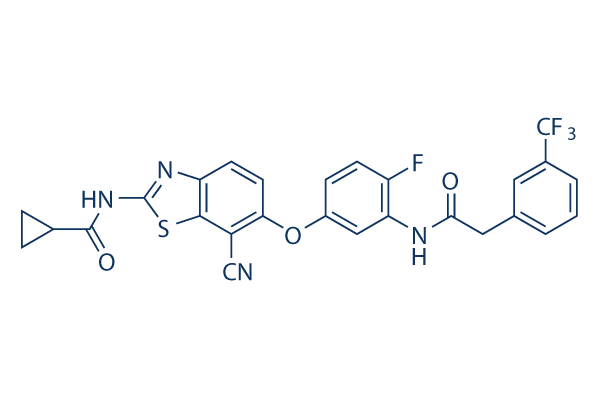
Chemische Struktur
Molekulargewicht: 554.52
Qualitätskontrolle
| Verwandte Ziele | ERK p38 MAPK JNK MEK Ras KRas S6 Kinase MAP4K TAK1 Mixed Lineage Kinase |
|---|---|
| Weitere Raf Inhibitoren | LY3009120 Exarafenib (KIN-2787) GDC-0879 Avutometinib (Ro5126766, CH5126766) PLX-4720 AZ 628 SB590885 GW5074 RAF265 (CHIR-265) PLX8394 (Plixorafenib, FORE8394) |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| human A375 cells | Function assay | 2 h | Inhibition of BRAF V600E mutant in human A375 cells assessed as phosphorylation of MEK after 2 hrs by Western blotting analysis, IC50=12 nM | |||
| human HMVII cells | Function assay | 2 h | Inhibition of NRASQ61k/BRAFG469V-mutant in human HMVII cells assessed as phosphorylation of MEK after 2 hrs by Western blotting analysis, IC50=49 nM | |||
| human HT-29 cells | Function assay | Inhibition of BRAF V600E mutant in human HT-29 cells assessed as phosphorylation of MEK, IC50=75 nM | ||||
| human HMVII cells | Proliferation assay | 72 h | Antiproliferative activity against human HMVII cells assessed as growth inhibition after 72 hrs by chemi-luminescence cell viability assay, GI50=0.2 μM | |||
| 293 cells | Function assay | 20 mins | Inhibition of N-terminal GST-tagged MEK1 (unknown origin) expressed in 293 cells using GST-ERK1(K71A) as substrate after 20 mins, IC50=3.7 μM | |||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 554.52 | Formel | C27H18F4N4O3S |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1228591-30-7 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | C1CC1C(=O)NC2=NC3=C(S2)C(=C(C=C3)OC4=CC(=C(C=C4)F)NC(=O)CC5=CC(=CC=C5)C(F)(F)F)C#N | ||
Löslichkeit
|
In vitro |
DMSO
: 100 mg/mL
(180.33 mM)
Ethanol : 2 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
Orally bioavailable, pan-raf inhibitor that targets both wild-type and mutant forms.
|
|---|---|
| Targets/IC50/Ki |
C-Raf
(Cell-free assay) 1.4 nM
B-Raf
(Cell-free assay) 8.3 nM
Aurora B
(Cell-free assay) 66 nM
PDGFRβ
(Cell-free assay) 120 nM
FGFR3
(Cell-free assay) 280 nM
GSK-3β
(Cell-free assay) 500 nM
CDK2
(Cell-free assay) 580 nM
p38α
(Cell-free assay) 600 nM
PDGFRα
(Cell-free assay) 610 nM
|
| In vitro |
TAK-632 hemmt die Phosphorylierung von MEK und ERK in Melanom-A375-Zellen (BRAFV600E) mit einer IC50 von 12 nM bzw. 16 nM. In menschlichen Melanom-HMVII-Zellen (NRASQ61K/BRAFG469V) zeigt diese Verbindung auch eine starke Hemmung von pMEK und pERK mit einer IC50 von 49 nM bzw. 50 nM. Darüber hinaus zeigt sie auch eine antiproliferative Aktivität in sowohl A375- als auch HMVII-Zellen mit einer GI50 von 66 nM bzw. 200 nM. Diese Chemikalie induziert die RAF-Dimerisierung, hemmt jedoch die Kinaseaktivität des RAF-Dimers aufgrund ihrer langsamen Dissoziation von RAF. Die Kombination dieser Verbindung und TAK-733 zeigt synergistische antiproliferative Effekte in BRAF- und NRAS-mutierten Melanomzellen.
|
| Kinase-Assay |
Kinaseprofil-Assay
|
|
Assays für Serin/Threonin-Kinasen unter Verwendung von radiomarkiertem [γ-33P]-ATP werden in 96-Well-Platten durchgeführt. BRAF und c-RAF werden als N-terminal FLAG-markiertes Protein unter Verwendung eines Baculovirus-Expressionssystems exprimiert. Die Reaktionsbedingungen sind für jede Kinase optimiert: BRAF (25 ng/Well Enzym, 1 μg/Well GST-MEK1(K96R), 0,1 μCi/Well [γ-32P]-ATP, Raumtemperatur, 20 min Reaktion); c-RAF (25 ng/Well Enzym, 1 μg/Well GST-MEK1 (K96R), 0,1 μCi/Well [γ-32P]-ATP, Raumtemperatur, 20 min Reaktion). Enzymreaktionen werden in 25 mM HEPES, pH 7,5, 10 mM Magnesiumacetat, 1 mM Dithiothreitol und 0,5 μM ATP, enthaltend eine optimierte Konzentration von Enzym, Substrat und radiomarkiertem ATP, wie oben beschrieben, in einem Gesamtvolumen von 50 μL durchgeführt. Vor der Kinase-Reaktion werden diese Verbindung und das Enzym 5 min lang bei der oben beschriebenen Reaktionstemperatur inkubiert. Die Kinase-Reaktionen werden durch Zugabe von ATP gestartet. Nach der oben beschriebenen Reaktionsdauer werden die Reaktionen durch Zugabe von 10%iger (Endkonzentration) Trichloressigsäure beendet. Die [γ-33P]- oder [γ-32P]-phosphorylierten Proteine werden in GFC-Filterplatten mit einem Cell Harvester filtriert, und dann werden die Platten mit 3%iger Phosphorsäure gewaschen. Die Platten werden getrocknet, gefolgt von der Zugabe von 40 μL MicroScint0. Die Radioaktivität wird mit einem TopCount-Szintillationszähler gezählt.
|
|
| In vivo |
TAK-632 zeigt eine überlegene orale Bioverfügbarkeit sowohl bei Ratten als auch bei Hunden. Diese Verbindung (3,9–24,1 mg/kg, p.o.) zeigt eine dosisabhängige Antitumorwirksamkeit ohne starke Gewichtsabnahme in einem Melanom-A375-(BRAFV600E)-Xenograft-Modell und einem menschlichen Melanom-HMVII-(NRASQ61K/BRAFG469V)-Xenograft bei Ratten. In einem NRAS-mutierten Melanom-SK-MEL-2-Xenograft-Modell zeigt diese Chemikalie (60 oder 120 mg/kg, p.o.) ebenfalls eine potente Antitumorwirksamkeit ohne starke Toxizität.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
