nur für Forschungszwecke
GSK2256098 FAK Inhibitor
Kat.-Nr.S8523
Chemische Struktur
Molekulargewicht: 414.89
Qualitätskontrolle
| Verwandte Ziele | EGFR VEGFR JAK PDGFR FGFR Src HIF FLT FLT3 HER2 |
|---|---|
| Weitere FAK Inhibitoren | Defactinib (VS-6063) PF-562271 (VS-6062) PF-573228 VS-4718 (PND-1186) PF-562271 HCl PF-562271 Besylate TAE226 (NVP-TAE226) PF-431396 Y15 Solanesol (Nonaisoprenol) |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 414.89 | Formel | C20H23ClN6O2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1224887-10-8 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | GTPL7939 | Smiles | CC1=NN(C(=C1)NC2=NC=C(C(=C2)NC3=CC=CC=C3C(=O)NOC)Cl)C(C)C | ||
Löslichkeit
|
In vitro |
DMSO
: 83 mg/mL
(200.05 mM)
Ethanol : 83 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
FAK
0.4 nM(Ki)
|
|---|---|
| In vitro |
GSK2256098 wurde entwickelt, um die FAK-Aktivität durch die gezielte Hemmung der Phosphorylierungsstelle von FAK, Tyrosin (Y) 397, zu hemmen. Nach einer 30-minütigen Inkubation hemmt diese Verbindung die FAK-Aktivität oder die Y397-Phosphorylierung in Krebszelllinien, OVCAR8 (Eierstock), U87MG (Gehirn) und A549 (Lunge), bei IC50-Werten von 15, 8,5 bzw. 12 nM. Darüber hinaus deuten die Daten darauf hin, dass die zelluläre Hemmung von FAK durch diese Chemikalie bereits nach 30 Minuten in kultivierten Zellen erfolgen und bis zu 12 Stunden in Maus-Tumor-Xenotransplantaten anhalten kann. Ihre Hemmung der FAK-Kinase-Aktivität kann die Akt- und ERK-Aktivität verringern. Die PI3K/Akt- und ERK-Signalwege tragen zum Zellüberleben bei, was einen pharmakologischen Wert dieser Verbindung bei der Abschwächung abnormaler Überlebenswege in spezifischen Arten von PDAC-Zellen impliziert. Sie kann die Apoptose in L3.6P1-Zellen über Caspase-9/PARP-bezogene Wege fördern. Sie schwächt abnormes Wachstum und aberrante Motilität von PDAC-Zellen auf eine FAK-spezifische Weise ab. Diese Verbindung hemmt auch Wachstum, Migration und Invasion und induziert Apoptose in einer Untergruppe von GBM-Zelllinien. |
| In vivo |
Pharmakokinetische (PK-)Studien an Mäusen und Ratten mit intakter Blut-Hirn-Schranke zeigen, dass die Penetration von GSK2256098 in das ZNS gering ist. Es erreicht jedoch Konzentrationen im Tumor von Patienten mit GBM (Glioblastom), die diejenigen der präklinischen Aktivität übersteigen. Diese Verbindung hat ein akzeptables Sicherheitsprofil, weist Hinweise auf eine Zielbindung bei Dosen bei oder unter der MTD (maximal tolerierte Dosis) auf und zeigt klinische Aktivität bei Patienten mit Mesotheliom, insbesondere bei solchen mit Merlin-Verlust. Im orthotopen Mausmodell von Ishikawa führt die Behandlung mit dieser Verbindung zu geringeren Tumorgewichten und weniger Metastasen als bei Mäusen, die mit Hec1A-Zellen inokuliert wurden. Mit dieser Chemikalie behandelte Tumoren weisen im Ishikawa-Modell eine geringere Mikrovaskulardichte (CD31), eine geringere Zellproliferation (Ki67) und höhere Apoptoseraten (TUNEL) auf als im Hec1a-Modell. Es könnte für Patienten mit PTEN-mutiertem Gebärmutterkrebs therapeutisch vorteilhaft sein, und PTEN stellt einen potenziellen prädiktiven Biomarker dar. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | p-CHK1/ CHK1 / γH2AX / c-PARP PTEN / p-AKT / AKT / pY397-FAK / FAK |
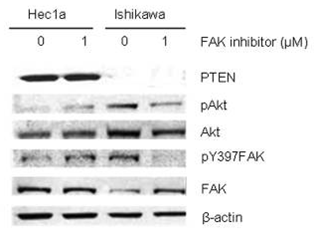
|
26295308 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT02551653 | Completed | Hypertension Pulmonary |
GlaxoSmithKline |
November 17 2015 | Phase 1 |
| NCT01938443 | Completed | Cancer|Neoplasms |
GlaxoSmithKline |
November 18 2013 | Phase 1 |
| NCT01138033 | Completed | Cancer |
GlaxoSmithKline |
July 27 2010 | Phase 1 |
| NCT00996671 | Completed | Cancer |
GlaxoSmithKline |
November 6 2009 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
