nur für Forschungszwecke
E7080 (Lenvatinib) VEGFR Inhibitor
Kat.-Nr.S1164
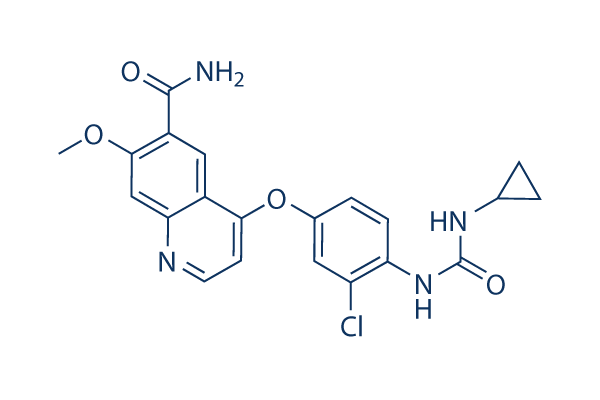
Chemische Struktur
Molekulargewicht: 426.85
Qualitätskontrolle
Produkte, die oft zusammen verwendet werden mit E7080 (Lenvatinib)
| Verwandte Ziele | EGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Weitere VEGFR Inhibitoren | SAR131675 SU 5402 Cediranib (AZD2171) Vatalanib (PTK787) 2HCl Anlotinib (AL3818) Dihydrochloride Linifanib (ABT-869) Apatinib (YN968D1) Apatinib (YN968D1) mesylate Ki8751 ZM 323881 HCl |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| TPC-1 and K1 cells | Function assay | 50 μM | 24 h | The inhibitory effects of lenvatinib on the viability of both cell lines were not influenced by the leptin treatment. | 30906321 | |
| ATC cells | Function assay | 1, 25 and 50 μM | 72 h | Phosphorylated/non-phosphorylated Akt or ERK1/2 proteins (evaluated by ELISA) in lenvatinib-treated samples were significantly reduced in ATC cell cultures. | 29517103 | |
| HCC cell lines Hep3B2.1-7, HuH-7, and JHH-7 | Proliferation assay | 6 days | Lenvatinib showed selective and potent antiproliferative activity against the HCC cell lines Hep3B2.1‐7, HuH‐7, and JHH‐7, with IC50 values of 0.23, 0.42, and 0.64 μmol/L, respectively. | 29733511 | ||
| HT29 cells | Cytotoxicity assay | 25, 50 nM | 72 h | cytotoxic dose: 50 nM and noncytotoxic dose: 25 nM | 24815456 | |
| DX3 and U2OS cells | Function assay | 1 μM and 10 μM | 16 hours | Lenvatinib inhibit tumor cells migration and invasion at concentrations that both inhibit its known targets and are achievable clinically. | 21781317 | |
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 426.85 | Formel | C21H19ClN4O4 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 417716-92-8 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | E7080 | Smiles | COC1=CC2=NC=CC(=C2C=C1C(=O)N)OC3=CC(=C(C=C3)NC(=O)NC4CC4)Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 20 mg/mL
(46.85 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
RET
VEGFR2/KDR
(Cell-free assay) 4.0 nM
VEGFR3/FLT4
(Cell-free assay) 5.2 nM
VEGFR1/FLT1
(Cell-free assay) 22 nM
PDGFRβ
(Cell-free assay) 39 nM
FGFR1
(Cell-free assay) 46 nM
PDGFRα
(Cell-free assay) 51 nM
Kit
(Cell-free assay) 100 nM
|
|---|---|
| In vitro |
E7080, als potenter Inhibitor der In-vitro-Angiogenese, zeigt eine signifikante Hemmwirkung auf die VEGF/KDR- und SCF/Kit-Signalübertragung. Gemäß den In-vitro-Rezeptortyrosin- und Serin/Threonin-Kinase-Assays hemmt diese Verbindung Flt-1, KDR, Flt-4 mit einer IC50 von 22, 4,0 bzw. 5,2 nM. Zusätzlich zu diesen Kinasen hemmt diese Verbindung auch FGFR1- und PDGFR-Tyrosinkinasen mit einem IC50-Wert von 46, 51 bzw. 100 nM für FGFR1, PDGFRα und PDGFRβ. Diese Verbindung hemmt potent die Phosphorylierung von VEGFR2 (IC50, 0,83 nM) und VEGFR3 (IC50, 0,36 nM) in HUVECs, die jeweils durch VEGF und VEGF-C stimuliert wird. Eine aktuelle Studie zeigt, dass die Behandlung mit dieser Verbindung (sowohl bei 1 μM als auch bei 10 μM) zu einer signifikanten Hemmung der Zellmigration und -invasion führt, indem sie die FGFR- und PDGFR-Signalübertragung hemmt. |
| Kinase-Assay |
In-vitro-Kinase-Assay
|
|
Tyrosinkinase-Assays werden mittels HTRF (KDR, VEGFR1, FGFR1, c-Met, EGFR) und ELISA (PDGFRβ) unter Verwendung der rekombinanten Kinasedomänen der Rezeptoren durchgeführt. In beiden Assays werden 4 μL serieller Verdünnungen dieser Verbindung in einer 96-Well-Rundplatte mit 10 μL Enzym, 16 μL Poly(GT)-Lösung (250 ng) und 10 μL ATP-Lösung (1 μM ATP) gemischt (die Endkonzentration von DMSO beträgt 0,1%). In den Wells für Blanks wird kein Enzym hinzugefügt. In den Kontroll-Wells wird kein Prüfartikel hinzugefügt. Die Kinase-Reaktion wird durch Zugabe von ATP-Lösung zu jedem Well initiiert. Nach 30-minütiger Inkubation bei 30°C wird die Reaktion durch Zugabe von 0,5 M EDTA (10 μL/Well) zur Reaktionsmischung in jedem Well gestoppt. Verdünnungspuffer, der für den jeweiligen Kinase-Assay geeignet ist, wird zur Reaktionsmischung hinzugefügt. Im HTRF-Assay werden 50 μL der Reaktionsmischung auf eine 96-Well 1/2-Fläche schwarze EIA/RIA-Platte überführt, HTRF-Lösung (50 μL/Well) wird zur Reaktionsmischung hinzugefügt, und dann wird die Kinaseaktivität durch Messung der Fluoreszenz mit einem zeitaufgelösten Fluoreszenzdetektor bei einer Anregungswellenlänge von 337 nm und Emissionswellenlängen von 620 und 665 nm bestimmt. Im ELISA werden 50 μL der Reaktionsmischung in Avidin-beschichteten 96-Well-Polystyrolplatten bei Raumtemperatur 30 Minuten lang inkubiert. Nach dem Waschen mit Waschpuffer wird PY20-HRP-Lösung (70 μL/Well) hinzugefügt und die Reaktionsmischung 30 Minuten lang bei Raumtemperatur inkubiert. Nach dem Waschen mit Waschpuffer wird TMB-Reagens (100 μL/Well) zu jedem Well hinzugefügt. Nach einigen Minuten (10–30 Minuten) wird 1 M H3PO4 (100 μL/Well) zu jedem Well hinzugefügt. Die Kinaseaktivität wird durch Messung der Absorption bei 450 nm mit einem Mikroplattenleser bestimmt.
|
|
| In vivo |
Bei oraler Verabreichung in einem H146-Xenograft-Modell hemmt Lenvatinib (E7080) das Wachstum des H146-Tumors bei 30 und 100 mg/kg dosisabhängig und führt bei 100 mg/kg zu einer Tumorregression. Darüber hinaus verringert diese Verbindung bei 100 mg/kg die Mikrovaskulardichte stärker als die Behandlung mit Anti-VEGF-Antikörpern und Imatinib. Sie hemmt signifikant das lokale Tumorwachstum in einem MDA-MB-231-Mamma-Fettpolster-Modell (m.f.p.) mit RTVs (berechnetes Tumorvolumen an Tag 8/Tumorvolumen an Tag 1) von 0,81 und reduziert sowohl Angiogenese als auch Lymphangiogenese etablierter metastatischer Knötchen des MDA-MB-231-Tumors in den Lymphknoten. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | Vimentin / E-cadherin / Snail / Zeb1 β-catenin Ki-67 / Cyclin D1 / CDK4 / p21 / p53 / Apaf-1 / p-NFκB / Bcl-2 / Cleaved-caspase 3 phospho-RET phospho-FGFR1 / FGFR1 /phospho-FRS2 / FRS2 / phospho-MEK / phospho-ERK |
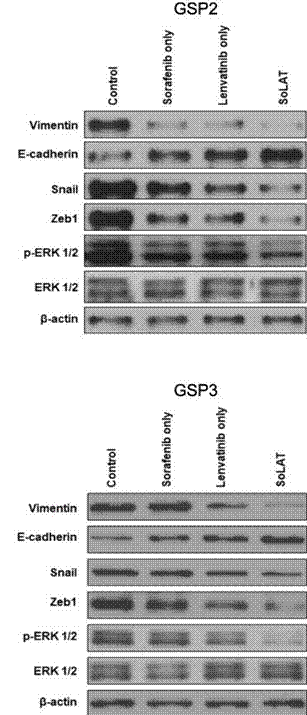
|
30286728 |
| Growth inhibition assay | Cell viability |
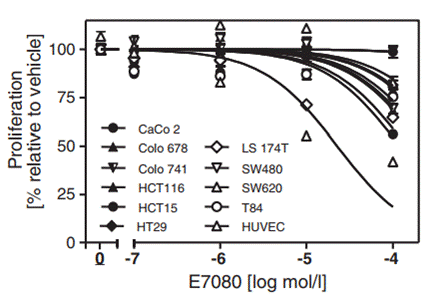
|
25425971 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT06161558 | Not yet recruiting | Neoplasms |
National Cancer Institute (NCI)|National Institutes of Health Clinical Center (CC) |
May 15 2024 | Phase 1 |
| NCT05846724 | Not yet recruiting | Kaposi Sarcoma|Classic Kaposi Sarcoma|Refractory Kaposi Sarcoma |
Fondazione IRCCS Ca'' Granda Ospedale Maggiore Policlinico |
February 1 2024 | Phase 2 |
| NCT05903833 | Not yet recruiting | Recurrent Vulvar Cancer|Persistent Vulvar Cancer|Metastatic Vulva Cancer|Locally Advanced Vulvar Cancer |
AGO Research GmbH |
January 1 2024 | Phase 2 |
| NCT05901194 | Not yet recruiting | Hepatocellular Carcinoma Non-resectable |
Assistance Publique - Hôpitaux de Paris|Laboratoire EISAI |
June 2023 | Phase 1|Phase 2 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
